������ǰ���˂�����l�F��������Ⱦ�İ��Y���˵Đ����[�����Ա���������������ע�会���ί����Y�IJ��ԡ���ǰ��һЩ�ض�����������ί����Y��������Ҳ�ɞ鿹���о������c�����磬ɳ�T�Ͼ����п���Ч��������ֱ�ӿ�����������
��������ֻ���ڵ����։��ėl�������L����ȱ�������ĽM���С����w�[���д���Ѫ����ͨ����ͽM�������ą^���e�����څ��������L����ֳ���@�o�\�Å������ί��[���ṩ����Ȼ�����뷽�������Dž������H���خ��Ե����ֺʹݚ��[���ķ����^�����[�������^��İ��������ò������⅒���������ԉľҡ��ⶾ�ж��Ȳ��Y����ȫ���}Ҳ�ǻ��څ��������ί����g�����R���D���ıډ�֮һ��
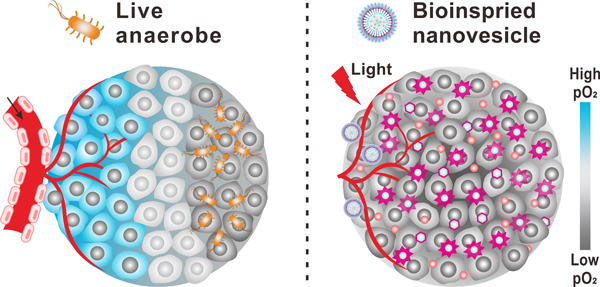
������Ͼ���W���W�����WԺ�߷��ӻ��W�c����W����Ⱥ�|�����������_�R�{��W����ɽ��У�c�����_�R�{������W�������t�W����ϵ���������܆��l�څ�������һЩ���ԣ���ͬ�аl��һ�N�ϳ��{�����������܉�ģ�M�������Ĺ��ܣ����F�����f�����@�N�{����������������߀ԭ������ƽ��l���ļ������^������һ���ù��մ���ƽ�⣬�����@ʾ��һϵ�Ѕfͬ�����������������Ķ�������������Ч��
���@��о��У������������{�������܉����[���ą����^�������������������߀�����[���к��m���셒���h�����M���|�l����ጷ�ˎ�ﲢ����ˎ��Ŀ����������Ƶõļ{�����ݲ��H�������h�����У�߀�܉�ͨ�^������ί����g�������D׃�ɻ��������|��ROS�������S��������Ķ�����Įa�������h�����{������������ą����l�����^�mͨ�^����߀ԭ�^�̶��������������{�����ݱ��⣬ጷų��\�d��ˎ��Tirapazamine���@�N����߀ԭ�Ϳ��[��ˎ�����څ����l���°l������߀ԭ�����a���������ɻ����M�����������������{������ע�䵽�ΰ�����ģ���w�Ⱥ����������{���wϵ����Ч�����[�����L���о��ˆT��ʾ���������Mһ���u��ԓ�oˎ�wϵ���L�ڶ��ԡ���ԓ�о�������푑�ˎ���f��ϵ�y���OӋ�ṩ���µIJ��ԡ�ԓ��������������߀�ܝ��������ί��c�������P�ļ���������ȱ�F�����L��

�Ͼ���W���W�����WԺ��ʿ�о����X�̸����S���Ԟ�Փ�IJ��е�һ���ߡ�ԓ�����õ�������Ȼ�ƌW�����L���W�ߺ̈́����о��F��Ŀ���Ї�������W�����Ŀ�Լ��Ͼ���W���㲩ʿ�о���������������Ӌ��A��֧�֡����P�����l����Angew. Chem. Int. Ed. 2017, DOI: 10.1002/anie.201611783�������x����c���£�Hot Paper���̓ȷ������¡�
ԭ��朽ӣ�http://onlinelibrary.wiley.com/doi/10.1002/anie.201701131/full
