�ɹ������и��`���ȡ����r�ɿغ��O�了�εȃ��c��Ŀǰ����K�ɹ�����Ҏģ�R�����õĆ��}�Ǵ���ȱ��^�\�����F�ɹ������ȵ�ͻ�ƌ�ԓ���g���R���D�����зdz���Ҫ�����x���c��Ҋ��^��400-700 nm���͂��y�Ľ��t��I�^��700-950 nm����ȣ����t��II�^��1000-1700 nm�����и����ĽM�����ա�ɢ�䡢�l����l�ɹ⣬�����������߽M���Ĵ�����������������t��I�^���l�ͽ��t��II�^�l��ij���ģʽ�ܵ��ˏV�����Pע����һ�N�෴�ij�����ԣ������t��II���l�����t��I�l���Пo����������L���L���t��⣨��1300 nm���ĘO�����������˂�������Ч�ؽ�������M���������ã����F��ӵĸ߷ֱ��ʳ���
�������ۿƼ���W���Ʊ���Ժʿ���㽭��W���X�E�����������״Έ���˾ۼ��T���l�⣨AIE����������1300 nm���t��II�^���l�ͽ��t��I�^�l��Ļ��w�p���ӳ������������X���ij�����ȳ��^1000 ��m����ǰ�ڵ��о������У��Ʊ���Ժʿ�Fꠌ��F�˻���AIE���ϵĽ��t�������ACS Nano, 2017,11, 7177�������t��II�^�ɹ����Adv. Mater., 2018, 30, 1706856���Լ��ɹ�-���pģʽ�ɿس����ί���Nat. Commun., 2018, 9, 1848���ȡ��c��ͨ�ğɹ������ȣ��p���ӟɹ����ģʽ����������һЩ�����c���������l�������͡���p��С���M����������������ֱ��ʸߵȡ����y�p���ӳ���ļ��l������Ҫλ��680-1040 nm�IJ��L�������l����V�t��Ҫλ��700 nm���µĿ�Ҋ�Ⲩ�Σ�����䴩���ֻ�Ўװ��ף��D1�����о��Y��������1300 nm��1700 nm�@�ɂ����L�Ĺ������С�ļ��l˥�p���|�����Ԍ��F���õĴ���Ⱥͳ���Ч����Ȼ�������y�ЙCȾ�����R���ۼ����ɹ��硱��ACQ���Ȇ��}�������ǹ�ܗ�Ա��^��Ľ��t����Ӹ������R�@һ���}��ʹ�L���L���l���p���ӳ���׃�÷dz����y��

�D1. ��ͬ���l�Ⲩ�L���X���������ʾ��D
���˽�Q���φ��}�������OӋ���ϳ��ˡ��з���Π�Ľo-���w��D-A����AIE���ӣ��D2����ԓ���ӵ����g�����Ǿ��к�D-A���õ�ƽ��Y���������ڌ��F����p�������ս��档�����Ϻ��ж������������D�ӵķ����D�ӣ�������Ч�ؿ˷�ACQ���}�������FAIE���ԣ��õ��ߟɹ����Ӯa�ʡ����ߌ�ԓAIE���Ӱ����ɳߴ�s��35 nm�ļ{�����ӣ����������λ��635 nm���l�䲨�L�t���Ը��w700-1200 nm�ķ�����ԓAIE�{�����Ӿ��кܺõķ����ԣ��俹��Ư�Ϳ�����������RONS������������FDA�J�C������ݼ�G��ICG��Ⱦ�ϡ�

�D2. ���з���Π��AIE���ӽY���ͼ{�����ӵ����|
AIE�{�����ӵ�������ղ��L��635 nm����ɱ�����λ��1300 nm�ġ��������ڸ�������1300 nm�w�뼤�����ļ��l�£�AIE�{�����Ӿ��к��ğɹ�l�䣨�D3����ԓAIE�{�����ӵğɹ����Ӯa�ʿ����_��13.9%�����p�������ս����1.22×103 GM�����ڳ��õ��ЙCȾ�ϡ���AIE�{������ͨ�^β�o�}ע�뵽�����w�Ⱥ���1300 nm�w�뼤��ļ��l�£�������X���p���ӟɹ��@����Y��������1065 ��m��ȵ�ë��Ѫ����Ȼ������Ҋ�����X�����|�^��>840 ��m���ͺ��R�w�^��>960 ��m�������Ԍ��F3.5 ��m�ij��߷ֱ��ʣ��D4������Ŀǰ���w���p���ӟɹ��������Ч����ͬ�r���X��Ѫ�ܵ����S�Y��Ҳ������Ҋ��������Ѫ�ܡ�ë��Ѫ���Լ�Ѫ���B�Ӳ�λ�ȡ�ԓ�p���ӳ���Y����Ҫ������1300 nm���t��II�^���l�ͽ��t��I�^�l������|�����ڂ��y�Ľ��t��I�^���l�Ϳ�Ҋ��^�l��ģʽ��ԓ�о��Y���������ЙCAIE���Ͽ��Ԍ��F�c�o�C�댧�w�����c���������ij���Ч�������ЙC���ϵ������t�W�����ṩ���µ�˼·��

�D3. AIE�{�����ӵ��p���Ӽ��l���|
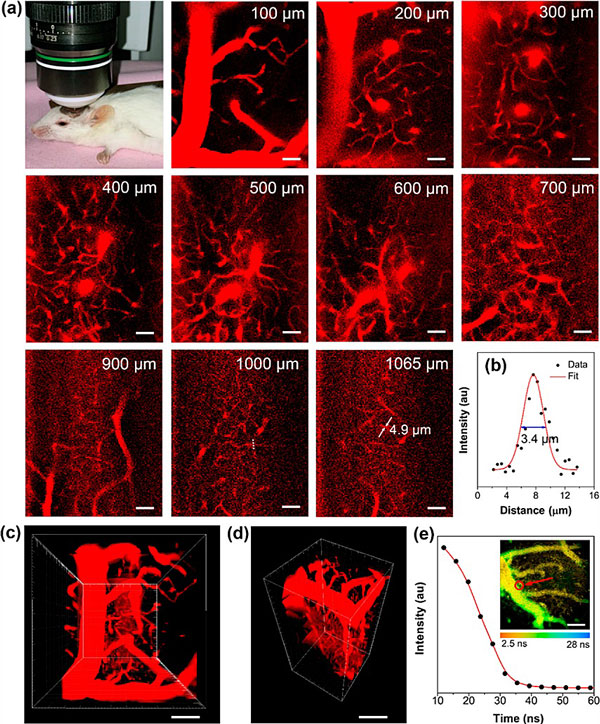
�D4. ���w�����X�����p���ӟɹ��@����
�@һ�ɹ����ڰl����ACS Nano �ϣ����µĵ�һ���ߞ���ۿƼ���W�IJ�ʿ���R�E���㽭��W���о����O������
ԓՓ�����ߞ飺Ji Qi, Chaowei Sun, Dongyu Li, Hequn Zhang, Wenbin Yu, Abudureheman Zebibula, Jacky W. Y. Lam, Wang Xi, Liang Zhu, Fuhong Cai, Peifa Wei, Chunlei Zhu, Ryan T. K. Kwok, Lina L. Streich, Robert Prevedel, Jun Qian, Ben Zhong Tang
- ���д����ڣ��w�� / �Ʊ��҈F� ACS Nano �����AIE�{���R�_ͻ���[������ - ���F���ʹ��\�� 2025-05-29
- �����ģ����ڣ��Ʊ���Ժʿ�����ڴ�W���|���ڵ� Nat. Protoc.: NIR-II���lAIE�����{�����ڷνY�˻��w��W�\�� 2025-04-18
- ������Ĵ�W�����ڣ��Ʊ���Ժʿ�F� AFM�����϶��·��Ƃ�AIE/����ľ�����ڷ��� - ������ˎ����Ⱦ���ڿ������� 2025-02-13
- ������Ĵ�W�����ڣ��Ʊ���Ժʿ/�w�����ڈFꠡ�ACS Nano��������Ĥ����ľۼ��T���l�����������ۙ�͓p���Ŀ�ҕ�� 2025-01-21
- ������Ĵ�W�����ڣ��Ʊ���Ժʿ�c�w�����ڈFꠡ�ACS Nano���C�����ۼ��T���l����ό��F�߷ֱ�������� 2025-01-07
- �������Ʊ���Ժʿ/�������賯 AM������AIE���Լ{�ͺ�ˮ���z�Ŀɴ�������ʽ��Ϣ-���в��� 2024-03-23
- ������ƽ����n�}�M Biomaterials��һ�N���Ͷ�ģ�Bˮ���zƤ��늘O 2022-01-05
