�����������W(xu��)�W(xu��)�����H피��ڿ���Journal of the American Chemical Society����JACS�����l(f��)���A�пƼ���W(xu��)��h��늇����о�������W(xu��)�Ľ����c���W(xu��)�c�����W(xu��)Ժ���\�����ڡ��Ͼ��]늴�W(xu��)���ϿƌW(xu��)�c���̌W(xu��)Ժ�w��(qi��ng)���ں���Փ�ġ���(x��)����Ĥ���D(zhu��n)�\(y��n)�ǹ��r�B�ӵğ������t�ɹ�{���������ڕr�g�ֱ�İl(f��)�����������Cell-Penetrating Peptides Transport Noncovalently Linked Thermally Activated Delayed Fluorescence Nanoparticles for Time-Resolved Luminescence Imaging��������W(xu��)�Ľ��ڡ����\���������w��(qi��ng)�����鹲ͬͨӍ���ߣ��A�д���h��늇����о����IJ�ʿ����ɲ��ͻ��W(xu��)�c�����W(xu��)Ժ��ʿ�������Փ�Ĺ�ͬ��һ���ߣ��A�д��Փ�ĵ�һ��λ��
�����L�������l(f��)�B(t��i)�ğɹ���̽��ڕr�g�ֱ棨time-resolved����������о�����Ҫ�đ�(y��ng)�á������ڷ�(w��n)�B(t��i)�ɹ���r�g�T�س���time-gated imaging����ɹ��������luminescence lifetime imaging���ȕr�g�ֱ漼�g(sh��)�����x���ԙz�y�L�����İl(f��)�⣬�_(d��)��ȥ��ɢ���������ԟɹ�ɔ_��Ŀ�ġ������(sh��)�L�������l(f��)�B(t��i)������̽ᘞ��^�ɽ���������o�C(j��)�������Ӳ��ϣ���Ҫ������ϡ����˱����^�ɽ��ٵĶ������ã��˂�һֱ�ڰl(f��)չ�o���ٵ��L�������l(f��)�B(t��i)���ϡ����t�ɹ⣨Thermally Activated Delayed Fluorescence��TADF�������ǽ�Щ��l(f��)չ��һ���Ҫ�ķǽ��ٟɹ���ϣ����ЙC(j��)�l(f��)����O���I(l��ng)��(y��ng)�ÏV�����@��ϵ��L�����ɹ�Դ�ڼ��l(f��)���ؑB(t��i)�ķ���ϵ�g�ZԽ�������ͨ�������������������cһ����^�ɽ��������ļ��l(f��)�B(t��i)�����ஔ(d��ng)������Ƿǽ������L�������l(f��)�B(t��i)̽ᘵď�(qi��ng)�����x��
Ȼ���������\(y��n)������(d��o)�����t�ɹ⼤�l(f��)�B(t��i)�ķ�ݗ���ԥ�����Ҽ��l(f��)���ؑB(t��i)�ױ�������⧜磬��(d��o)�������ܽ��B(t��i)�µĵİl(f��)���^�����y���\(y��n)������������С���Щ���mȻ��һЩ�����Lԇ�����t�ɹ����̽����ڕr�g�ֱ����������Ǒ�(y��ng)�÷����dz����ޡ���ˣ��˂��l(f��)չ�����t�ɹ�{��̽ᘣ�ʹ�Ã��H�ۺ��������ˮ�����t�ɹ�����γɼ{�����ӣ��M(j��n)��������������ǣ��@Щ�{�����Ӵ��ȱ�����������ԣ����ܿ����M(j��n)�뼚(x��)������������Ҫ��(sh��)С�r�ķ����r�g�������ڌ��r�ɹ����
���������������������״Ό���(x��)����Ĥ�ģ�Cell-Penetrating Peptides���������t�ɹ�{�����ӵļ�(x��)����Ĥ�D(zhu��n)�\(y��n)����(g��u)����һ�l�����۱������ᡢ���۸ʰ���Ͱ˾۾�����M�ɵ�һ�l���H�Դ�Ĥ�ģ����ڽM�����t�ɹ�{�����ӣ��D1����ԓ��朵İ˾۾�����Ĥ���ã����۱����������ˮ�ˣ���ͨ�^�ǹ��r����ˮ���ýY(ji��)��һЩˮ���ܵ����t�ɹ���ӡ�ͨ�^һ���ԽM�b�ķ�����ԓ��朿����c������(j��ng)�����ˮ���t�ɹ���ӷքe�M�b�γɲ�ͬ�ɹ��ɫ�ļ{�����ӡ�

�D1�����H�Դ�Ĥ���c���t�ɹ���ӽM�b�γɼ{������
��(j��ng)�^������(y��u)�������γ�������90-300 nm������(n��i)�����ӣ����@Щ���ӱ��渽���Ĵ�Ĥ�������£��@Щ���ӿ����^�÷�ɢ��ˮ��Һ�У��������^���M(j��n)�뼚(x��)�����ɹ�۽��������ʽ��(x��)���g(sh��)�Y(ji��)����������(j��ng)�^5��犷����Ϳ��ԙz�y����(x��)����(n��i)���@Щ���ӵğɹ���̖������f���˴�Ĥ�Ŀɽ錧(d��o)�ǹ��r�B�ӵ������M(j��n)�п�Ĥ�D(zhu��n)�\(y��n)�����⣬������ˮ���Ӿۼ������Ӄ�(n��i)����������Ч���������ӵĔU(ku��)ɢ�ͷ��ӵķ�ݗ����ԥ������@Щ�������Ҝ������l����Ҳ�����L���������t�ɹ⣬�����������l���µĉ������뼉���ϣ�ͨ�^��ʮ����(sh��)�ټ{������t���@Щ�L�����l(f��)����̖�����cɢ��⡢�̉����ԟɹ�^(q��)���_�����D2�����r�g�ֱ�ɹ����Y(ji��)����������(j��ng)�^1С�r�ķ��������@���z�y����(x��)����(n��i)���L�����ɹ���̖���D3����
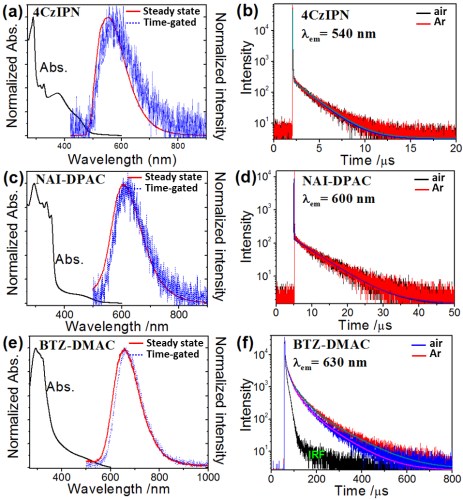
�D2���{�����ӷ�ɢҺ�����ա���(w��n)�B(t��i)�����t�ğɹ���V��a��c��e�������l(f��)���S�r�g��˥�p׃�� ��b��d��f����[4CzIPN] = [NAI-DPAC] = [BTZ-DMAC] =12.5 ��g/mL��

�D3���{���������ڕr�g�ֱ�ļ�(x��)���ɹ����[4CzIPN] = [NAI-DPAC] = [BTZ-DMAC] = 1.6 ��g/mL.
���������������Ƃ�����t�ɹ�{�����ӣ��@Щ���Ӿ����^��Ĵ�Ĥ���ʡ������ڹ��r���Ĥ�ĵğɹ�̽ᘣ�ԓ�����H��һ�l��Ĥ�Č��F(xi��n)�����N�ǹ��r�B�ӵķ����M(j��n)�뼚(x��)������������������㣬�ɱ����͡�
�@�N������������������ˮ���ӻ����ӵĿ�Ĥ�D(zhu��n)�\(y��n)��������Ҫ���F(xi��n)�е����t�ɹ�����M(j��n)�л��W(xu��)��Ϳ��Ԍ������ڼ�(x��)���ĕr�g�ֱ��������ɢ���������ԟɹ�ɔ_���������Ҫ�����x�����⣬�@�N���H�Դ�Ĥ�ĵ��O(sh��)Ӌ˼·�����\(y��n)�õ�������朵��O(sh��)Ӌ�У����ڟɹ⡢ˎ����Ӻͼ{�����ӵĿ�Ĥ�\(y��n)ݔ������Н��ڵđ�(y��ng)�á�
ԓ�����õ�������Ȼ�ƌW(xu��)����51603152��51525302��61775074��61825503�����Ї���ʿ�����2017M620315��2018T110757�����Y����
�\���P(gu��n)ע�߷��ӿƼ�

- �������C(j��)����500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ��h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��
- �Ј���300�|��PMEC China ɫ...
- ����ע�ԣ�2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ(x��n)����...
- �����ϸ��Լ��ӹ����g(sh��)Ҫ�I(l��ng)��...
- ������/���ƴ�Ժ����ƽ...
- �B�T��W(xu��)�܌W(xu��)������ Macromo...
- ɽ���܂������ڡ���(j��)���w�ɷ�...
- �A���r(n��ng)������p���ڡ�����x...
- �Ї��ƴ���Ƙ�/���������...
- �B�T��W(xu��)������ڈF(tu��n)� AFM��...
- �Ľ�ƽ�����A�ƴ�F(tu��n)�ţȽ��...
- ̫ԭ������W(xu��)�����ֽ��� Adv...
- ����κ�ܽ��ڈF(tu��n)� CEJ������...
- �Ϸ��Ƽ���W(xu��)�����w���ڈF(tu��n)�...
- ���ϴ�W(xu��)������/����Ⱥ/����...