���֧��ֲ���g(sh��)���ί������͚���Mխ����Ч�ֶΡ�Ȼ�����Թ����z���Ƃ���ϵ����Ú��֧�܃H���зdz����εĹܠ��OӋ�������c��ܵď��s�Θ�(g��u)�Ͳ�ƥ��������g(sh��)���w�Ƶ��L�U�������nj��ڃ�ͯ���߁��f���������ښ�����L���µ�֧���Ƴ��c��Q�����˽M���p�����L�U�Լ����g(sh��)��ʹ�ࡣ��ˣ��_�l(f��)���Ը���(j��)���������ƵĂ��Ի������՚��֧�ܾ��ИO����t(y��)�W�����dz�Ҏ(gu��)�����켼�g(sh��)�y�ԝM���Һĕr���F���c�t(y��)�W������Y(ji��)�ϣ�3D��ӡ���g(sh��)�邀�Ի��t(y��)����е�Ŀ��������ṩ��ǰ��δ�еęC���������ǻ��ڹ�ۺϵ�������������_���(y��u)�ķֱ��ʺʹ�ӡ�|(zh��)�������电(sh��)�ֹ�̎�����g(sh��)��DLP������ϧ���ǣ��܉�����DLP���������ݼ��ɽ�����Ϸdz����ޣ����õĿɽ���DLP��ӡ����һ�������Ե;����ԝM��Һ�w��֬�Ĵ�ӡ����(sh��)�������W�����_��������֧�ܵ�����˜ʡ�
���գ��K����(li��n)�������WԺ��ETH Zurich��ˎ�WϵJean-Christophe Leroux�����c�U�����о��T�n�}�M(li��n)�ϲ���ϵA(ch��)ndr�� R. Studart���ڡ��K������W�t(y��)Ժ��UZH��Daniel Franzen�t(y��)���Լ��K���������t(y��)ԺBrigitte von Rechenberg��������˻���DLP�Ĺ�ۺ�3D��ӡ���Ի������՚��֧�ܣ������W���������̘I(y��)�����z֧���ҿ��Ա��M����ȫ���ա��о��ˆT����D,L-�������ͦ�-����(n��i)���ɷN���w�oҎ(gu��)���ۣ��Y(ji��)�ϱ�ϩ�������ܻ��ϳ���һϵ�о��в�ͬ��������Һ�B(t��i)����Ծۺ�����ÿɼӟ�DLP��ӡ�C���ɹ����F(xi��n)���^�߷������ɽ���ۺ����3D��ӡ��ͨ�^���ɷN��ͬ�Y(ji��)��(g��u)�c�������ľۺ���������{(di��o)�أ����Եõ�һϵ�в�ͬ����ģ���͔������L�ʵ�3D��ӡ�����w�����У�������15000�����;ۺ����c������600�ľ��Ե;��ﰴ������75:25��ϕr��3D��ӡ������_���c���z�����w�������µ����W���ܣ��D 1���������@һ��(y��u)���M�ϣ������Ƃ䲻ͬ�Θ�(g��u)�͵ĸ߾���3D��ӡ֧�ܡ�

�D1. �ɽ���3D��ӡ�ۺ�����ϵĽY(ji��)��(g��u)�OӋ�����W�����c��ӡչʾ
�о��ˆT�Mһ���yԇ��3D��ӡ���ϵļ������ԺͲ�ͬ�l�����_Һ�еĽ����О顣���l(f��)�F(xi��n)ԓ���Ͼ��кܺõļ��������������c�m�˵Ľ������ԡ���37�z�϶ȵ����ᾏ�_Һ�Ѓ���5�����|(zh��)���ɓpʧ�s20%������50�z�϶��H6�ܱ�pʧ40%���ڞ���3���µ����W���ܸ�ۙ����аl(f��)�F(xi��n)��3D��ӡ֧����37�z�϶��¾��к����Ŀ������ȵĜp��������50�z�϶��H1���±���ȫʧȥ���W���ȡ��Č�����@��Ƭ���Կ��������О錧�µ����@���^׃����
�S���о��ˆT����CT����@���������m���Ä���ģ�͵Ě�ܽY(ji��)��(g��u)���OӋ��ӡ���N�����Π�Ă��Ի��ɽ���֧�ܡ����������OӋ���m���ڄ���ģ�͵�֧���f���b�ã�3D��ӡ���Կɽ���֧���״α�ֲ�뵽������w��ܡ���3D��ӡ֧����ԭλ�Ƃ���ٽ�ʹ�����ڄ����п��Ա�X�侀���r�O(ji��n)�y���о��l(f��)�F(xi��n)�ڻ��w���ǰ7��3D��ӡ֧���ڰ��Ú���в�δ�l(f��)�����@λ��׃�������ĵ�8���_ʼ֧����ʧ����ζ����u�����֧�ܱ���ܽM�����ա��M����Ƭ����������֧��ֲ���ǰ���ܚ�ܽM�������ܵ������l(f��)�����@���װY�c�p�����S��֧�ܵĽ����c���հY����u�p�p������10���װY��ʧ������Ƥ������ȫ�֏ͣ��D2�����������3D��ӡ֧�ܱ����������õ������������c�������������ܡ�

�D2. �����p�ۺ��������75/25����֬�Ă��Ի�3D��ӡ���֧�ܡ���ҕ���f�ͼ������ܽM����Ƭ��
�@��о��״Ό��F(xi��n)�����������z���W���ܵ�����ɽ���ۺ���ļ���3D��ӡ�����ɹ������ڂ��Ի�������֧�ܵ��Ƃ��c�yԇ���D3����ԓ�о��_�l(f��)��3D��ӡ�����cϵ�y(t��ng)�����Ƅ�����ɽ���ۺ����ڱ��������t(y��)���I(l��ng)��đ��ã������t(y��)��ֲ������Ի���е���M��֧�ܣ�ˎ���f���Լ�������ӵȵȡ�ԓ������ǰ���}�顰Digital light 3D printing of customized bioresorbable airway stents with elastomeric properties���l(f��)���ڇ��H֪���ڿ�Science Advances����λ�����˾��o�������u�r����The experimental results showed that the new 3D printed stents offer several advantages over the silicone stents�������Y(ji��)�������µ�3D��ӡ֧���ڲ�ͬ���惞(y��u)�ڹ����z֧�ܣ�����the work is interesting and compelling������헹�����Ȥ������עĿ������the overall study has high clinical impact and deserves publication in a leading journal�������w�о����R���Ͼ��и�Ӱ�����������피��ڿ��ϰl(f��)������
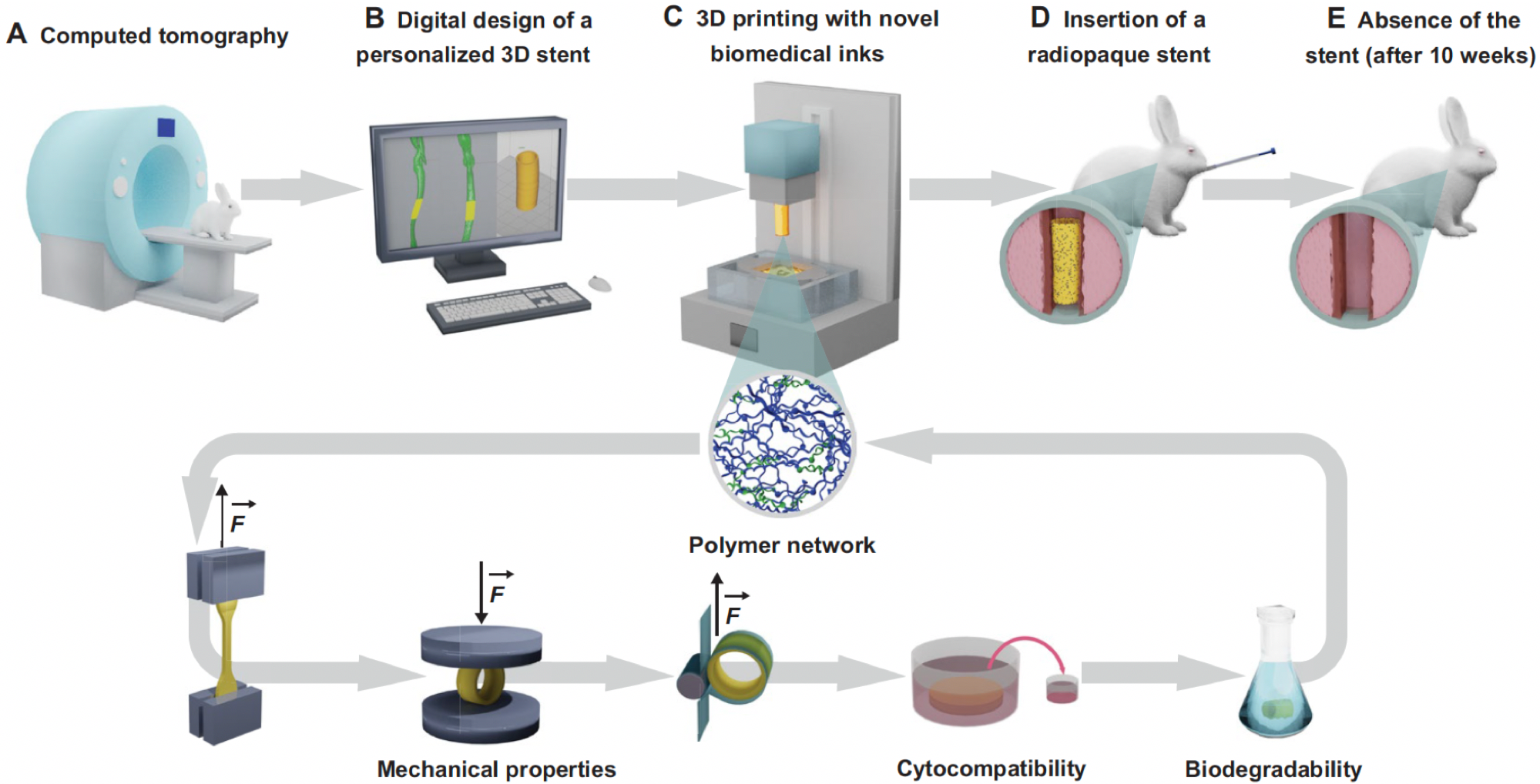
�D3. ���������յĂ��Ի�3D��ӡ���֧�ܵ��OӋ�c�Ƃ�����
ETHˎ�Wϵ��ʿ��Nevena Paunovic�c���о��T�U�����鹲ͬ��һ���ߣ�ǰ�ߞ�3D��ӡ���Ϻϳ��c��������Ҫ����ˣ����ߞ�3D��ӡ�����cϵ�y(t��ng)����Ҫ�OӋ�ߣ�ͬ�rҲ��ǰ�ߵ�ֱ�ӌ�����ETH����ϵ��ʿ��Fergal B. Coulter��3D��ӡ�D���ļ���֧���f�������OӋ���Լ�Kunal Masania���F(xi��n)������������������ڣ���3D��ӡ�C�ӟ�ϵ�y(t��ng)���OӋ�ߡ�UZH��ʿ��Anna K. Geks��Fabienne R��ber�����о��T Karina Klein��Peter W. Kronen��������Ҫ����ˡ�ETH����ϵ��ʿ��Ahmad Rafsanjani���F(xi��n)���ϵ�����W�����ڣ��ṩ���WӋ��ģ�͡�ETHˎ�Wϵ�Tʿ��Jasmin Cadalbert�c����ϵ��ʿ��Nicole Kleger����σ�(y��u)�������W��������ӡ�C�����ṩ������UZH���о��TAgnieszka Karolؓ؟�M����Ƭ�c������ETHˎ�Wϵ��ʿ���_���ṩ֧�ܿ�ҕ��������ETHˎ�Wϵ���о��TDavide Brambilla���F(xi��n)������������W�������ڣ���UZH����Brigitte von Rechenberg�քe��ԓ�Ŀ�ṩ�����ͅf(xi��)�{(di��o)���ETHˎ�Wϵ����Jean-Christophe Leroux�����µ�ͨӍ���ߣ�ETH����ϵ���� Andr�� R. Studart��UZH���t(y��)��Daniel Franzen�鹲ͬͨӍ���ߣ��քe��ԓ�о��ṩ���w��ָ����
ԓ�о�����ʿ���ҿƌW���������e�ĺ����ĿSinergia�����Y����230�f���ɣ���Jean-Christophe Leroux���ڞ�ԓ�Ŀ�Ŀ�ؓ؟�ˣ��U�����о��T���n�}�M�L��Andr�� R. Studart���ڼ�Daniel Franzen�t(y��)�������ؓ؟�ˡ�
Փ��朽ӣ�https://advances.sciencemag.org/content/7/6/eabe9499
�n�}�M朽ӣ�https://galenik.ethz.ch/people.html
- �б���W����/�����ɡ�����������С�� Compos. Part B��3D��ӡ�������³ɹ�-���������ϽY(ji��)��(g��u)�OӋ���Ƃ估�C���о� 2025-06-06
- �A��������ِ�A�����n�}�M CEJ������3D��ӡ���g(sh��)��(g��u)���Ŀɴ��������|�XĦ��늂������ڲ��ϸ�֪�I(l��ng)��đ��� 2025-05-29
- ���������WԺ�߂������n�}�M�c������ Science���������(q��)�ӵĻ��w�����3D��ӡ���g(sh��) 2025-05-09
- �Ͼ���W���x����ڈF� Angew: �Aƫ������⼤��IJ����Q��ۺϷ������ںϳɾ��ЈAƫ��l(f��)����ԵIJ��� 2025-03-09
- ����������W�u��ȫ���ڈF� CEJ�����ڽ��t���ۺϵ����w���3D��ӡ���g(sh��) 2025-02-24
- �㹤�����ܡ�����Ժꐼ� AHM�����ڟɹ�ۺ����ԽM�b���Ԙ�(g��u)��θʳ�ܷ����\�༈�������� 2025-01-16
- ���Ӌ�����ڡ����i�о��T�F� Nat. Commun.����p�Y(ji��)������ë�ǵ���/�����w�S������������պ��������ݵ���ƿp�� 2025-03-31
�\���P(gu��n)ע�߷��ӿƼ�

- ���HƷ�ơ�ǰ�ؕ��h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��
- �Ј���300�|��PMEC China ɫ...
- ����ע�ԣ�2025����������չ...
- ���a���υ��^�A��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ����...
- �����ϸ��Լ��ӹ����g(sh��)Ҫ�I(l��ng)��...
- �Ї������ƌW��36%���١���...