���Ӿ�ٿؼ��gͨ�^���w�h���и�Ч����-��-�Cе������Ķ����ٿ،���ʩ���g�ӹ�W�����F�h�̹�W�ٿء��c���y�����ȣ����Ӿ�ٿؼ��g�����ٿع��ʵ͡���p��С�ȃ��ݡ���ٿع����@��������ҪԴ����Ч�Ĺ���D�QЧ�������w�ھ���ض��ݶȈ����@���ğ�Ӿ�w��������ͨ�^�����OӋ�ض��ݶȈ��͘���������������Ӿ�ٿؼ��g�Ɍ��F�������w�ĸ߾��Ȳٿأ����{�w���������w��������w�����ۺ����w������Ӿ�w�����:����������ӵȡ�
���գ����A��W�O�鲨���ں����պ��������ڡ�ACS Nano���ڿ��ϰl�����}�顰Opto-Thermophoretic Manipulation���ľC�����£�ԓ�C�����U����Ӿ����C�Ƴ��l��ϵ�y��B�˹��Ӿ�ٿؼ��g���_�l���lչ�ͼ��g�����������Y�������z�w�ƌW�������ƌW���I��đ��ð������D1�������⣬���ߌ����Ӿ�ٿؼ��g�İlչǰ���M����չ�������؏��{�����ԓ���g����������Ԍ����،����������ƌW�I���õ���Ҫ�Բ��ṩ���������о�˼·��

�D1 ���Ӿ�ٿؼ��g������C�ơ����g���c�����ð���
���z�w�ƌW�I���z�w�M�b��ӡˢ���������z�w�������Ƃ������Ҫ���x�����Ӿ�M�b���gͨ�^�����ɢ�������z�w�w���g���I�������ɹ����F���ڲ�ͬ�z�w�w���Ķ��ӻ��M�b��ͨ�^�����OӋ�z�w�w���ijߴ硢���|�����gλ�÷ֲ����Ɍ��F�����Գ������ӵĿ���M�b���D2����ͨ�^�Mһ���{�؟�늈������������μ��g��ʹ�z�w�w���˷��w��-�����g�Ą݉������Ԍ��F�z�w���ϵ��D����ӡˢ��

�D2 ���Ӿ�M�b���g�����Գ�������
���⣬�������:���ͷ����ڜضȈ���Ҳ�ձ���ڟ�Ӿ�w�ƬF���Ӿ�ٿؼ��g�������ƌW�I�������Խ��Խ��Ҫ�Ľ�ɫ�����磬���ù��Ӿ�ٿؼ��g�����y�����Y��ӛ������ݣ��Ɍ��F�����ٰ���ǰ���ٰ��Ȱ��Y��̽�y���D3�������⣬ͨ�^�O�y��ͬ���ӽY��ǰ��ɹ⏊�ȵ�׃�����Ɍ��F�����g����õ�̽�y��
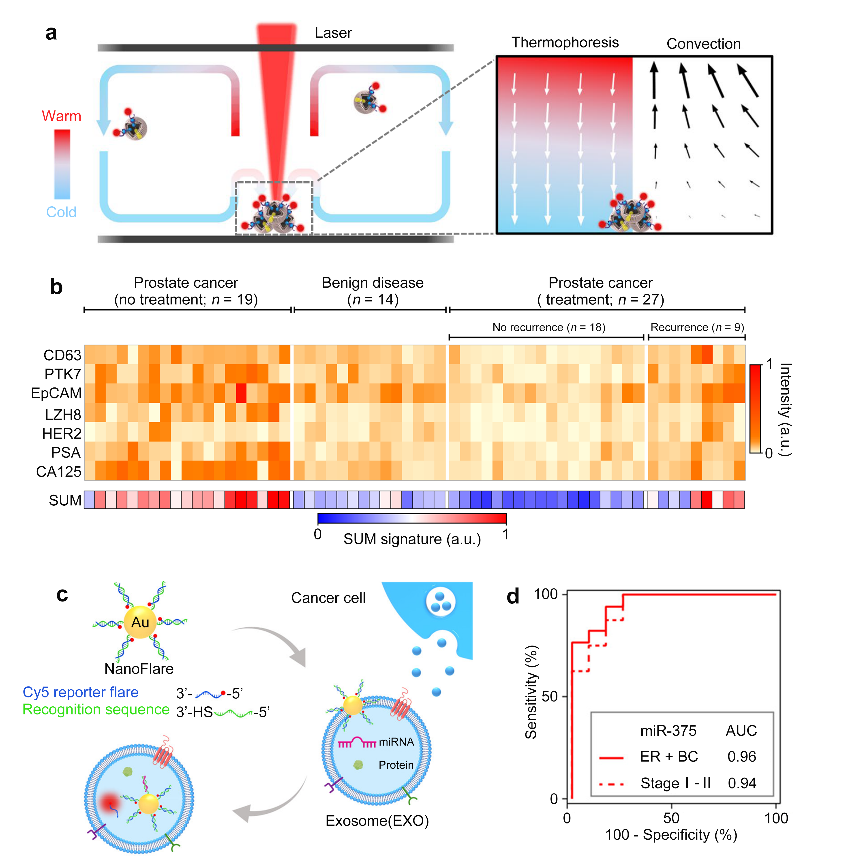
�D3 ���Ӿ�ٿؼ��g���ڰ��Y�\��
ԓՓ�ĵĵ�һ���ߞ����A��W���܃x��ϵ��ʿ�����ٷ���ͨӍ���ߞ��O�鲨���������պ���������
Փ��朽ӣ�https://pubs.acs.org/doi/10.1021/acsnano.0c10427
- ���o���P��
