�^�����ɽ����ˮ���z֮���ɄӑB�߷��ӾW�j�M�ɵ�ˮ���z�������䪚�ص����������������������Pע��һ���棬�@ӑBˮ���z�����������S�������B���ϣ�ʹ�ü�������ȵ�𤸽�c�չ���О��п��ܲ��ܲ��Ͻ�������ƣ���һ���棬�@ӑBˮ���z���ص����W���ܣ�Ҳ�o�䌍�H���Î����˱����������ע���c���ޏ����ܣ�ʹ�øɼ���-ˮ���z�ͺ�ע�������ɞ���Ӹ�Ч���ί��ֶΡ�߅�������ڈF�����������-���w����w��Host-Guest-Macromer, HGM�����ԣ����������̈́ӑBˮ���z���_�l�������ڸɼ������B�c�M�������I��đ��á�����F����ڵ��о��аl�F��ͨ�^������-���w����ý����������ӣ�һ��������������W�����ԣ�ʹ��������L�r�g�ɼ������B�c�о�����һ���棬����-���w����Ä����W�О飨����-���w���Y�j�����ʳ�������Ӱ푣�ԓ������������õ����Sˮ���z���F���������W��ɢ����ע��������Σ��Լ����S���ټ�����������c�����@һ��µ��о��У�ԓ�F��c������Ĵ�W����ϵ����һ�����F������Mһ��̽ӑ������-�w���Y�j�ϵĄ����W�����������О��Ӱ푡�
��D1��ʾ�����ˆΪ�����HGM�ӑBˮ���z�������������ԣ������@����׃������W�����ԣ�ԓ�F��OӋ�˃ɷN���w��������ADA��đ��CA��������|�ᣨHA������HA-ADA��HA-CA��ͬ�r�����˴��M����𤸽���@�ɷNHA���M����RGD���ԓ�о��l�F����HGM���ԣ�ͨ�^�ɽ�b-�h������CD���cHA-ADA��HA-CA��j���γɵ���-���w����w������ͨ�^�⽻�Ƃ�����ɼ����ij�����ˮ���z��CD-ADA��CD-CA�����w�Y���w��������ğ����Wƽ�ⳣ����Keq����Ȼ��CD-ADA�Ą����W������kon, koff���h����CD-CA�����W������������õ��ăɷN�����wˮ���z���քe��CD-ADA��CD-CA�Y���w�����mȻ���F��������o�B���W����������Û�О飬����ģ���ȣ�����ͬ�rչ�F�Į��ĄӑB���W�������p��ģ�������C����CD-ADA����ˮ���z���и��ߵĄӑB���|�����P��Ҫ���ǣ���CD-ADA�齻ˮ���z�У��ɼ������F����ͬ�����ij������S�Ǡ��չ�����b��18С�r��������CD-ADA�齻ˮ���z�У��ɼ��������S�չ�t�@���^�����@���l�F���������w������ˮ���z�������潻�Ą����W���������b��ˮ���z���S�W�j�еĸɼ����İl���О�������Ҫ���{�����á�
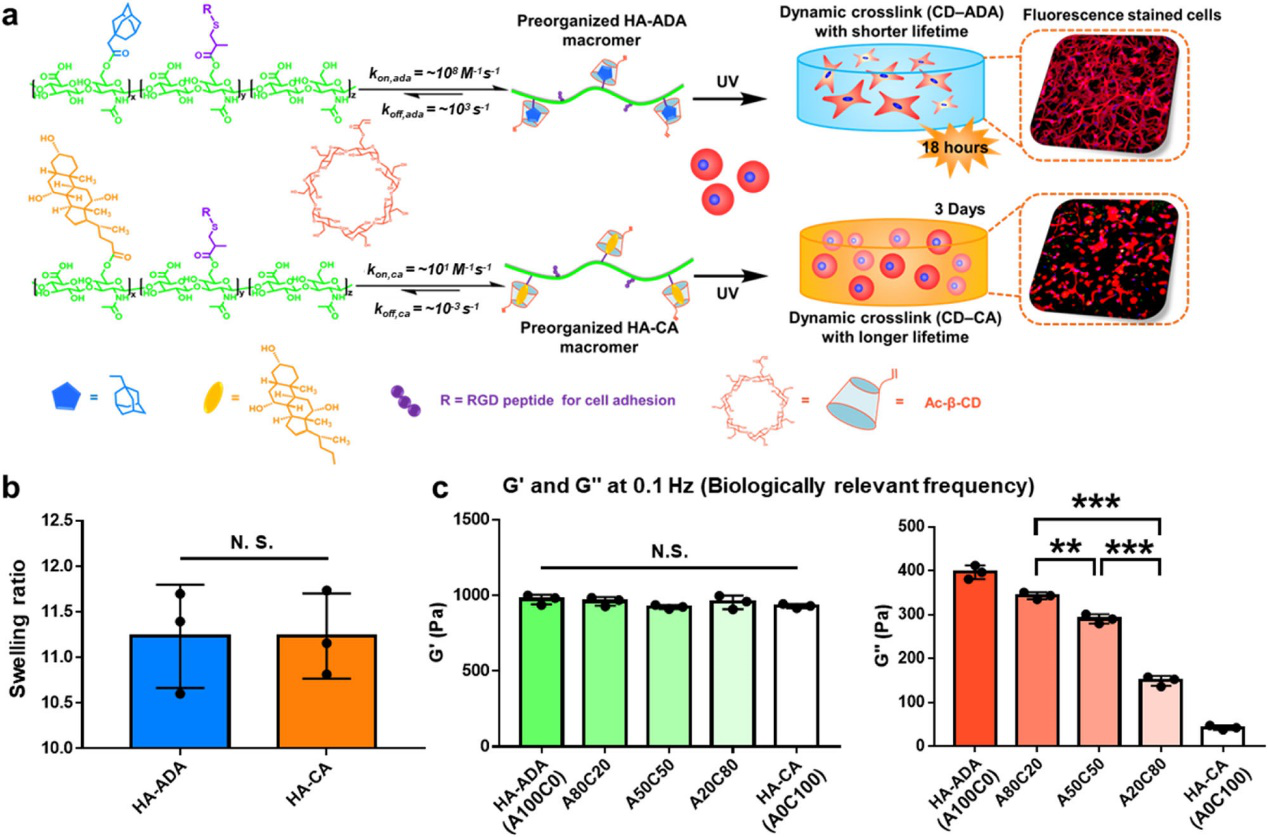
�D1. �ӑB������ˮ���z�Ę����������W���|�ͼ����չ�О顣
�Mһ���о��l�F����CD-ADA���ľ��и��߾W�j�ӑB���|��ˮ���z�����ӿ켚�����S�չ���⣬߀�@�������ɼ��������S�ӑBˮ���z�еęCе����̖�D��������˼������W�����D�����YAP�ļ������D�\��ͨ�^Ӌ��Cģ�M�����ӄ���MD�������W���ؿ����㷨KMC����ԓ�о�Ҳ�C���˄ӑBˮ���z�������W�������������W�c���S�չ��Ӱ푣��D2����
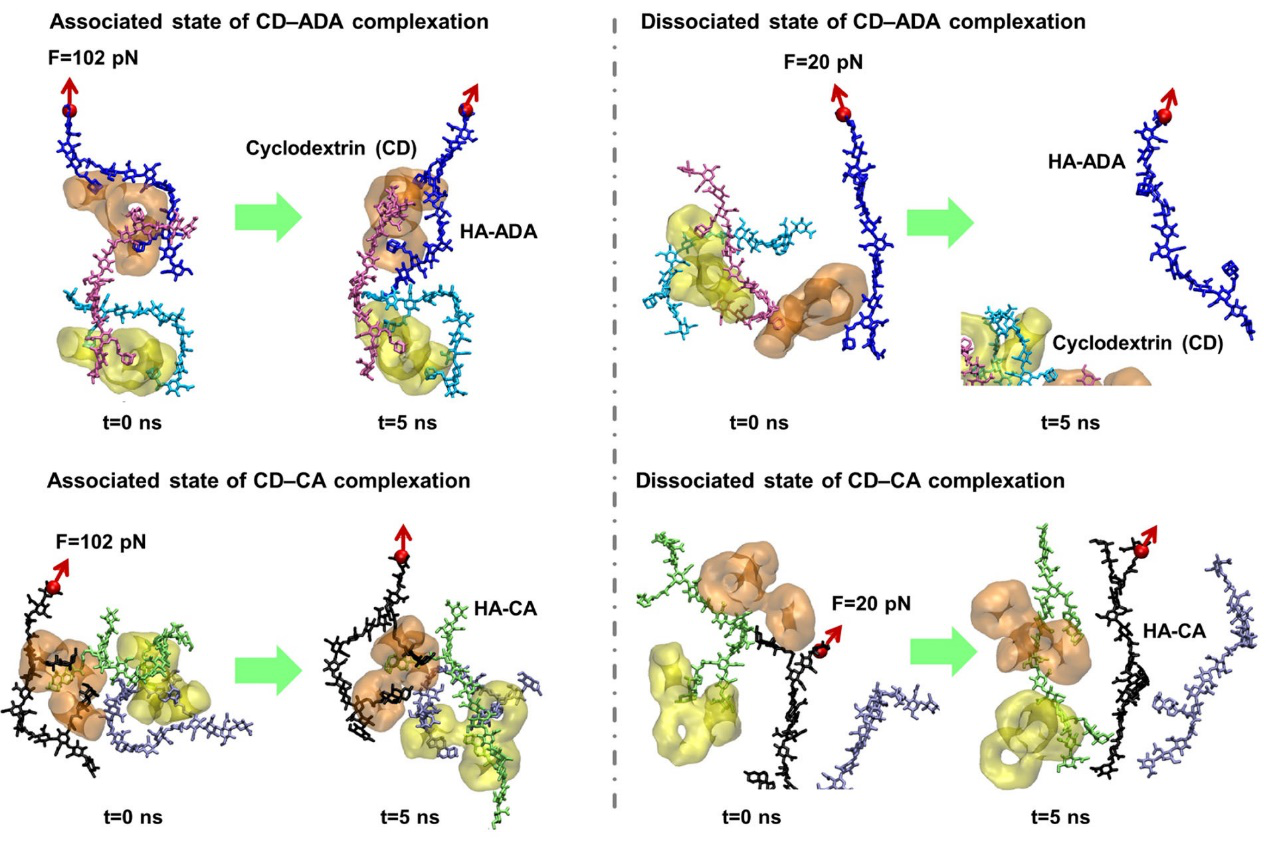
�D2. Ӌ��Cģ�Mˮ���z�еĄӑB�����ü����ڼ������W�����µĿ���j�ϡ�
���⣬ԓ�о�Ҳ�l�F���������ڄӑBˮ���z��������������W�����ĸ�֪�c������Ҳȡ�Q���������ӾW�j�Y���ļ���𤸽������ֻ�Ю�RGDͨ�^���r�I��ķ�ʽ�B����ˮ���z�W�j�Еr�����������S�չ�ŕ��@���܄ӑB�����|��Ӱ푡�����RGDͨ�^�ǹ��r�ķ�ʽ�B����ˮ���z�W�j�Еr�������t�o����֪�W�j�ĄӑB�������M�п������S�չ���D3����
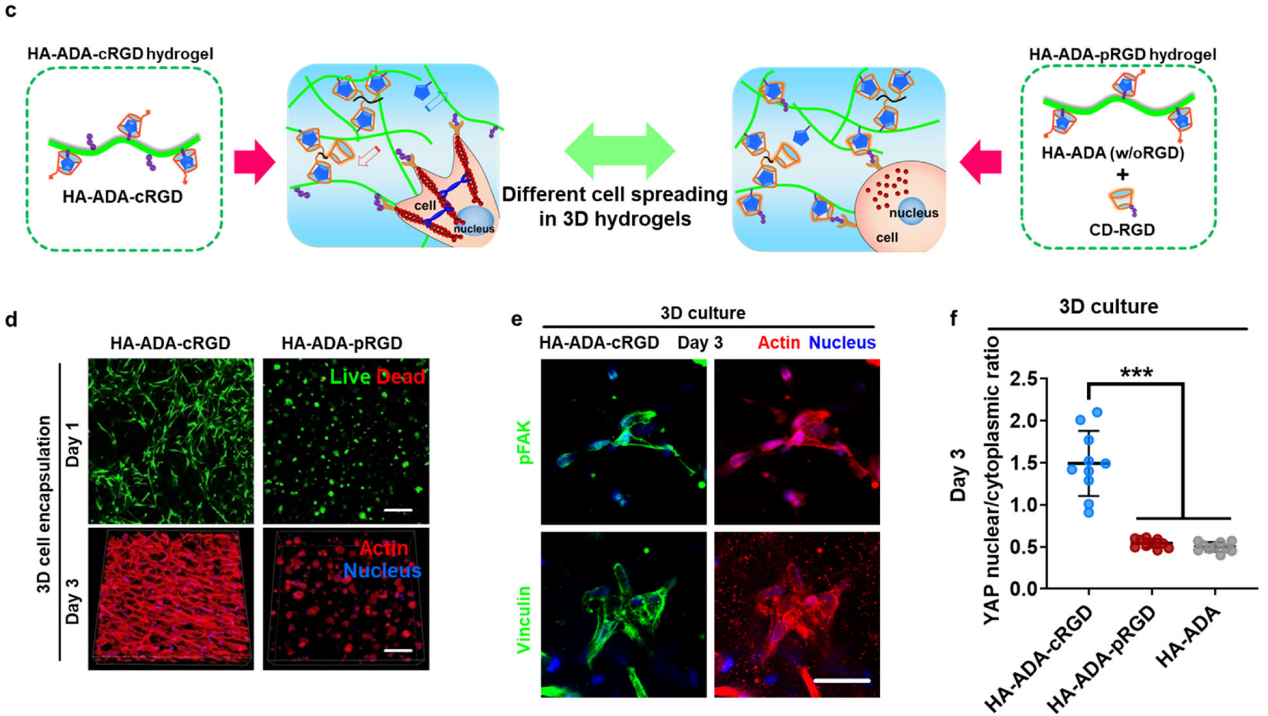
�D3. �ӑBˮ���z�W�j�ļ���𤸽����䌦�������S�չ��Ӱ푡�
�Mһ�����о��l�F���Y�Ͽ��ٿ��潻�c���rRGD��ĄӑBˮ���z�����ڸɼ����ijɹǷֻ��������@�Ĵ��M���ã���ˣ��������H�����ڸɼ����ķֻ��{���Լ����ͽM�����̲��ϵ��_�l�С��@��о��Y���ڽ����ԡ�Enhanced mechanosensing of cells in synthetic 3D matrix with controlled biophysical dynamics������}�l���ڡ�Nature Communications���ϡ�
ԓ������һ���ߞ�������Ĵ�W�����t�W����ϵ��ⲩʿ�c�F�r������ʿ����ϿƌW�c���g�о������f�ײ���ʿ��ͨӍ���ߞ�߅����������2021�����A��������W�����t�W�ƌW�c���̌WԺ���F����Ƹ���ڣ��c������Ĵ�W����ϵ��һ������
����朽ӣ�https://www.nature.com/articles/s41467-021-23120-0
߅���������L�������ڰlչ���M�{�ײ����cˮ���z�����������t�W�I��đ��ã�������u�����ˏĻ��A���όW�������t�W�о����t�������о��Ķ�������о���߅�����n�}�M�����ڸ�ˮƽ�W�g�ڿ��l����ƪՓ�ġ�
1.+Wong, S.H.D.; +Xu, X.; Chen, X., Xing, Y.; Xu, L.; Lai, N.C.H.; Oh, J.; Wong, R.W.K.; Wang, X.; Han, S.; You, W., Shuai, X.; Wong, N., *Tan, Y.; *Duan, L.; *Bian, L. Manipulation of the nanoscale presentation of integrin ligand produces cancer cells with enhanced stemness and tumorigenicity. Nano Letters, 2021.
2.+Zhao, P.; +Yang, B.; Xu, X.; Lai, N.C.H.; Li, R.; Yang, X.; *Bian, L. Nanoparticle-assembled vacuolated coacervates control macromolecule spatiotemporal distribution to provide a stable segregated cell microenvironment. Advanced Materials, 2021, 33, 9, 2007209
3.+Yuan, W.; +Wang, H.; +Fang, C.; Yang, Y.; Xia, X.; Yang, B.; *Lin, Y.; *Li, G.; *Bian, L. Microscopic local stiffening in supramolecular hydrogel network expedites stem cell mechanosensing in 3D and bone regeneration. Materials Horizons, 2021.
4.Bioadhesive hydrogels demonstrating pH-independent and ultrafast gelation promote gastric ulcer healing in pigs. Science Translational Medicine, 2020, 12, 558, eaba8014.
5.Immunoregulation of macrophages by dynamic ligand presentation via ligand-cation coordination. Nature Communications, 2019, volume 10, Article number: 1696.
6.Conformational manipulation of scale-up prepared single chain polymeric nanogels for multiscale regulation of cells. Nature Communications, 2019, volume 10, Article number: 2075.
7.Synthetic presentation of noncanonical Wnt5a motif promotes mechanosensing-dependent differentiation of stem cells and regeneration. Science Advances, 2019, 5: eaaw3896.
8.Dynamic and cell-infiltratable hydrogels as injectable carrier of therapeutic cells and drugs for treating challenging bone defects. ACS Central Science, 2019, 5 (3), pp 440�C50.
9.Remote control of heterodimeric magnetic nanoswitch regulates the adhesion and differentiation of stem cells. J. Am. Chem. Soc., 2018, 140 (18), 5909-5913.
10.In situ reversible heterodimeric nanoswitch controlled by metal ion-ligand coordination regulates the adhesion, release, and differentiation of stem cells. Advanced Materials, 2018, 30(44), adma.201803591.
���d��Enhanced mechanosensing of cells in synthetic 3D matrix with controlled biophysical dynamics
- ������κ�/������ Small �C��: ���W���ܿ��{�ӑBˮ���z����3D��������B 2025-06-27
- �A��������W߅�������ڈFꠡ�Biomaterials��: �����w�ӑBˮ���z���M��̥�ɼ������L�����S���B�е���ֳ���Ա��� 2022-09-22
- �A��������W߅�������ڈFꠡ�Chem. Rev.���C�����Y���ӑBˮ���z���������t�W���� �C ����^�������c�^�ӑB��֮�g������ƽ�� 2021-07-06
- ꃿƴ����W������/�h������ Small��ä��ճҺ���l�ĸ��������ޏͳ�����ˮ���z���ڶ���Թ�늿ɴ����O�� 2025-01-20
- �пƴ����J���� Adv. Mater.������CB[8]-����������w���W������푑�������ˮ���z 2024-08-28
- �ֻ������Q�о��T�����ꐳ������� Nat. Commun.���{���w�S�ؽ錧�Ķ��ӑB�fͬ���Ø�������ճ��-���x��ˮ���z���Ƥ�w 2024-05-10
- ��۳Ǵ����ɏ���ڈF� AFM����ƫ������ϩ�o늼��z�{���w�S���ɼ����ɹǷֻ����{�� 2023-11-01
