�����[���LJ�(y��n)�����{��������ش���Ŀǰ�����y(t��ng)�����g(sh��)�� �ů��ͻ����⣬߀������һϵ���[���ί��·���/�����������ί��������ί��������ί�(��ᡢ�⡢�š�늡���)�̈́����W(xu��)�ί��ȡ����������[���ɼ�(x��)���Լ���(f��)�s���[���h(hu��n)��Ӱ푣��������ί����y�͏�(f��)�l(f��)�ȳɞ��[���ί����y�Կ˷����ϵK���������ͬ�ί������Y(ji��)����һ���f(xi��)ͬ�ί��[����ȡ�ø��õľC�ϯ�Ч�����ɷN���N��ͬ�������pģ�Ͷ�ģ�B(t��i)���f(xi��)ͬ�ί��[�������H��Ч�ߣ�20���������ʳ��^90%������������С������ʹ��ˎ���͡�������չ�ԏ�(qi��ng)���о��Y(ji��)�������[���f(xi��)ͬ�ί�Ч�����@��(y��u)�چηN�ί�������������?y��n)��[����(f��)�l(f��)���������ί����y��Ŀǰ�����Ѕf(xi��)ͬ�ί������܉��_(d��)���R���ί���Ҫ����ӽ��R���[����(f��)�l(f��)���������ί��ĬF(xi��n)������о��ˆT���[��������Ƥ���L��300 mm3�����γɴ��[��ģ�ͣ����w�e�����L��ʢ���ί��y�ȸ����[��ģ���L�r(sh��)�g��40-80�죩�^�����(f��)�l(f��)��r���鯟Ч���u�И�(bi��o)��(zh��n)�ܸ��õ��u�r(ji��)�[���f(xi��)ͬ�ί�Ч����
�����������Thermodynamic therapy��TDT���ǽ�������l(f��)չ������һ�N���̈́����W(xu��)�ί������������c(di��n)�����ßἤ��������a(ch��n)���������ɻ������[��������ه���[���ĭh(hu��n)����Ŀǰ��Ҫʹ�õğ��������2,2''-ż���p[2-(2-������-2-��)����]���}���}��2,2��-azobis[2-(2-imidazolin-2-yl)propane]dihydrochloride��AIPH����ԓ��������(w��n)��(40-50��)�ֽ�ų����ɻ���һ����Ҫؓ(f��)�d���d�w���M(j��n)���w��(n��i)���ӟ᷽���й⣬�żӟ�ȡ�����ğ�����ؗl����(y��ng)ԓʹ�ί���λ����40-65���^�L�ĕr(sh��)�g(����10���)���^������AIPH�ֽ⡣����@Щ�ӟ᷽���c���������ƥ���Բ��ã�߀�]�Ќ��T���ڟ�����ί��ļӟ�ϵ�y(t��ng)������ᘌ��[����/�������Ҫ���ڶ����������Y(ji��)����ָ��(d��o)�£������{�ӹ����g(sh��)�缤����g�ȣ��аl(f��)��һϵ�П�����ί����T��늟�ᘣ���(j��ng)�^��(y��u)���O(sh��)Ӌ(j��)��һ�N�λ�·늼ӟ�ᘣ����ü��⼼�g(sh��)���п���w�ڴ����(d��o)�������γɻ�·���D1 �ϣ���ԓ늟�ᘿ���0.2-2 V�ĵ�늉���(sh��)�F(xi��n)�����w��(n��i)1��犿��������Ұl(f��)��λ�ÿ��{(di��o)�����܌�(sh��)�F(xi��n)���L���_�l(f��)��أ��e�m�����[������ᯟ/������ί������(sh��)�(y��n)����60 s��(n��i)С���[����λ�ضȏ�34.7 ��������53.8 �棬�ӟ�20 s�[���ضȾ��_(d��)��50 �棬�ӟ�2 min�ض��_(d��)����(w��n)�B(t��i)���[�����ضȼs65 �棬����2 V��늉����[���ֲ�40~65�淶���S���ض��ض�T��7�� 20������ϣ��D1 �£����Ї�����ZL202010490961.0����
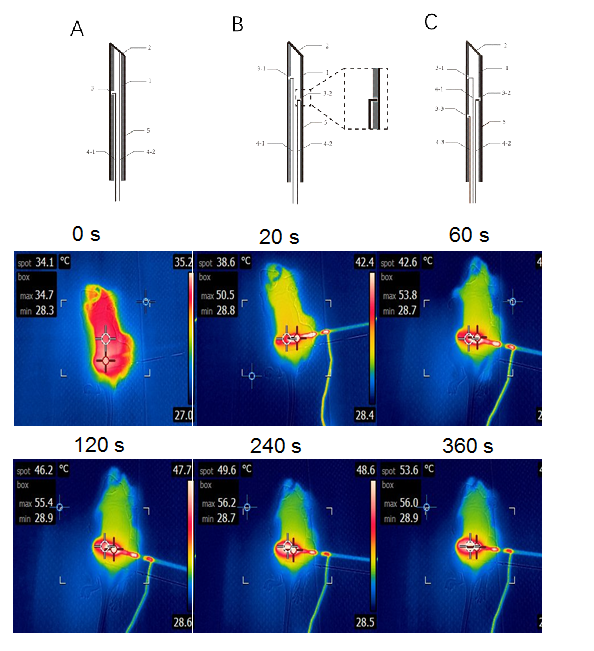
�D1.늟�ᘵĽY(ji��)��(g��u)�c���|(zh��)
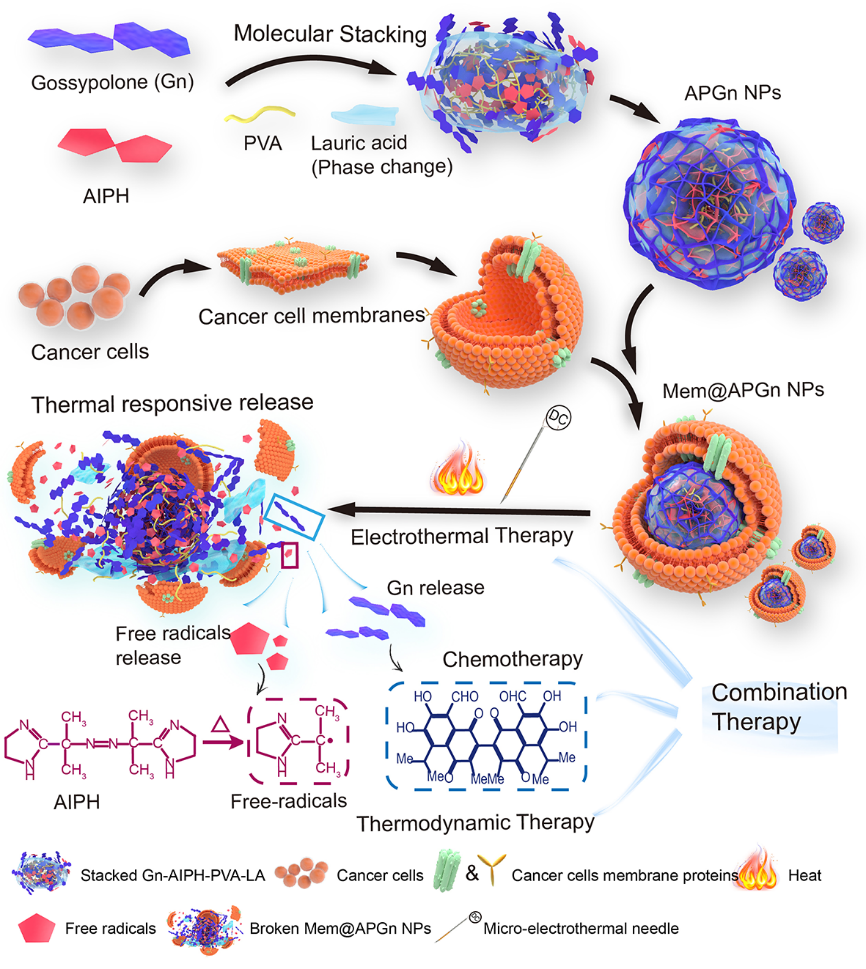
�D2.���[��늟�/�����/������ģ�B(t��i)�f(xi��)ͬ�ί�
APGn@MemNPs�M(j��n)���w��(n��i)������ͬԴ�[����(x��)��Ĥ�����[����λ����늟�ᘼӟ��ᯟ��ͬ�r(sh��)���¹���Ѹ����׃ጷ�AIPH���a(ch��n)���������ɻ������[������Gn��ጷ��������������L�ڻ������@�N������늟�/�����W(xu��)�ί��c�L�ڻ�����Y(ji��)�ϵIJ��Կ�������ȵذl(f��)�]��ͬ�ί������į�Ч�����ڴ��[��(30mm3���C���ί�Ч���@����

��D3A��ʾPBS�M���[���@�����L��16���ƽ���w�e���^1200 mm3����Mem@APGn��һ������NPs���[�����L���p���������á�Gn��AIPH�ģ�5 mg kg?1���ί��M�[�������L�H�ڽoˎ������(n��i)�ܵ����ơ����ڽoˎ���������p���[�����M(j��n)չ���@�c�R����(j��ng)�(y��n)�ĽY(ji��)��һ�¡��چΪ�(d��)��ETT��H���M���^�쵽���_���[�����L���ơ�H1��100 mm3ģ�ͣ����[�����������cH3����300 mm3ģ�ͣ����ƣ��[��������TIR�ӽ�90%������Mem@APGn�ضȿ��ƽMNPs(Mem@APGnNPs+H����̎��100��300 mm3�[�������@ʾ��ͬ�ȵį�Ч����16���[��������TIR�քe��96.97%��99.89%���D3B�����D3C�@ʾ��H1����H3�е�һЩ�[����(f��)�l(f��)��r��Mem@APGnNPs+H3�M60���[����(f��)�l(f��)�ʃH20%�������Y(ji��)���@ʾ��ԓ������(y��u)���Ĵ��[���ί�Ч������δ�����[���ί��о��ЏV韑�(y��ng)��ǰ����
ԓ�о��ɹ���ǰ�� ��Molecular Stacking Composite Nanoparticles of Gossypolone and Thermodynamic Agent for Elimination of Large Tumor in Mice via Electrothermal-Thermodynamic-Chemo Trimodal Combination Therapy�����}�ڇ��H�����W(xu��)�g(sh��)�ڿ���Advanced Functional Materials�� (IF=18.8)���ھ��l(f��)������һ���ߞ�������ͨ��W(xu��)�����W(xu��)Ժ��ʿ�����������ǵ��ν��ڞ�ΨһͨӍ���ߣ�������ͨ��W(xu��)�����t(y��)�W(xu��)��Ϣ���̽��������c(di��n)��(sh��)�(y��n)�Һ������W(xu��)Ժ��ԓՓ�ĵĵ�һ��ΨһͨӍ���߆�λ��ԓ�о��ɹ��Džǵ��ν����n�}�M�ڟo����λ�ۺ���(li��n)�ϻ����ί��[����Int J Nanomedicine 2017,12; 4085�C4109���B�m(x��)3�� ESI�߱���Փ�ģ����[����ữ����Biomaterials 2018, 154;197-212�����/�o����λ�ۺ����pˎ�f(xi��)ͬ�[���ί���Advanced. Functional. Materials 2021,31(24); 2100954��֮�����һ��Ҫ�ɹ���
ԓ�����õ��ˇ�����Ȼ�ƌW(xu��)����͇����ش�ƌW(xu��)�x���O(sh��)���(xi��ng)Ŀ���Y����������ͨ��W(xu��)�����yԇ���Ğ鱾�����ṩ�˴����yԇ����֧�֡�
Փ��朽ӣ�https://doi.org/10.1002/adfm.202201666
- ���ϴ�W(xu��)��ӡ���� Angew���ξ��w����(n��i)���^�Y(ji��)��(g��u)�Ŀ��g�{(di��o)�� 2025-05-05
- �|�A��W(xu��)�����ΈF(tu��n)�(du��) Macromolecules��ܛ�{���������w��׃��ʾ���p�Y(ji��)��ԭ���͘O�� 2025-04-17
- �㽭��W(xu��)����F(tu��n)�(du��)��Adv. Sci.��������ʽ�{�������T��(d��o)��(x��)���~�������ڸ�Ⱦ�Է����ί� 2025-02-27
- �V�������n�}�M Adv. Mater.: ���ھ���ϩ���sȩ��׃Һ�w��ȫ����(ji��)�nj��Q����׃ɫ�� 2025-06-03
- �A��������W(xu��)�����A���ڈF(tu��n)�(du��) AFM���ɶ��ӽM�b�ݿY(ji��)��(g��u)�ľ���ϩ��/̼��(f��)�Ϛ����z��(sh��)�F(xi��n)���������p���պ�ˮ���Π�ӛ��Ч��(y��ng) 2025-05-14
- �ϴ�����x/��犡������_�G�� Adv. Mater.������ģ������ϩ��ˮ���z늽��|(zh��)��(sh��)�F(xi��n)�o֦���\�x��늳� 2024-11-16
- ���д����ڣ��w�� / �Ʊ��҈F(tu��n)�(du��) ACS Nano �����AIE�{���R�_(d��)ͻ���[������ - ��(sh��)�F(xi��n)����(zh��n)���\�� 2025-05-29
�\���P(gu��n)ע�߷��ӿƼ�

- ����(b��o)���C(j��)����500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ��h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c(di��n)������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��
- �Ј���300�|��PMEC China ɫ...
- ����ע�ԣ�2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ(x��n)����...
- �����ϸ��Լ��ӹ����g(sh��)Ҫ�I(l��ng)��...
- �Ϸ��Ƽ���W(xu��)�����w���ڈF(tu��n)�(du��)...
- ���ϴ�W(xu��)������/����Ⱥ/����...
- ̫ԭ������W(xu��)�~���/��ʯ��...
- ���_������W(xu��)/�����ش�W(xu��) CR...
- ��h��W(xu��)ꐳ������߶���/��...
- ��ƴ��R��l(f��)�݈F(tu��n)�(du��) AFM��...
- ����W(xu��)�~������ Macromole...
- ����������n�}�M��Macromol...
- ����݆֪ͨ | ����ø߷���...
- �Ͼ���W(xu��)����x/��� Angew....
- �K�������һԺ������...