���_��W���������n�}�M��Adv. Mater.����ˮ��Һ�зǹ��r�ۺϼ���ij������t���Ҝ��������D(zhu��n)�ƽM�b
������������˹��ϳɴ�h(hu��n)���w�ij����ӹⲶ�@�wϵ�ܵ��ˏV�����P(gu��n)ע�������������W̽ᘡ��l(f��)����ϡ��⻯�W�����I(l��ng)���@ʾ���˪���(chu��ng)�Եđ�(y��ng)�á�Ȼ���������(sh��)�ш�����˹��Ⲷ�@ϵ�y(t��ng)���ܵ����w��ɫ�F���ɱ���Ķ̟ɹ���������ƣ���ˣ����ҿ�����ľ����L�����l(f��)��Ĺ��w�팍�F(xi��n)�������f�^���Ƿdz���Ҫ�ġ���ˣ����г��L�l(f��)������ͳ���˹�п�˹λ�Ƶ��ЙC�Ҝ��⣨RTP����ҕ���Q�������}����Ч���������ڴˣ�RTP�����D(zhu��n)���wϵ�Ę�(g��u)����u�ɞ�һ���µ��о����c��������ͨ�^���t�������^�́����L��Ʒ���ɹ�Ⱦ�����w�ĉ��������������ӛ����Ϣ��ȫ�ʹ̼�푑�(y��ng)���ϵȷ����@ʾ����Ҫ�đ�(y��ng)��ǰ����Ȼ����Ŀǰ��ֹ��ˮ��Һ�м���L�������t�⣨NIR���l(f��)�����ܺͰ�����������������ij������Ⲷ�@ϵ�y(t��ng)�Ę�(g��u)����Ȼ����Ҋ��
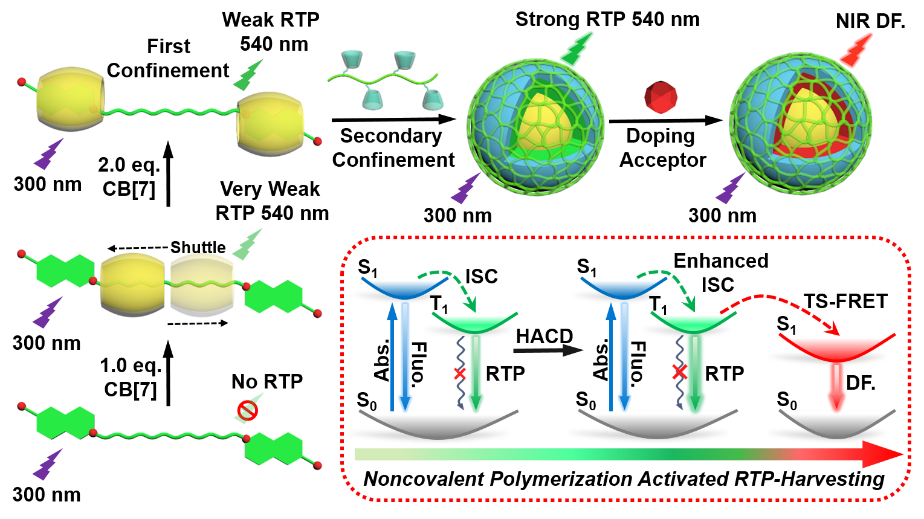
�D1. ˮ��Һ�о��н��t��l(f��)��ij����Ӽ��ЙC�Ҝ��Ⲷ�@ϵ�y(t��ng)�Ę�(g��u)��ʾ��D
���գ����������n�}�M���ں��J[7]�壨CB[7]������-�h(hu��n)������֦���|(zh��)�ᣨHACD����������h(hu��n)����ͽM�b�����ɹ���(g��u)����һ�N�ǹ��r�ۺϼ��������t��l(f��)��RTP���@ϵ�y(t��ng)���cʮ�����朘�(li��n)��6-�宐��������G����ȣ����ڴ�h(hu��n)���w�T�����w�������Ч��(y��ng)������νM�bG?CB[7]��540 nm̎���F(xi��n)��һ�������w�j(lu��)���T����RTP��̖���S����������-�h(hu��n)����ǻ���Mһ��������b��ͨ�^HACD��G?CB[7]�ķǹ��r�ۺ�����ʹ��ԭ����������59.0 ��s���ӵ�0.581 ms�������Mһ��������RTP�l(f��)�䏊���s8������Ҫ����������G?CB[7]@HACD�M�b�w�����������ɷN��͵��ЙCȾ�ϣ����_�{���ģ�4-����������߲�����������w���ڸߵĹ�/���w�����¿��Ԍ��F(xi��n)��Ч��RTP�����D(zhu��n)�Ʋ����S���L�����Ľ��t�����t�l(f��)�����ܣ�680 , 710 nm������Ȥ���ǣ�ͨ�^�������|(zh��)��İ������������Ƃ��RTP���@ϵ�y(t��ng)�ɹ��ؑ�(y��ng)���ڻ��w�[�������İ���NIR�����@���H�鄓(chu��ng)������M��ˮ����NIR������ṩ��һ�N���ķ����������ڹ�������W���С�������ί��ȷ�����Н��ڵđ�(y��ng)�Ãrֵ�����P(gu��n)�ɹ��Ԙ��}�顰Noncovalent Polymerization Activated Ultrastrong Near-Infrared Room-Temperature Phosphorescence Energy Transfer Assembly in Aqueous Solution���l(f��)������Advanced Materials������DOI: 10.1002/adma.202203534�������_��W���W�WԺ��ʿ�о������F(xi��n)�y��Փ�ĵ�һ���ߣ����_��W���W�WԺ���������鱾��ͨӍ���ߣ�Փ������: Xian-Yin Dai, Man Huo, Xiaoyun Dong, Yu-Yang Hu, and Yu Liu����

�D2. ˮ��Һ���������T�����������ЙC�Ҝ��⣺��a�����wG�м�����J[7]�������t�l(f��)����V׃������b��G?CB[7]�������˥�p�����Լ�ͨN2ǰ�������t�l(f��)����V׃������c��G?CB[7]�м���HACD������t�l(f��)����V׃������d��G?CB[7]@HACD�M�b�w�������˥�p��������e���M�b�^���й�W�^��׃���Լ����_���F(xi��n)��f��G?CB[7]@HACD�M�b�w�ĄӑB(t��i)��ɢ������Լ�����R�D��

�D3. �ǹ��r�ۺϼ���Ľ��t���Ҝ��������D(zhu��n)�ƣ���a���wһ����G?CB[7]@HACD�M�b�w�����t�l(f��)����V��NiB�����չ��V���l(f��)����V����b��G?CB[7]@HACD�M�b�w�м���NiBǰ������t�l(f��)����V����c���wһ����G?CB[7]@HACD�M�b�w����u����NiB������t�l(f��)����V׃������d�����ܺ�540 nm��680 nm���L̎�l(f��)���������˥�p������

�D4. �[������������t������a���˷ΰ���������b���ˌm�i����������c������λ���Ⱦɫ�Y(ji��)������d������̥�I��������
ԓ���������������n�}�M�����P(gu��n)����h(hu��n)���w�����ЙC�Ҝ������䑪(y��ng)�÷���������Mչ֮һ�����^ȥ�������У����������n�}�M��ԓ����ȡ����һϵ���о��ɹ������������S��׃���ZԽ�����ؾ��p�L�l(f��)�⡱��Angew. Chem. Int. Ed. 2019, 58, 6028�C6032; Chem. Sci. 2019, 10, 7773�C7778�������f(xi��)ͬ���ԃ���������Angew. Chem. Int. Ed. 2020, 59, 18748�C18754; Angew. Chem. Int. Ed. 2022, 61, e2021152������ˮ�������������Nat. Commun. 2020, 11, 4655; Chem. Sci. 2020, 12, 1851�C1857; ACS Appl. Mater. Interfaces 2022, 14, 4417?4422; J. Med. Chem. 2022, 65, 7363?7370; Chin. Chem. Lett. 2022, 33, 851�C854�����������ۯBȫ�ZԽ����Adv. Mater. 2021, 33, 2007476; Adv. Sci. 2022, 9, 2201182�������p����������λ����J. Am. Chem. Soc. 2021, 143, 13887�C13894; Adv. Sci. 2022, 2201962��������(li��n)��Ⲷ�@����Angew. Chem. Int. Ed. 2021, 60, 27171�C27177; Small 2022, 18, 2104514; Adv. Sci. 2022, 2201523; Chem. Sci. 2022, 13, 573�C579���������������_�P(gu��n)����Adv. Sci. 2022, 9, 2200524; Adv. Sci. 2022, 9, 2103041; Small 2022, 18, 2201821; Adv. Optical Mater. 2022, 10, 2102169�����������l(f��)���C����Acc. Chem. Res. 2021, 54, 3403�C3414; Chem. Rev. 2022, 122, 9032�C9077; Chem. Soc. Rev. 2022, 51, 4786�C4827; Chem. Sci. 2022, 10.1039/D2SC01770A���ȣ����h(hu��n)�����ЙC�Ҝ�����������������Ϣ���ܡ����β��ϵ�����đ�(y��ng)���ṩ����˼·��
ԭ��朽ӣ�https://doi.org/10.1002/adma.202203534




