�Ĵ���W�O��/���彭��Mater. Horiz.��������-����ԽM�bͿ����������ˮ���z���F�����fͬ�ί��Ă�������
�����о��l�F��������Ե��������܉���m�Է��ڶ�N�������|���{�ز����Ƃ����܇��h����ֱ���������ϡ�Ȼ�������ί��^���п�����ˎ����ձ�ʹ���������������������@���Ě�������������ί�Ч�������H��ˣ����ڱ����Ŀ�ԭ���|��������ֱ���c���ڽ��|Ҳ������һϵ���װY��������ˣ�����ڱ������������Ե���r����Ч���������ɔ_�t�ǽ�Q���}���P�I��
���ڣ��Ĵ���W�����t�W���̌WԺ/���������t�W���Ϲ��̼��g�о����ď��d��Ժʿ�FꠌO���о��T/���彭�����܆Ό�����F�x���������õĆ��l���������������_�l��һ�N����-����ԽM�b�{��Ϳ�ӣ����Y��ǰ���w�Sˮ���z�Ĺ������A��Compos Part B-Eng 2023, 250, 110451�����������������b�d�����Ȼ��������w�S���������|���γɵĿ�ע���w�Sˮ���z�У��D1�����@�N����-���Ϳ���܉���Ч���ζ�N��Ҋ�����،����w�ĸɔ_��ͬ�r���ܾS�־��w������������Ӻ;��w��ֳ����֧������m�����ط��ڹ��ܻ����ЙC��������ᣩ���w�Sˮ���z�W�jҲ���������ṩ��һ��֧�ֱ��o�Ŀ��g��������ֱ���c���ڽ��|�����װY����С��ȫƤ�ӂ���ģ���У��@�N����-����ԽM�b������ˮ���z��Gel/L@FeTA���c����������ˮ���z��Gel/L����ȣ��ڰ��S�c��ù���ί��ėl���£��܉��@�����M�����{����Ѫ�������Լ��M������һϵ�������^�̣��M�����ق������ϡ��@�N�ԽM�bͿ��+ˮ���z�p�ӱ��o�wϵ��������������������������ڽM���ޏ��е��ί��ṩ��һ�����ο��еIJ��ԡ�ԓ��������Metal-phenolic self-assembly shielded probiotics in hydrogel reinforced wound healing with antibiotic treatment�����}�l���ڡ�Materials Horizons�������µ�һ�������Ĵ���W��ʿ������ʹTʿ���u��Ƽ���о������õ�ʮ�������c�аl��헺͇�����Ȼ�ƌW�����֧�֡�

�D1. ����-����ԽM�b������ˮ���z���Ƃ�
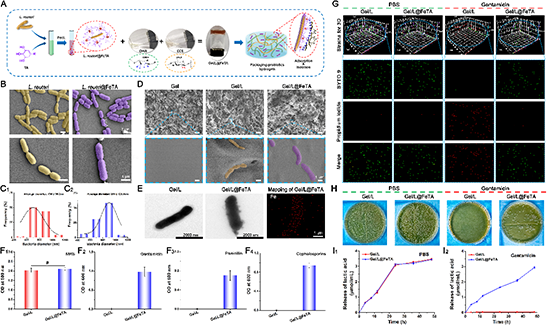
�D2.����-����ԽM�b������ˮ���z���Ͽ������ί��r�܉���Ч���־��w�Ļ����c����
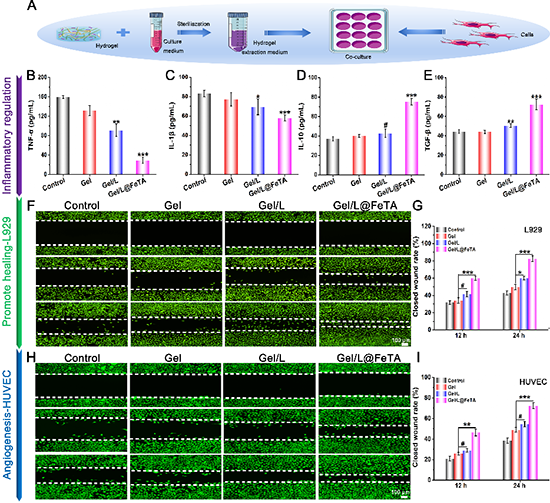
�D3.����-����ԽM�b������ˮ���z��Ч�M�������{�ز����M���w�S�����Լ�Ѫ�܃�Ƥ��������ֳ�c�w��

�D4.����-����ԽM�b������ˮ���z���Ͽ������ί��r���F�����õĴق�����������
ԓ�����LjF����w�S�������z֧�������M�������е����Mչ֮һ�����ڽM���γɳ��ڿ������w�S�����Y�B���|�����ɼ����l���h���@һ���c���F꠰lչ��ϵ�������c��/�����Խ��w�S�������z֧�ܣ�������Ƥ�w��ܛ�ǺǽM���������^ȥһ���У��F�ͨ�^Ӌ��C�����OӋ���_�l�ԽM�b�����Ӷ������z�����zԭԭ�w�S�����M��ܛ�Ǽ�������ֳ���S������ܛ�DZ��ͣ�Bioact. Mater. 2022, 8:396����ͨ�^���ܻ����|���������ӽ�������Ч�����zԭ�w�S�c�u����ʯ���lչ�˿�ճ�����Թ��ޏ�֧�ܣ���������B���R��ȱ�p��ԭλ�ޏ�Ч�ʣ�Nat. Commun., 2022, 13:2499; Adv. Funct. Mater., 2023, 33: 2212738-����Փ�ģ�������3D��ӡ���g������Y�������w�S�����L�����W���d��ͨ�^�c�w�S�������z�ĸ�Ч���ϣ��lչ���g�Ķ��ؿ�϶�������ޏ��w��Adv. Sci., 2023, 10: 2300038; Small, 2023, 19: 2206960; ACS Appl. Mater. Inter., 2022, 14: 20591/2022, 14: 32914�����@һ����Ҳ�������LЧ����dˎ�{���z�����������w�S�������z���|�����ጷŵİ����ͼ{��������������Ƥ�w���Բ�׃���g��Ͱl�������M�䲡׃�^��ë�l�֏ͣ�J. Control. Release, 2023, 356: 219����Ҳ���������Թ��f�ͼ{���u����ʯ��PD-L1���Ƅ�������Ƥ�w���Բ�׃�����߯�Ч��ACS Nano, 2022, 16: 18921����
ԭ��朽ӣ�
https://pubs.rsc.org/en/content/articlelanding/2023/mh/d3mh00033h




