��(j��)����һ�ڡ���Ȼ·ͨ�š��s־��(b��o)��������(gu��)Ү����W(xu��)�о��ˆT���ü{�������аl(f��)��ˎ��ݔ��ϵ�y(t��ng)����ʹ���w�M����(du��)���w����ϵ�y(t��ng)���[�����F(xi��n)�����Ķ��p����������ֲ�IJ��l(f��)�Y��
�����(l��i)���M��������ֲ�I(l��ng)��ȡ���˺ܴ��M(j��n)���������ں��L(zh��ng)�������Ů�����(y��ng)��Ȼ�����L(f��ng)�U(xi��n)��T��(x��)�����R(sh��)�e��������İ�Ѫ��(x��)����Ҳ�������Ů�����(y��ng)�������ҪԪ��֮һ����������Ч��Ч��(y��ng)ӛ��T��(x��)�����ɹ��w����Ѫ�܃�(n��i)Ƥ��(x��)����������(x��)����ԭ��HLA�������
�о��ˆT�ÿ���K�л�����_(d��)��siRNA��С�ɔ_RNA����(l��i)�@��(g��)�����oĬ�����ó�Ҏ(gu��)ݔ�ͷ�����siRNA��Ӱ푃H���m(x��)���죬�����������w��ֲ�����٣�ͨ����Ҫ��(sh��)�܁�(l��i)���������ͽ����Ů�����(y��ng)�L(f��ng)�U(xi��n)�����⣬siRNA߀��(hu��)�o������Ҫ�ί����������ٵ�Ѫ�܃�(n��i)Ƥ��(x��)������(l��i)�����á�
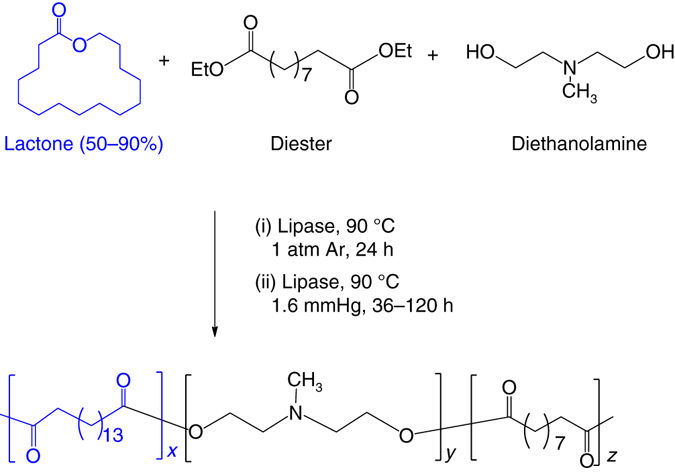
�������m(x��)siRNA�����ã�Ү����W(xu��)�о��ˆT�_�l(f��)��һ�N�µ�ˎ��ݔ��ϵ�y(t��ng)�����л��ھۺ���ļ{�����ӣ��ɔy��siRNA���_(d��)��ֲ��λ������ጷ�ˎ�����߀�_�l(f��)���ڹ��w���ٱ���ֲ֮ǰ���{�������������еķ������@��ˎ��ֻᘌ�(du��)��ֲ���ٶ�����ȫ����
�@Щ�{�����ӿ�ᘌ�(du��)�ض������M(j��n)���{(di��o)�����䎧�е�����늺�ͬsiRNA����ؓ(f��)늺�����ã�ʹ�{�����ӳɞ�ˎ�����Ȼ�d�w��ͻ����Ŀǰ���ü{�����ӃH�ܔy������ˎ��ĘO�ޡ�
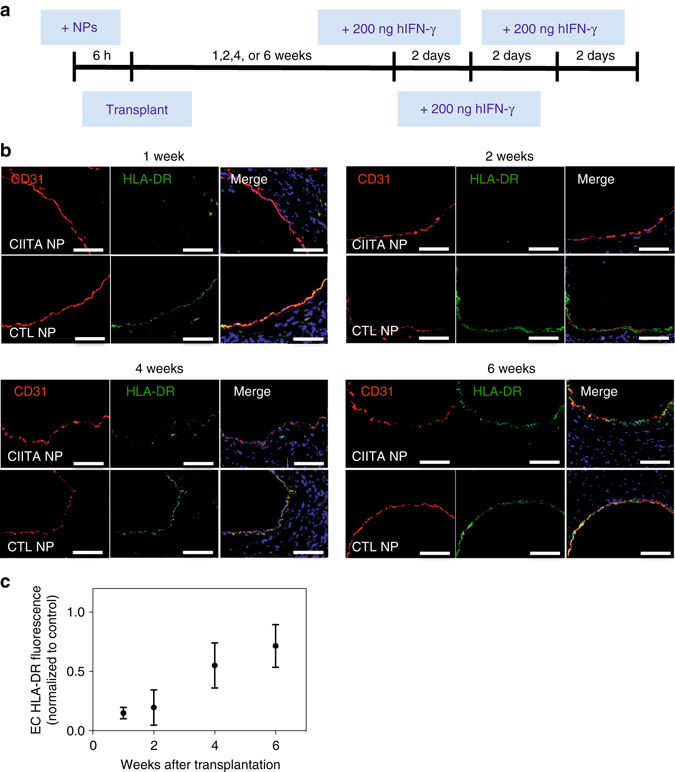
�������о��У��о��ˆT��ֱ������IJ����˄�(d��ng)�}�Ôy��siRNA�ļ{�������M(j��n)����̎����Ȼ����ֲ��ע�������T��(x��)��������ȱ��С��ĸ�������(d��ng)�}���Y(ji��)���l(f��)�F(xi��n)������ֲ���ܺ{��������Ȼ�����ڹ��w�M���������@�oĬ�˵��ױ��_(d��)�����ң������P(gu��n)���ٵ�Ѫ�܃�(n��i)Ƥ��(x��)�����o(w��)�p����
�о��ˆT��ʾ����ֲ�������������P(gu��n)��Ҫ�����t�Ů�����(y��ng)���_ʼ�r(sh��)�g����ʹ�Ů�����(y��ng)׃�ø��غ͡������ƣ������Ů�����(y��ng)Ҳ��(hu��)���١�
- �����������ڈF(tu��n)�(du��) Angew�����и�Ч�[����e�͝B���ܵİ���ø푑�(y��ng)늺ɷ��D(zhu��n)ˎ��ݔ��ϵ�y(t��ng) 2023-02-09
- �㽭��W(xu��)����/��LjF(tu��n)�(du��)��ACS AMI�����ڷ���(f��)���r����ˎ���ί����ԸΓp�� 2022-09-21
- Science�ӿ����ܶ��߆��l(f��)�������ٟo(w��)ʹ�NƬע�����ѳɹ����� 2019-08-09
- ���ϴ�W(xu��)��ӡ���� Angew��?ji��n)ξ��w����(n��i)���^�Y(ji��)��(g��u)�Ŀ��g�{(di��o)�� 2025-05-05
- �|�A��W(xu��)�����ΈF(tu��n)�(du��) Macromolecules��ܛ�{���������w��׃��ʾ���p�Y(ji��)��ԭ���͘O�� 2025-04-17
- �㽭��W(xu��)����F(tu��n)�(du��)��Adv. Sci.��������ʽ�{�������T��(d��o)��(x��)���~�������ڸ�Ⱦ�Է����ί� 2025-02-27
�\(ch��ng)���P(gu��n)ע�߷��ӿƼ�

- CPHI����չ��(sh��)�(y��n)�҃x���c�O(sh��)��...
- ���ܹ��A��朆���������22��...
- ����(b��o)���C(j��)��(hu��)��500+ˎ��...
- ��(gu��)�HƷ�ơ�ǰ�ؕ�(hu��)�h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c(di��n)������...
- ��(gu��)�a(ch��n)������٣����(gu��)���^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��(hu��)
- �Ј�(ch��ng)��300�|��PMEC China ɫ...
- ����ע��(c��)��2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �Ĵ���W(xu��)���A���ڈF(tu��n)�(du��)��Adv....
- �Ĵ���W(xu��)���������ڈF(tu��n)�(du��) Ang...
- �A��������W(xu��)���ָ���ڈF(tu��n)�(du��)...
- �칤����x/�R�w�R/���ƽ� S...
- �A���r(n��ng)�����/������...
- �Ʊ��ҽ���/�֘s�I(y��)���ڈF(tu��n)�(du��)...
- ��ӿƴ����|��/�������F(tu��n)�(du��)...
- �A������������� Angew: ...
- �Ĵ���W(xu��)������ AFM������ʯ...
- ��۳��д�W(xu��)�����n�}�M CEJ...
- �Ї�(gu��)�ƴ����d���n�}�M���邐...