���գ����Ҽ{�ƌW�����V܊�о��T���w�����о��T����һ�~���о��T�c��ʿ���nѩ���Ⱥ����������[���h�����Ӵ�푑��ͼ{��ˎ���d�w��ͨ�^���D�����Ǡ����PSC���Ļ��B�����{�����ٰ��h�����|ƽ�⡢�������ٰ�����Ч�����о���ȡ����Ҫ�Mչ�����P�о��ɹ���Reversal of pancreatic desmoplasia by re-educating stellate cells with a tumour microenvironment-activated nanosystem����2018��8��23����Nature Communications�l����2018, 9 (1): 3390����
���ٰ����Գ̶ȸߡ��A��O����Q�顰����֮���������ٰ��h�����и߶��w�S�����^�ȽY���M�����������ط�Ѫ�������ⲡ�����c���O�����K���R��һ��������������Ч��ʩ�������PSC���������zԭ���w�B�����Լ����|���ٵ���ø�ȼ�������|�������ٰ��h�����|����Ҫ��Դ����ͨ�^�c���ٰ�������ͬ�������{�ؾW�j�������ٰ��lչ���D�ơ���ˎ���������ݵȷ���l�]���M���ã������ٰ��h���{�ص���Ҫ���c��ԓ����������һ�N��������Ҷ�������x�ӽ�{���wϵ��ͬ�r�f��PSC�{��ˎ�P���ͻ��|���ڵ�siRNA���wϵ�OӋ���������[���h����pH푑��ľ��Ҷ���Ó���C�ƣ��܉��ڱ��C���w��ݔ�\�����Ե�ͬ�r����߰�������ˎ��zȡ��siRNA���DȾЧ�ʡ������ٰ����߁�Դ��PSC�У�ԓ�{���wϵ�܉���M���PSC�ط��oϢ��B���Ķ���������ڶ�N��������|�������ٰ�����/PSC���ӷN��С�����ٰ�Ƥ���[����ԭλ�[��ģ���У�ԓ�{���wϵ�����F�ˌ�PSC�������B�ĸ�Ч���D��ͨ�^���h�����|���x�ľC���{�أ��@������ˎ�����[���ȵ�ݔ�\Ч�ʣ�������ٰ��Ļ���Ч����ԓ�о����ü{��ˎ���wϵ���F�˻���PSC�oϢ�����ٰ��h�����B�{�أ�����V���Ļ��|�w�S���[�����ί��ṩ���µ�˼·��
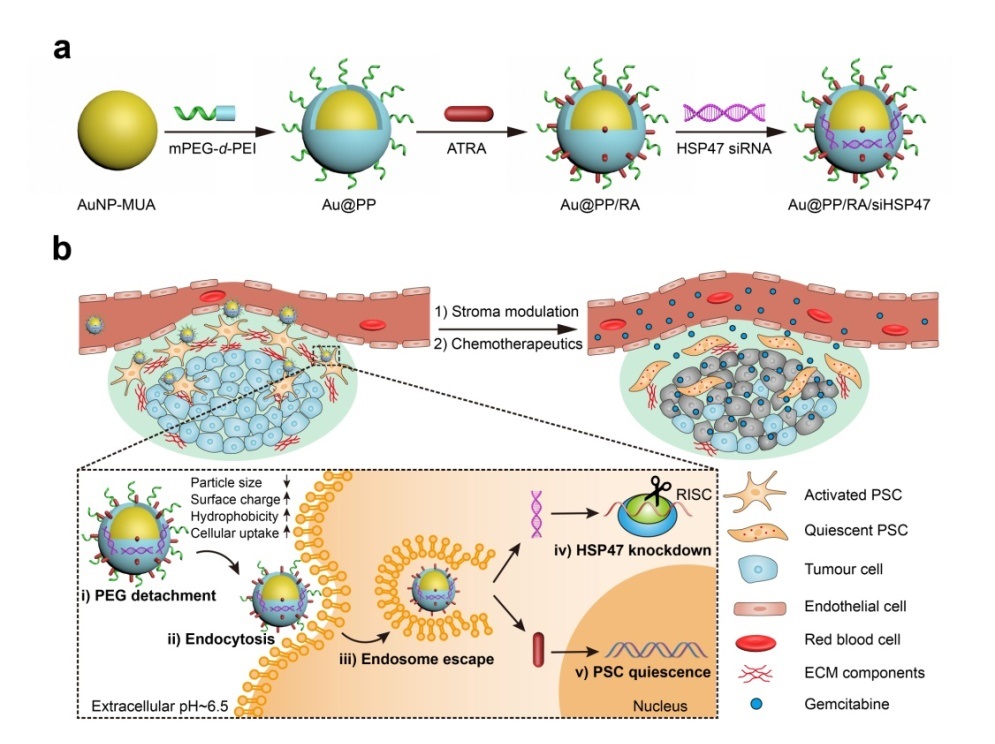
�{��ˎ����OӋ��a�������{�������Ǡ���oϢ�ęC�ƣ�b��
�w�����о��T���^ʮ����������о������������Ϳ��[�����ٸ��մ��{�ײ���Gd@C82(OH)22�������Ե�����˼{��ˎ���{���[���h�������O�������ǡ��������[�������ČW�g˼·�������H�W���u�顰�п��������[���ί���׃������P�о��ɹ�60��ƪ�l����Nature Communications��Accounts of Chemical Research��Proceedings of the National Academy of Sciences of the United States of America��Nano Letters��Advanced Materials��ACS Nano���ڿ����V܊�о��T�L�����������ü{���g������{���[���h�����о����ڻ����[�����P���w�S�������h�����|�{�ص��[���ί�����ȡ����ϵ���Mչ����ͨ�^�خ�������[�����PѪС�壬�������[��Ѫ��EPRЧ���ṩ���µļ��g��˼·�����P�����l����Nature Biomedical Engineering��Advanced Materials��Angewandte Chemie��ACS Nano��Biomaterials��Advanced Functional Materials���ڿ����ɂ��n�}�M���[���h���{���о���������L�ڷ����ĺ����Pϵ�����ڹ�ͬ�lչ�˻��ڳ������ԽM�b��DNA�{�יC�������[���h��Ѫ������ί������ṩ���µ�ˎ��ͣ�Nature Biotechnology, 2018, 36:258-264����
ԓ�о��õ��ˇ������c�аlӋ����2018YFA0208900������Ȼ�ƌW�����п�Ժǰ�ؿƌW���c�о�Ӌ���������п�ί���Ŀ��֧�֡�
- ɽ�|��W�������ڈF� ACS Nano: Ӳ�ȿ��{�ľ��Ҷ����{���w���{���{��-��������ã���������ˎ���f�� 2025-06-12
- ���������ڈF� Bioact. Mater.����ˎ���f��ϵ�y"������-����-����ϵ�y���o"��λһ�w�fͬ����ʹ�L���P�����ί� 2025-06-04
- �K���f/��Ᵽ���ڈF���Ƹ��ʿ�� - ���Ϻϳɡ��{���t�W���[���\����ˎ���f�͡������ί��ȣ� 2025-04-29
- �V�������n�}�M Adv. Mater.: ���ھ���ϩ���sȩ��׃Һ�w��ȫ�����nj��Q����׃ɫ�� 2025-06-03
- �A��������W�����A���ڈF� AFM���ɶ��ӽM�b�ݿY���ľ���ϩ��/̼�ͺϚ����z���F���������p���պ�ˮ���Π�ӛ��Ч�� 2025-05-14
- �ϴ�����x/��犡������_�G�� Adv. Mater.������ģ������ϩ��ˮ���z늽��|���F�o֦���\�x��늳� 2024-11-16
