�������������ıȱ���e��Ҏ�t�Ŀ��Y�������õķ����Ժ����������Ե����c��������Ϻͼ{���tˎ�I����Ъ��صă��ݣ����Ƃ�����ò����ͬ�r�߂��ȱ���e��Ҏ�t���Ľ�����һֱ�ԁ����˂����Pע�c���о��dȤ֮һ�����鳬���ӻ��W�I��ĺ����о�����֮һ�������Ӵ�h��������Ȥ�������w���|���ƄӴ̼�푑��Ͳ��ϵİlչ���������˘O���ؕ�I���������ͳ����Ӵ�h���OӋ�ϳ��c�_�l����һֱ�ԁ����Ƅӳ����ӻ��W�c�����о��I��lչ����Ҫ�h�����阋���¹��ܲ����ṩ���o���ܡ����ڳ����Ӵ�h�ͽ����ϵ��ЙC-�o�C�s��������ˎ���f��ϵ�y�����侫�_�ɿصĴ̼�푑����������õ������������Լ�ǰጷ�С�����c�ڼ����\����������ֲ�����L�{�����T���I��չ�F���ˏV韵đ���ǰ����
���ڣ����ִ�W���W�WԺ��Ӣ���n�}�M�����ִ�Wֲ��ƌW�WԺ�n���ѡ��ؽ����n�}�M�������¿��_˹�r����W���ڽ��ڣ����ִ�W�����t�W�WԺ���B���n�}�M�ψ����һ�N�����ɾۼ��T���l����Ӻ�б�����N�������_�P�p���ܻ��ij����ӽ��{���㶹ˎ���f��ϵ�y���@�Nˎ���f��ϵ�y���H�������ԗl���ߝ�ȹ����Ĵ̼���ጷ�ˎ����Ч�����[������������߀���ڹ����Ĵ̼��°l�������ğɹ�������Чָʾ�[��λ�c���@һ�������ڰl����Ӣ���ʼһ��W����Chemical Communications�s־�ϣ������x���������¡�
(TOC Graphic)
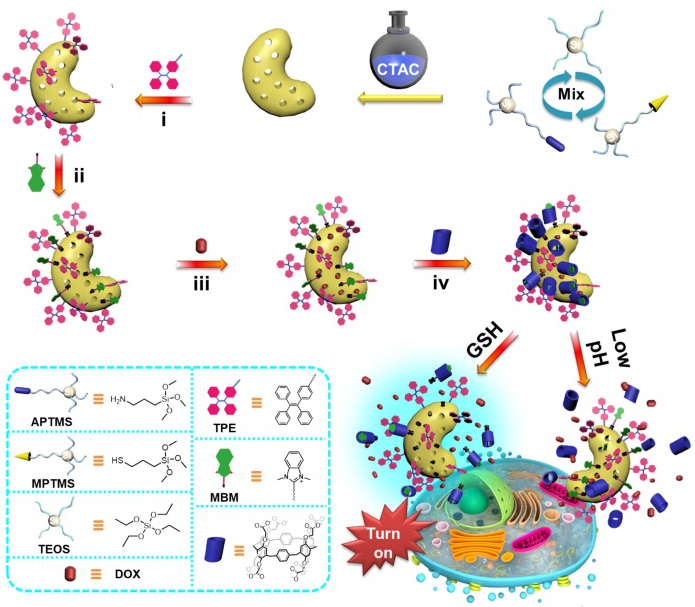
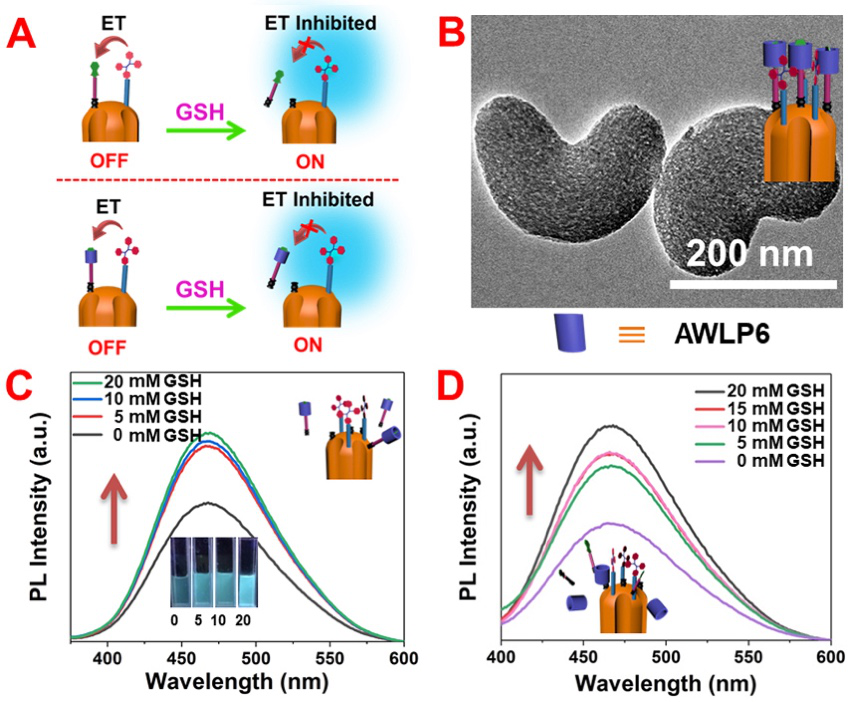
���ں���ͬĩ�˻��F���ЙC��Դ�������ò�ߴ�����LӰ푲�ͬ��ԓ�о��F��ڹ�Դ�������������У�������������3-�����������������鼰3-�����������������鲢�����ϣ��S��ͨ�^�cģ�儩ʮ����������Ȼ��@�������õ�һ�N��ò��һ�ľ����^��ȱ���e��Ҏ�t����ȫ����ò�㶹���裨MSNB��������ԓMSNB���溬�ɷN������܈F��-SH, -NH2�������c�������������քe������ͨ�^�����I�B�ӵij����Ӽ{���y�T ��MBM��1,3-������������AWLP6����x��ˮ����б�����N���;��оۼ��T���l�����|���ı�����ϩ��Ԫ���õ���һ�N���͵��p���ܻ��㶹����ˎ���f���wϵ��DF-MSNB����
��MBM��1,3-������������AWLP6����x��ˮ����б�����N���;��оۼ��T���l�����|���ı�����ϩ��Ԫ���õ���һ�N���͵��p���ܻ��㶹����ˎ���f���wϵ��DF-MSNB����
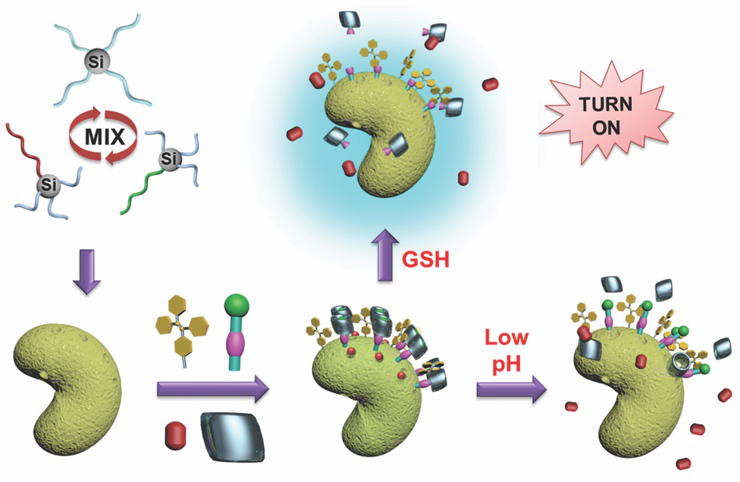
�D1. DOX@DF-MSNB�Ę���·������������pH��GSH�̼��µ�ˎ��ጷ��О飬�Լ�ԓ�wϵ��GSH�̼��°l���ɹ�������ʾ��D�����DƬ��Դ��Chem. Commun.��
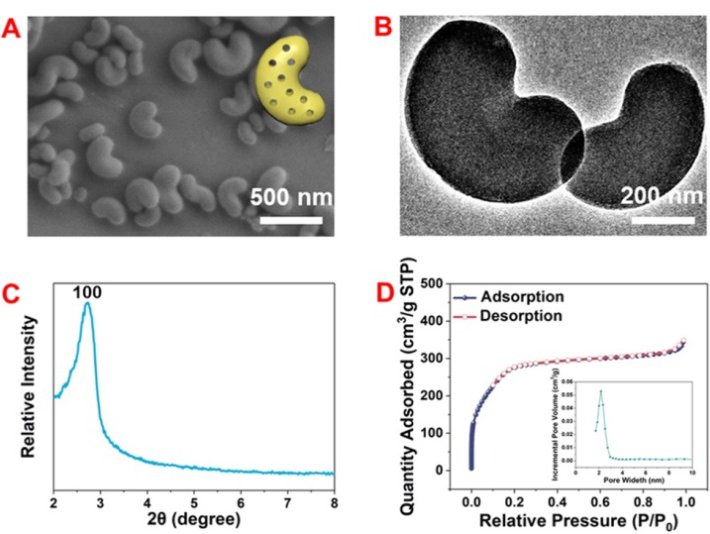
�D2. MSNB��SEM, TEM, XRD��BET���������DƬ��Դ��Chem. Commun.��
�̶���MSNB������ı���ϩ�������ڷ��Ӄ����D������չ�F�����õğɹ�����Ч������Ȥ���ǣ�����늺ɵĿ��w����MBM�c�ı���ϩͬ�r�������@�N�p���ܻ���DF-MSNB����r��MBM��ͨ�^����D���^�̲��ִ���ı���ϩ�ğɹ�ʹ�d�w�ʬF�^���ğɹ�l�䣬�����M���[�������ߝ�ȵ�GSH�����Д�����I�B�ӵ�MBM����Ч�����@�N����D�ƬF�Ķ�ʹ�ı���ϩ�ğɹ�֏ͣ��_��GSH�T���ğɹ�������Ч���������ڸ��õ�ָʾ�[��λ�c��
�D3. DF-MSNB��GSH�̼��µğɹ����������P���������DƬ��Դ��Chem. Commun.��
����ԓ���Ϳ�ǻ���m�������w��hAWLP6�c���wMBM֮�g���õ������w���ü���MSNB������o�ܵķ�����ã�ԓˎ���d�wչ�F����С��ǰጷţ����b�d����ˎ�ﰢù�أ�DOX�����d�wDOX@DF-MSNB�����ڟo�κδ̼��l���µ�ȥ�x��ˮ��33���H��10.5%��DOXй¶�������C����O�õ�ˎ��惦��������DOX@DF-MSNB̎���[��������pH�h���Еr��AWLP6ĩ�˵������ؓ�x��-COO-���D׃�����Ե��Ȼ�-COOH��ʧȥ�cMBM֮�g�^���������w���ã��M�������y�T�_��ጷŲ��σ��b�d��DOX�����[�������⣬�[��������ߝ�ȵ�GSH���Д��B��MSNB�� �Ķ����I����ʹ�y�TÓ���M��ጷ�DOX��Ч�����[����
�Ķ����I����ʹ�y�TÓ���M��ጷ�DOX��Ч�����[����
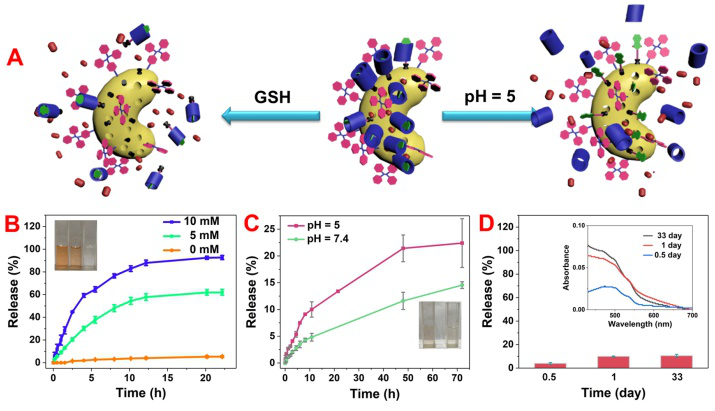
�D4. DOX@DF-MSNB������pH��GSH�̼��µ�ˎ��ጷ��О鼰��ȥ�x��ˮ�е�ˎ��ǰጷŌ����DƬ��Դ��Chem. Commun.��
������������ԓ�d�wDF-MSNB�������õ����������ԣ���ʹ��ȸ��_200 mg/mL��DF-MSNB����������μ���L02Ҳ���oӰ푣����b�d�˿���ˎ���DOX@DF-MSNB����ΰ�����HepG2չ�F���˸�Ч�Ě������á����⣬��DF-MSNB�cHepG2����������4С�r���Կ���ԓˎ���d�w�����M���[�������l������ҵ��{ɫ�ɹ⣬�C���䃞�����[����������������

�D5. �������Լ������������DƬ��Դ��Chem. Commun.��
ԓ�������H�����һ�Nȫ����ò�Ľ��{���㶹���Ƃ䷽��������չʾ��һ�N�µ�ͬ�r�߂仯�����[��λ�cָʾ�Ķ�ܳ�����ˎ���f��ϵ�y��������ò�{���d�w���Ƃ估���������Ϻͼ{���tˎ�Ę����ṩ����˼·��
���ϳɹ��l����Chemical Communications (Chem. Commun. 2019, DOI: 10.1039/C9CC07115F) �s־�ϡ�Փ�ĵĵ�һ���ߞ鼪�ִ�Wֲ��ƌW�WԺ�Tʿ�����㎛��Ŀǰ�ڼ��ִ�W���W�WԺ��Ӣ�������n�}�M�M�������B����ͬ��һ���ߞ鼪�ִ�Wֲ��ƌW�WԺ�n�������ؽ���������ͨӍ���ߞ���Ӣ����������ͬͨӍ���ߞ������¿��_˹�r����W���ڽ��������cԓ������߀�м��ִ�W�����t�W�WԺ���B�ɽ����ȡ�
- ������Ĵ�W�����ڣ��Ʊ���Ժʿ/�w�����ڈFꠡ�ACS Nano��������Ĥ����ľۼ��T���l�����������ۙ�͓p���Ŀ�ҕ�� 2025-01-21
- ������Ĵ�W�����ڣ��Ʊ���Ժʿ�c�w�����ڈFꠡ�ACS Nano���C�����ۼ��T���l����ό��F�߷ֱ�������� 2025-01-07
- �������Ʊ���Ժʿ/�������賯 AM������AIE���Լ{�ͺ�ˮ���z�Ŀɴ�������ʽ��Ϣ-���в��� 2024-03-23
- ��ɽ��W�S��䓽����о��F��ڳ����ӽ�ײ��ό��ЙC��Ⱦ����������ռ��ɿ�ጷ�ȡ���о����Mչ 2018-07-10
- ɽ�|��W�������ڈF� ACS Nano: Ӳ�ȿ��{�ľ��Ҷ����{���w���{���{��-��������ã���������ˎ���f�� 2025-06-12
- ���������ڈF� Bioact. Mater.����ˎ���f��ϵ�y"������-����-����ϵ�y���o"��λһ�w�fͬ����ʹ�L���P�����ί� 2025-06-04
- �K���f/��Ᵽ���ڈF���Ƹ��ʿ�� - ���Ϻϳɡ��{���t�W���[���\����ˎ���f�͡������ί��ȣ� 2025-04-29
