�������f���d�w�Ę�(g��u)���ѳɞ黯�W(xu��)�����όW(xu��)������W(xu��)���t(y��)�W(xu��)�ȶ��W(xu��)�ƾC�Ͻ����I(l��ng)���ǰ�غ͟��c(di��n)�����˽�Q���y(t��ng)�������������Ҳ��֡����ί�Ч�ʵ����Ҷ����������@�Ć��}����ģʽ�ί��ĸ��������ܵ��V���P(gu��n)ע����������ƌW(xu��)������������x���f���d�w�Ŀ��O(sh��)Ӌ�ԡ�������ԣ����ЙC(j��)�������ԇ������\����ˎ��ȹ������|(zh��)���뵽��x�Ӻ����f��ϵ�y(t��ng)�У��Ԍ��F(xi��n)���м�(x��)���Ķ�ģʽ�ί����w��(n��i)�⌍�Y(ji��)�������@�N��ģʽ�ί�ϵ�y(t��ng)���Ѓ�(y��u)����Ч������ͬ�rҲ�������Ƃ��^���У����ˌ��F(xi��n)��(g��u)������f���d�w��Ŀ��(bi��o)����Ҫͨ�^��(f��)�s�����������W(xu��)�������f���d�w�M(j��n)������f���d�w�������@Щ��ˮ���ܷ����Ժɱ���ĸ�׃�����������|(zh��)���Ƿ��܉��O(sh��)Ӌ����ͬ�r���_(d��)��N��ᡢ��������������������|(zh��)����ͨ�^�f���d�w��(d��o)��м�(x��)������ͬһ���м�(x��)�����_(d��)�������ܵ����F(xi��n)����Ķ�ģʽ�ί��DZ��о��ij��l(f��)�c(di��n)��
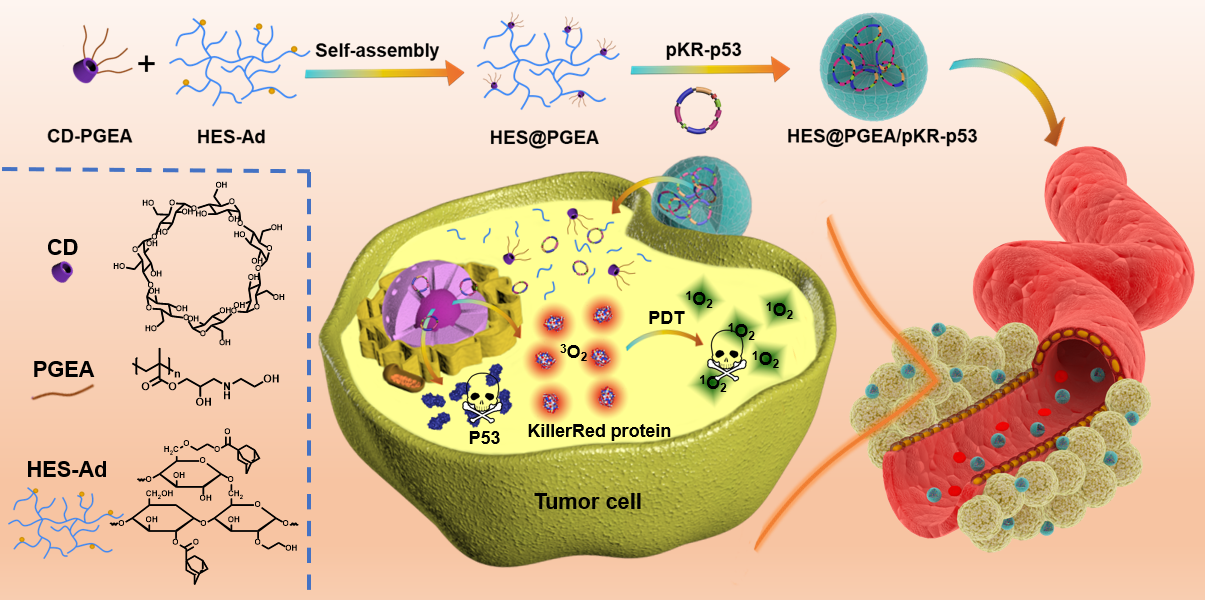
�D1. �����Ӻ���{���f��ϵ�y(t��ng)�Ę�(g��u)�����[����ģʽ�ί��^��
��D1��ʾ���츣�����ڈF(tu��n)��Խ���������u�һ����ۣ�HES-Ad�����Ҵ������ܻ��Ħ�-�h(hu��n)�������ۼ���ϩ��sˮ��������CD-PGEA������l(f��)�c(di��n)��ͨ�^�����ӽM�b�ķ�ʽ�õ����Ͷ��ǻ���x���f���d�w��HES@PGEA����ԓ�d�wͨ�^�y�������O(sh��)Ӌ�Ŀɷքe���_(d��)�������ף�KillerRed��KR�����[�����Ƶ��ף�P53�����|(zh��)����pKR-p53���M(j��n)���[�������F(xi��n)�����{(di��o)���µļ�(x��)������/������������pģʽ�ί���
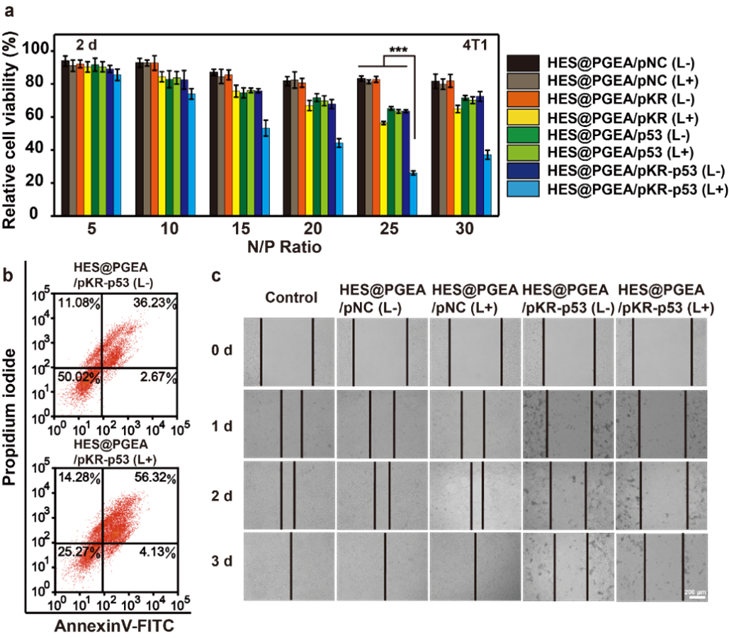
�D2. �w���[����(x��)�����ƌ������P(gu��n)�Y(ji��)��
ͨ�^�w���[����(x��)�����ƌ������P(gu��n)��(sh��)��(j��)���Ե�֪���D2��������چΪ�(d��)�f��p53��������͆Ϊ�(d��)�f��pKR�����M(j��n)�й�����ί����ί�Ч�������о�����(g��u)���ġ�pKR-p53��һ�w���|(zh��)���܉����d�w�Ĕy������ͬһ��(x��)����ͬ�r���_(d��)�ɷN�����_(d��)���f(xi��)ͬ������Ч����
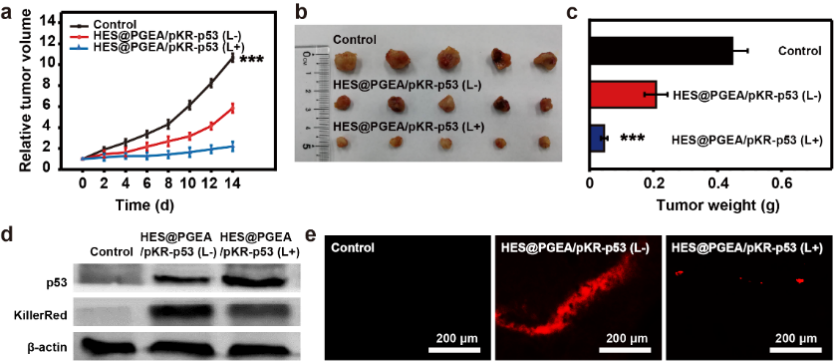
�D3. �w��(n��i)�����������P(gu��n)�Y(ji��)��
�о��F(tu��n)��M(j��n)һ���ں���С���w��(n��i)��C���@�N�����ģʽ�ί����ԵĿ����ԡ���D3��ʾ����������(g��u)���ĸ�ЧHES@PGEA�d�w���Գɹ��f��pKR-p53�|(zh��)���M(j��n)���[���M����(x��)�������_(d��)�ɷN���P(gu��n)���ס��ڹ����{(di��o)���£�ԓ�pģʽ�ί�����ȡ�������õ�����Ч�����@�N�����ģʽ�ί�ϵ�y(t��ng)��������[���Լ������������ί��ṩ���µ��ί����Ժ�˼·��
�������P(gu��n)�ɹ��ԡ�Genetically multimodal therapy mediated by one polysaccharides-based supramolecular nanosystem�����}�l(f��)����Biomaterials�ϡ�Փ�ĵĵ�һ���ߞ鱱��������W(xu��)���ϿƌW(xu��)�c���̌W(xu��)Ժ���S����ʿ�ʹTʿ�о�����������ͨӍ���ߞ��츣�����������Ȼ��������
Փ��朽ӣ�https://doi.org/10.1016/j.biomaterials.2020.120031
- �пƴ�������/����F(tu��n)� Nat. Biomed. Eng.: �O(sh��)Ӌ������ԭ��mRNA�f���d�w���w��(n��i)�ؾ���������APC 2025-04-01
- ����W(xu��)ʷ־�h(yu��n)���ڈF(tu��n)���Ƹ�������� - �߷��ӻ��W(xu��)�����z/����/֬�|(zh��)�w��ø�����f���d�w������ 2024-12-17
- ����W(xu��)ʷ־�h(yu��n)���ڈF(tu��n)���Ƹ�������� - �߷��ӻ��W(xu��)�����z/����/֬�|(zh��)�w��ø�����f���d�w�����켚(x��)�������� 2024-10-14
- ��ʮ���d�����������W(xu��)���Ǻӽ��ھ��������ۺ���朳����ӽM�b�c���ܻ�: �ך���Һ���ۺ������ 2025-01-14
- ͬ��(j��)��W(xu��)�����h������������W(xu��)�w����Ժʿ Nat. Commun.�������ӽM�b�w�ĄӑB(t��i)���Է��D(zhu��n) 2024-11-14
- ꃿƴ����W(xu��)���������A�����Wꖵ� Nano Today�����ڳ���������õ��Π��m��(y��ng)ˮ��ճ�ϲ��� 2024-04-24
- �K���־�h(yu��n)/�������K��һԺ����� Nat. Commun.���[��Ѫ���m��(y��ng)�ԡ�ճ���ԺͿ������������ڿɳ��m(x��)�Ľ�(j��ng)���}���W(xu��)˨���ί� 2025-07-09
�\���P(gu��n)ע�߷��ӿƼ�

- ���ܹ��A��朆���������22��...
- �������C(j��)����500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ��h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c(di��n)������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��
- �Ј���300�|��PMEC China ɫ...
- ����ע�ԣ�2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ(x��n)����...
- �Ї��ƴ����d���n�}�M���邐...
- �A��������W(xu��)���V�ա����ݴ�...
- �A�ώ����� Small���w�S��...
- �K���־�h(yu��n)/�������K��һ...
- ���������W(xu��)�����¡��S�؈F(tu��n)...
- �㽭��W(xu��)�߳����ڈF(tu��n)� ��Nat...
- ���д����ڣ��Ʊ��ҡ�����...
- �������/˾һ�����۳Ǵ�...
- ����W(xu��)�����h(yu��n)���ڈF(tu��n)� AFM...
- ��ɽ��W(xu��)����n�}�M CEJ����...
- ���ݴ�W(xu��)�����ƽ��ڈF(tu��n)ꠡ�Ac...