���ϱ�/����������_�l���ϸ߸���ֵ���õ���Ҫ�h�����oՓ������Դ���h������늺������ƌW�I��������Ҫ�����á����y�ľۺ��ﱡĤ��/������ԣ����ںϳɷ������s��ԭ���������������Բ��ȱ�c���b�ڴˣ�Խ��Խ��ķ�����/������Է����������Ŀǰ���^�·f�Ľ�Q���}�IJ������£�һ������������WMessersmith�n�}�M��2007�����ľ۶�Ͱ��wϵ�����ǰĴ�����ī������WCaruso �n�}�M��2013�����ĆΌ���(tannic acid, TA)-�F(III)�j����(Fe III -TA)�wϵ���@����wϵ�Ĺ�ͬ�������������������������Ĺ��r�I�ͷǹ��r�I(���I�������A�����ѷe��������)���������F���佻�ۺϺ��ڲ��ϱ�/�����𤸽�ԣ����F���ڶ�N���ϱ�/����Ĺ��ܻ����¼��g��;����������������ȱ�c�Dz��ϸ��Ժ�ı�/����ʬF��ɫ���ߺ�ɫ����Ͱ��ۺϙC����s���ۺϕr�g�L�����a�����オ���Բ����_��Ϳ�ӷ����Բ��Ϳ�ӱ�/����ֲڵȡ��@Щȱ�c���¾۶�Ͱ����wϵ�в����ڸ��¼��g�I���e���������tˎ�I�õ��V���Č��H���á���ˣ��lչһ�N�oɫ��������h�����ɽ��⡢�o��Ⱦ�������Ըߡ�𤸽�ԏ������m�Ը����܉�˷��۶�Ͱ��ȷ���ȱ�c��Ϳ���\���ڱ�/��������Ȟ���Ҫ��
���D׃�ܾ�ø��Phase-Transited Lysozyme��PTL��������ꃎ�����i�����n�}�M��2012�������Macromol Biosci, 2012, 12(8): 1053?1059������һ^�e�ڂ��y���ۘӵ����|�ۼ���������ۘӵ����|�M�b�wϵ��Ŀǰ���wϵ���ٰ����ɷN�·f�Y�����w�S�W�j�ͼ{�ױ�Ĥ�������ڸ���^���ϱ����挍�F����𤸽���ԣ���һ�N���Ρ����١��ͳɱ����������ݵĵ����|Ϳ�ӣ����ڽ��١��o�C���ۺ���ͻ�����{���w���ϳɹ�𤸽���n�}�M���Hϵ�y̽ӑ����M�b�C����Angew Chem Int Ed 2017, 56: 13440-13444���������F���ڶ�N�I��đ��ã��e���ڱ�/����D����������������ӹ��̡���/��������V�����[����Ϣ��ݔ�����ӷ��x����ЧѪҺ����ˎ�マጡ��ί������|���е��I��Adv Mater, 2016, 28(34): 7414-7423��Adv Mater, 2016, 28(3): 579-587��Angew Chem Int Ed, 2017, 56, 9331-9335; Adv Mater, 2018, 30(38): 1802851��Adv Funct Mater, 2018, 28(4): 1704476��Nat Commun, 2018, 9(1): 5443��Adv Mater, 2019, 31, 1803377��Adv Mater, 2019, 31(46): 1903973��Angew Chem Int Ed, 2020, 132(7): 2872-2881��Adv Mater 2020, 2000128����
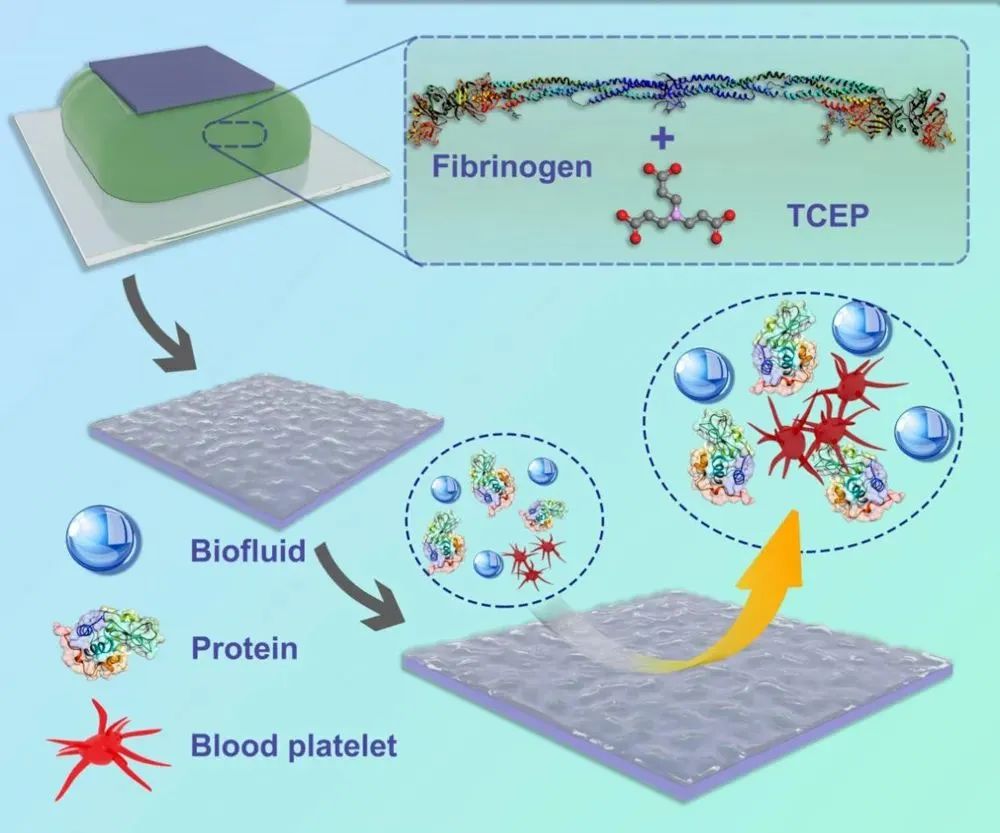
�����֮ǰ��������ܾ�ø�����ȷ������^С�ҽY���^�麆�εĵ����|�����о����x���w�S����ԭ��һ�N�������Y��������s���������خ����������ĵ����|��ͨ�^һ���������Ҝغ�ˮ���wϵ���Ƃ����w�S����ԭ���S�{�ױ�Ĥ���Ҍ���Y���c�����M���˳�����̽���Ϳ��ơ��Y��������Ϳ�ӷ����Ժã���W���Ըߣ����Է�������ģ�M����Һ�w�У����F�ˌ����١��o�C�ǽ��١��߷��ӵȲ��ϵı�����ԡ�������÷��棬�w�S����ԭ��Ĥ��һ�N��������Ϳ�ӣ��ӽ��چη���ˮƽ��6 nm ��ȼ��Ɍ������wҺ�������|��ѪС���������Ⱦ��F��ͬ�̶ȵĵֿ������⣬ԓͿ���Ƃ䷽�����Σ����ˏ��s�Ļ��W�����͌������|���A̎�����^�̡���ˣ�������������w�S����ԭ��ۘӾۼ���Ĥ��������һ����͵���������ϣ������ڿ�Ѫ˨��Ѫ��֧��Ϳ�ӡ�����Ϳ�ӵȸ�������tˎ�����I�����@�N�������خ����������ĵ����|ͨ�^��ۘӾۼ����D׃��ֿ��������ӷ��خ��������Ŀ���Ϳ�ӵ�˼·���Ɇ��l�҂�ȥ̽��������ڹ��ܵ�����ۘӾۼ��wϵ�Ŀ��ۙC�ơ�
�����������}�顰�w�S����ԭ��ۘӾۼ�Ĥ���Ƃ估�������о����l���ڡ��߷��ӌW��2020���8�ڡ��cף������Ժʿ80�A�Q������ (��������, �߷��ӌW��, 2020��51(8), doi: 10.11777/j.issn1000-3304.2020.20051)��Փ��ͨӍ���������i������ԓ�n�}�õ��ˇ�����Ȼ�ƌW����ί (No. 51673112) ���Ŀ���Y����
ԭ��朽ӣ�https://doi.org/10.11777/j.issn1000-3304.2020.20051
- �㽭��W��ӭ�������x����ڈFꠣ�IBE����Adv. Sci.������Ѫ���l�ӑB�������Ƃ�༉����������� 2022-12-02
- ����W�����h���ڈF� AFM���־õ��p���ԝ��p��Ϳ���x�貣��99.5%�ij������� 2025-07-08
- ��ɽ��W����n�}�M CEJ�����ßɹ�⧜猍�F�h������Ϳ����ʯīϩ���^��ɢ�Ŀ�ҕ���c�����u�� 2025-07-08
- ���ϴ�W������/����Ⱥ/���� Adv. Mater.����������ʿ�{�{��ܷ��������ݶȿ���Ϳ�� 2025-07-01
