�μ�������HCC��Ŀǰλ��ȫ�Y�l���ʺ�������ǰ��λ�����[���ί��^���У����y�������ڌ��������������P�����M�����ٵķ��خ��Լ������Զ��ܵ����ơ��ΰ����Եļ{���d�wˎ��ͨ�^���ˎ�����[���M�����[�������ȵķֲ���u�ɞ��tˎ�о��I��ğ��c֮һ����ˎ���������䝓�������ί�Ч����ͻ�������������Ԍ��[���ί��\����ЏV韵đ����_�l������
���գ����_��W���H�����tˎ�a�I���g�о�Ժꐴ�ȫ���ڈF���һ�^ֲ��ˎ���s־��Phytomedicine���ϰl�����}�顰Novel Chinese Angelica Polysaccharide Biomimetic Nanomedicine to Curcumin Delivery for Hepatocellular Carcinoma Treatment and Immunomodulatory Effect�����о�Փ�ġ������ڽ�������������������tˎ�w����Փָ���£��Y���˂��y��ˎ�w����Փ��ɫ���c�M�нY������Ԍ��F�ΰ����d�w�OӋ�����M��ϵ�ЙC��C���о���
���Ĉ����һ�N����ˎ���w��Ҫ���Գɷ֮��w���ǣ�APS��������Ǽ��M�а�����ļ{���d�w��ͨ�^���d������Գɷֽ��S���γɵĸʲݴ���-���w����-�����I-���S�ؼ{���z����GACS-Cur�������н��S��ǰ�wˎ�����ԡ�ͬ�r�������L�w���Lѭ�h�r�g����GACS-Cur�Լt����Ĥ��RBCm������������GACS-Cur@RBCm���Ա����w�Ⱦ��ɼ������ɣ��D1. ��������APS�������c�ΰ����������¶�����w��MR���Ͱ��������w��GR���خ��ԽY�ϣ���������ĸʲݴ��ᣨGA��С���ӿ��c�ΰ���������ĸʲݴ������w�Y�ϣ����ԓ�{���d�w���w����������K��

�D1. �[�������h����GACS-Cur@RBCm��ˎ���f��ʾ��D
���ĵĄ����c��
-
1. �����tˎ�w����Փָ���£��������w���ǡ��w�ν����{���d�w��
-
2. �����ϡ��ʲݣ��ʲݴ��ᣩ��ʹ���w�ν����{���d�w�����ˎЧ��
-
3. ������M�ֽ��S�ع��顰������ɫ���d���f���wϵ�У�������dˎ����ˎЧ��
-
4. ���_���w���Lѭ�hЧ��������t����Ĥ���d�w�M�а�����ͬ�r�_�����K�����������������á�
�Y��������APS�{���d�w�������õ��dˎ���������������Ժ��w����fͬ���w�ν������ΰ������á�ֵ��ע����ǣ��c���|�ᣨHA���{���d�w��ȣ�APS�{���d�w���и���Խ�ġ��w�ν������ΰ���Ч�ʣ��D2��3��������m��ˎ�d�w���߷��Ӳ��ϵİlչ��������d�w�������w�S�ṩ�˅��������������tˎ�F�������W�ƽ�����һ�����b���x��
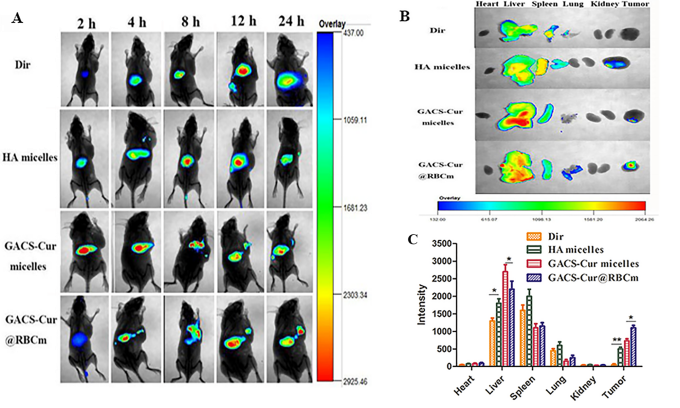
�D2. �������r�ɹ����ͽM���ֲ��Y��
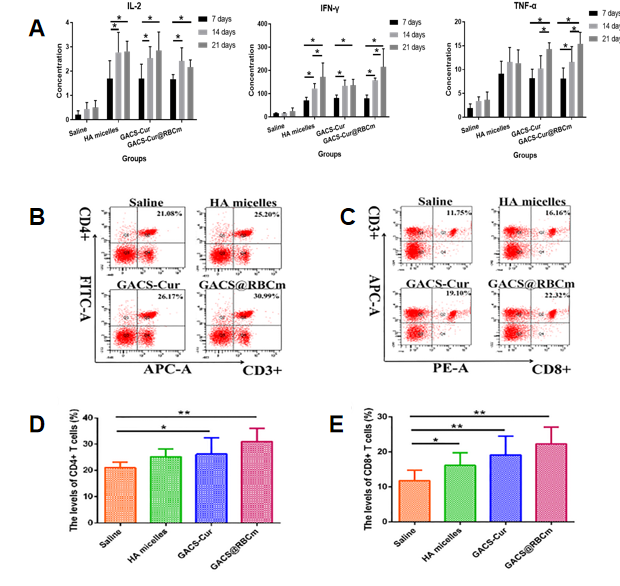
�D3. �����{���о��ĽY��
ɽ�|ʡ̩ɽ�W�ߡ����_��W���H�����tˎ�a�I���g�о�Ժꐴ�ȫ������Փ�ĵ�ͨӍ���ߣ��о������P������������������������������˴����Ĺ��������u��W�����x���������tˎ��W���G�����Ї����t�ƌWԺ�S������Ҳ���˴���������ԓ�����õ���ɽ�|ʡ̩ɽ�W�߹��̣�No.qnts20161035����ɽ�|ʡ��Ȼ�ƌW�����ش���A�о��Ŀ(No.ZR2019ZD24����ɽ�|ʡ�����������No.ZR2019YQ30�����Y��֧�֡�
Փ��朽ӣ�
https://doi.org/10.1016/j.phymed.2020.153356
DOI: 10.1016/j.phymed.2020.153356
- �V����W���P���� IJBM��XSBR�錧�������|�ۺ��� - һ�N��Q��Ȼ���ǻ���Ĥ���g�Ժ��Hˮ�Ե��²��Լ���ʳƷ���b�еđ��� 2025-06-23
- ����������W���x���R�������ڈF� ES&T: �՚�ֱ�ӝ����f�� 2025-06-01
- �������Ƽ�����WԺ�w�o Macromolecules�����I�������ǻ����z���F�������c�Ѽy�Uչ��׃ 2025-05-22
- �Ĵ���W�α�/���꼪 ACS Nano���߷��ӻ�����{��ƽ�_�ί��c�� 2023-12-24
- �A�������삥 Adv. Sci.�����ڼt������MOF-��ø���˹������s���w���ڸ�����Ѫ�Y�ί� 2023-12-17
- �L����Ч | ���Ͻ����ܽB�����ڈF��\�в�ʿ������Tʿ - ���ϡ������t�W���� 2023-09-23
- ���д����ڣ��w�� / �Ʊ��҈F� ACS Nano �����AIE�{���R�_ͻ���[������ - ���F���ʹ��\�� 2025-05-29
