��������ۼ��T���l��AIE�l���w(AIEgens) �о��ܵ����˂��ďV���Pע�����������ͼ����ί��\���W�������ȡ�����L����Mչ��Ȼ���������AIEgens���ÃH�����w��y����С�����С��ʹ������ڷN�g����@����������AIEgens ���R���D����������`�L���ģ���ڴ_���{��̽����������t�W���ü�����K�R���D�����L�U����̎����l�]����Ҫ���á���ˣ��������D��֮ǰ��������Ҫ���ڻ���M�W�����ʌW���������ܺ��z���������c����������Ե���N����������`�L�Ӻ�M���R��ǰ�о���
���գ��㽭��W������ں��A��������W/��ۿƼ���W�Ʊ���Ժʿ����ͨ�^��С�������С������ӣ�����Ӻ�ģ�ͣ�������AIEgens�M�й�W����������������g�M����ϵ�y�Ͷ�����ʾ���о�������Folic-AIEgen���FС���á���Ӻ��N����ģ�͵�ǰ���ܰͽY(SLNs)��z��������Ĥ��ɢ�Ե�СSKOV3��Hela�[���M��ָ���г����Y��������Folic-AIEgen������һ�N��Ч����ݵğɹ�̽ᘣ���SLNs��С�[���M�о��_�z�y��ԓ�R��ǰ�о����������ӿ�AIEgens���R���D���^��(�D1)��
�D1. AIEgens �Č���_������ʾ��D
������ģ�����о���Folic-AIEgen�錧�ğɹ����g������������������r�z�y���г�SLNs�Ŀ�����(�D2a)����Folic-AIEgenƤ��ע��������ǰצ��|����¶�N�C�ܰͽY�^���r�^���ܰͻ�����ע���Folic-AIEgen�M���ܰܣ�Ȼ���M���B�Y���N�C�ܰͽY��ע���30�����ң���365nm����������£��ܰܺ�Ҹ�CSLN�ɹ���u������Ҋ (�D2b, i&ii)��Folic-AIEgen�����⾀�������ܮa�������ҷ����ğɹ⣬�Ɍ��r����SLN�Ĝʴ_�������г�(�D2b, iii)��SLN�������@�����ğɹ���̖���s�錦��LNs��4��(P < 0.001)(�D2c, d)����Ҹ�C��LNs���֞��S��أ�Ƕ��֬���У����������SLNs��λ���g�г����y�ȡ������Mһ���C��Folic-AIEgen�ğɹ��ҕ�������g�����еĿɿ��ԣ���������ģ�����M���ˌ��rSLN�z�y���г�(�D2e)��Ƥ�½oˎ����365 nm����������£������^�܇����ܰ��������^�쵽Folic-AIEgen�ď��ɹ���̖(�D2f, i-iii)��ע���3 min, Folic-AIEgen�ğɹ��Mһ�������ܰܣ����B��̎��SLNs�o���R�e���[����֬���M���С��S����������������^�mۙFolic-AIEgen�ɹ⣬���Ԝʴ_�R�e���г�SLN(�D2f, iv-vi)���c����LN��ȣ�SLN���и����ğɹ���̖(�D2g, h)�����⣬Folic-AIEgen���ܰ�ϵ�y�Ⱦ������õ������ԣ�����SLN�зֲ�������Ҫ���ǣ� Folic-AIEgen�ďV���ֲ����]������SLN�M�����ΑB�W��׃������Folic-AIEgen�����^�ߵ�����������(�D2h)��
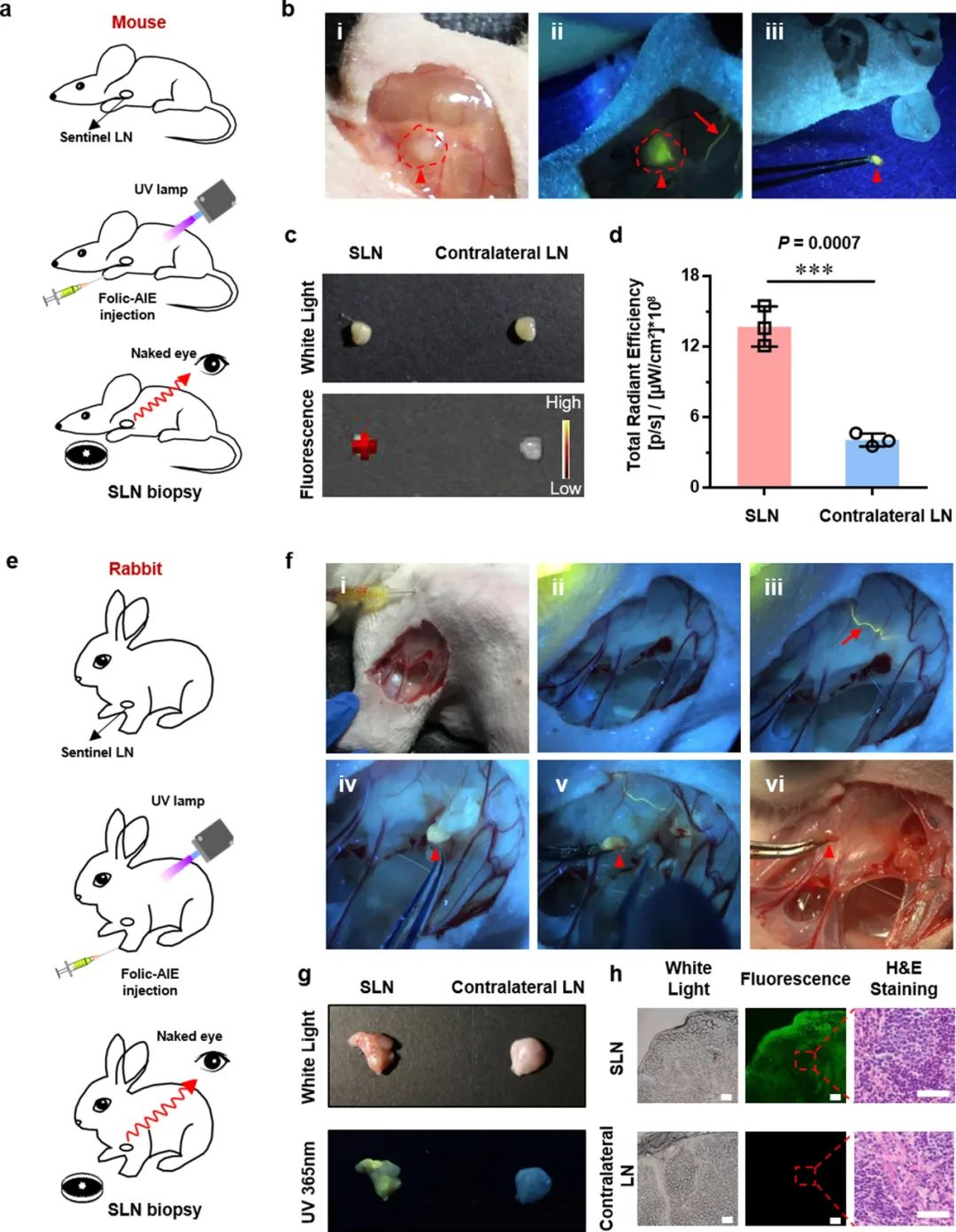
�D2. ����folic-AIEgen �ğɹ����g�������ڌ�������Ä���ģ��SLNs��z
Ŀǰ���{�ײ��ϱ��V���OӋ����������g���������ڴ��̈́��������`�L������M�оC���u�����b�ں�Ӻ��c������S������֮̎������Ӻ���R��ǰ�о����ڼ{�ײ��ϵ��R���u�����R���D�����P��Ҫ��ֵ��ע����ǣ���Ӻ���Џ��s�Ľ��ʽY��������Ҹ�C�ȱ����С���ȵ��ܰͽY���@�c�����������ȫ��ͬ����ˣ������ں�Ӻ�ģ�����Mһ���о��˻���Folic-AIEgen�ğɹ����g��������SLNs��z�Ŀ����ԺͿ��؏���(�D3a)���ں�Ӻ��҂��镞Ƥ��ע��Folic-AIEgen (�D3b, i&ii)����ע���s2 min�����ܰ��п����^�쵽Folic-AIEgen�ğɹ�(�D3b, iii)��֮��Folic-AIEgen�������ӣ���15 min��ͣ����SLN̎���c�����SLNʾۙ����ȣ�Folic-AIEgen��SLN�ȵı����r�g���L���@��Ч�������SLN��z�Ĝʴ_�Ժ��؏��ԡ����⣬Folic-AIEgen�ṩ�ĕr�g�g��Ҳ������t��ͨ�^�ɹ���̖��λ���г�LNs�ṩ�����ĕr�g��������⼤�l���Sɫ�ɹ������£���SLN�г�(�D3b, v)���г��ɹ���̖��ʧ������SLN�ѳɹ��ľֲ��ܰ�ϵ�y���г�(�D3b, vi-viii)�����г���SLN�п����^�쵽���ҵğɹ���̖������������LN�Л]�Йz�y�����@�ğɹ�(�D3c-e)���c�����Y��һ�£�Folic-AIEgenδ����SLN�M���l���κ��ΑB�W��׃��������������õ�����������(�D3e)��

�D3. ����Folic-AIEgen �ğɹ����g�������ں�Ӻ��SLNs��z
�C�����������о������AIEgen�ĺ����Ƃ估���ڟɹ����g�����еĶ�ܑ��á����÷����ğɹ�ͺ��m�ijߴ磬AIEgen�ѳɹ����ڏ�С�����`�L�Ӻ��ǰ���ܰͽY���`���z�y�;��_��λ���о��Y��������AIEgen ��������һ�N��Ч�ҷ���ğɹ�̽�����ǰ���ܰͽY��z�;��_�z�yС�[����ԓ�����������`�L�����R��ǰ�о��ṩ���Ѓrֵ�Ĕ������@���O��ش��M����AIE�İl��̽����R���D���е��Mһ���lչ��
ԭ����Ϣ��Aggregation-induced emission luminogens for image-guided surgery in non-human primates, Nature Communications, volume 12, Article number: 6485 (2021)
Փ��朽ӣ� https://www.nature.com/articles/s41467-021-26417-2
- ������Ĵ�W�����ڣ��Ʊ���Ժʿ/�w�����ڈFꠡ�ACS Nano��������Ĥ����ľۼ��T���l�����������ۙ�͓p���Ŀ�ҕ�� 2025-01-21
- ������Ĵ�W�����ڣ��Ʊ���Ժʿ�c�w�����ڈFꠡ�ACS Nano���C�����ۼ��T���l����ό��F�߷ֱ�������� 2025-01-07
- �������Ʊ���Ժʿ/�������賯 AM������AIE���Լ{�ͺ�ˮ���z�Ŀɴ�������ʽ��Ϣ-���в��� 2024-03-23
- ��ɽ��W����n�}�M CEJ���ڟo�����AIEgens����r�£������̘I���������̻����Ĵذl�����|���F�h��Ϳ�������p���z�y 2024-09-26
- �ۿƴ��Ʊ���/��ƿ� Nat. Commun.�����s�hAIEgens����Ч�����{�� 2023-07-21
- �����˄P�о��T����ǹ���ڈF�����Small�������а�l��Ͷ��ش̼�푑��� Janus- AIE �{���w�S 2022-05-24
- ��������˹�����tˎ���о�������Ƹ�о��T/���С���ʿ��������ؔ������/����ҹ��������� 2023-12-18
