ˎ����ӵļ������D����ˎ���f��ϵ�y�зdz���Ҫ��һ�h���������ӻ��Hˮ��ˎ���Ĥ�f����Ȼ��һ���ش����𡣼���Ĥ�ģ�cell penetrating peptides, CPPs����һ���x�Ӷ��ģ�������Ч���^����Ĥ���y������������|�M�뼚����һ���J��CPPs����ͨ�^һ�N���N;���M�뼚�����������r�£���������Ҫ�Ĕzȡ;����ͨ�^����;���f�͵ľ����������ɱ���ăȺ��w/��ø�w�Ĝ����ͽ��⣬�@Щ�����Գɞ��˽��ͼ������f��Ч�ʵ���Ҫ���ء����������ñ����ƻ��ȳ��^�ֵ�r��CPPs��ͨ�^ֱ����λ�C���M�뼚�������п��γɽ錧��ֱ����λ�C���Կ��ٸ�Ч�Ĵ�Ĥ���ݳɞ����о����c����������_��W���W�WԺ��ꖈF��״λ��ڿ��γɵĻ���ԭ���OӋ�ϳ���һϵ�и����������Ĥ�ۺ�����ԓ�ۺ����ͨ�^���γɽ錧�ķǃ��̙C����Ч�M�뼚�����ĸ����Ͻ�Q���������`�Ć��}�����䑪���ڻ����f�ͣ�PT25-R2-C6�@ʾ����PEI 25K���ߵ��DȾЧ�ʺ��͵ļ������ԡ�
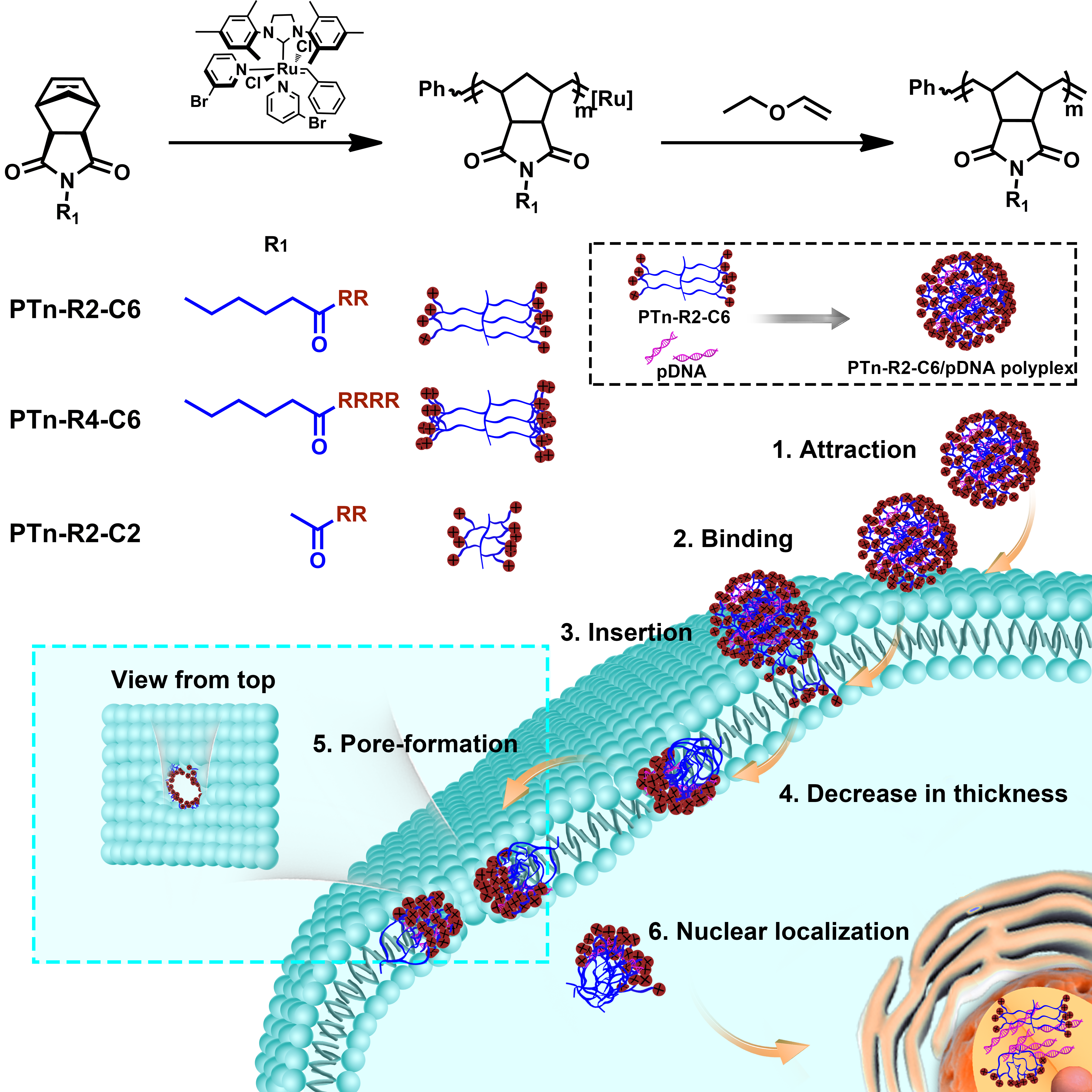
ͨ�^����ͬ��朽Y���ۺ���ĺY�x���_�������NԪ���DZ��C��Чֱ����λ���P�I��������1�����H��ˢ��ۺ���Y���ԽM�b�ɼ{���w�����γɾ۴���x�Ӛ���������Ĥ�ľֲ���_�ӣ���2������Ƭϩ���Ͷ���֮�g��������ˮ�B�ӱ������ڌ�����������Ă�朲�����֬�p���ӌӵ���ˮ�^���c�h�ˌ�����ã���3��������m���ľ�����H���Ա��C�ɿ�������߀���Ա��C��ȫ�ԡ�PTn-R2-C6��һ�N�ˢ��ۺ����ÿ�l������Ѓɂ������ᚈ����һ�����Լ����B�ӱۣ��܉���Ч���ڼ���Ĥ���γɿײ�ͨ�^ֱ����λ�C�ƃȻ��������У��D2����
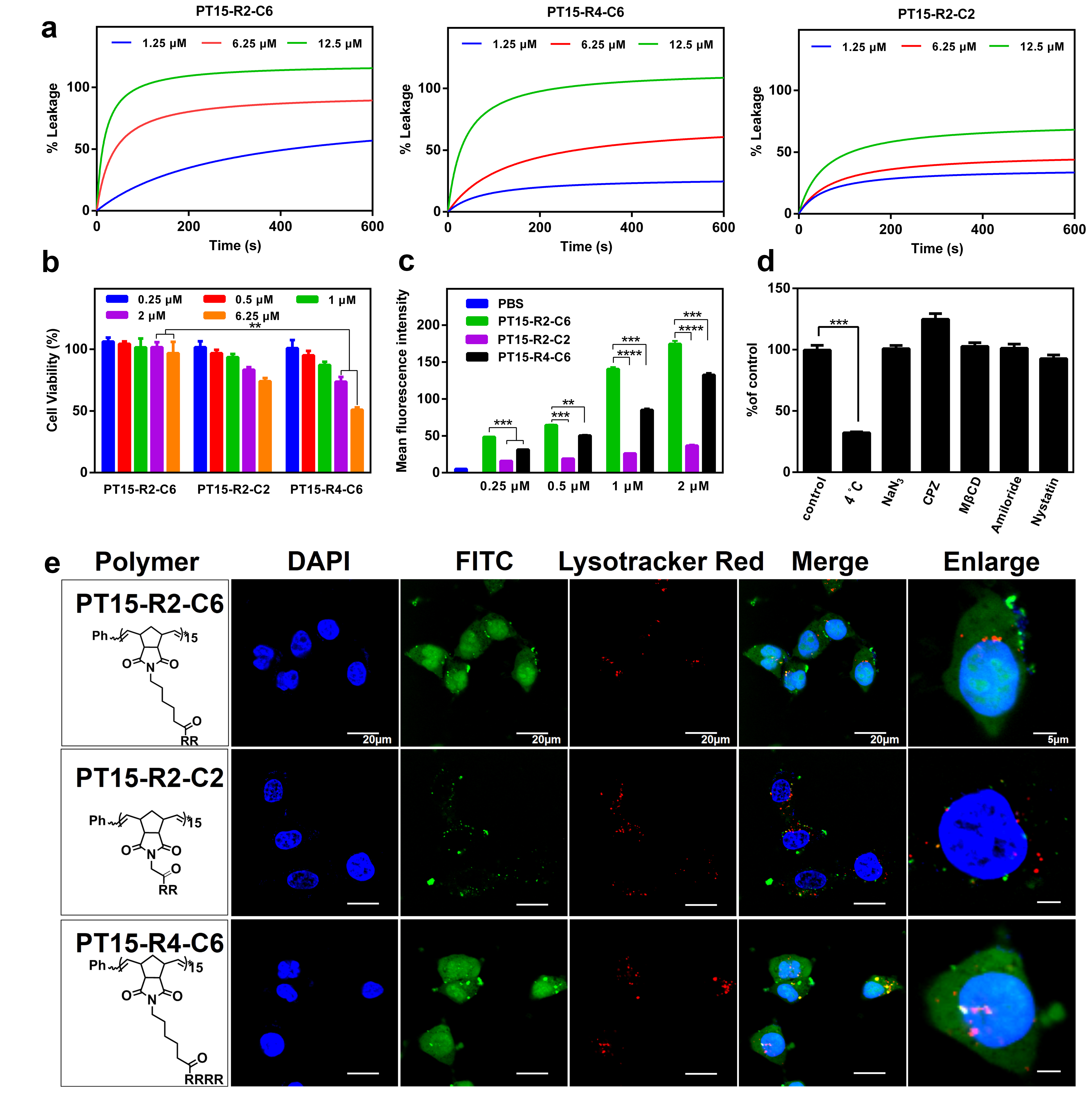
���⣬�F�߀�о���PTn-R2-C6��������f���d�w�ĝ�����PTn-R2-C6��ͨ�^��ͬ��ֱ����λ�C�ƌ��|���\ݔ�������|�У��D3a����ͨ�^�{��PTn-R2-C6�ľۺ϶ȣ��Mһ�������DȾЧ�ʡ�PT25-R2-C6�@ʾ����PEI 25K���ߵ��DȾЧ�ʣ��D3b�����͵ļ������ԣ��D3c����PTn-R2-C6�ۺ���İl����ˎ��ĸ�Ч�����ٵĿ缚��Ĥ�����f���ṩ��һ���Ѓrֵ��ƽ�_���ڼ����ί��������_�l�����̵��I����о�đ��Ý�����

�D3. �ۺ���PTn-R2-C6�����ڻ����f�͵��о�
�������P�ɹ��ԡ�Arginine-Rich Polymers with Pore-forming Capability Enable Efficient Intracellular Delivery via Direct Translocation Across Cell Membrane�����}�l���ڡ�Advanced Healthcare Materials���ϣ�ԓՓ��ͨӍ���ߞ����_��W���W�WԺ�߷��ӻ��W�о���������ڡ�ԓ�о��õ��˿Ƽ������c�аl����Լ�������Ȼ�ƌW������Ŀ֧�֡�
- �Ͼ��֘I��W�S����/��ȼ�A�n�}�M Nat. Protoc.�����늼��{���w�S�İ����f�ͼ����ڼ��������ί��đ��� 2025-01-23
- �A��������W���x�F� Nano Lett.�����ۘ�׃�²��϶���ί�����Ɲ��Ĭ�Y 2024-10-09
- �|�A��W������/ʷ��ꖽ��ڈF� ACS Nano��������Եĺ��ט����������ͨ���͵����|�f��ϵ�y���������Ŀ����ί� 2024-01-12
- ����������ꐝ�/����ϼ�F� Angew����ˢ��ۺ������z�������Ӿ��w�Ĺ��܄�׃ɫ�`���ȷ���ȡ���Mչ 2024-08-26
- ���₥���ڈF� Mater. Horiz.��ˢ��ۺ����Ƕ�D����Һ�B���پW�j���F��Ч�ӑB����� 2023-11-26
- ������\�s���ڈFꠡ���������ȺԺʿ����܊���ڈFꠡ�Mater. Horiz.��: ͨ�^������朻��i��������Ì��Fˢ��ۺ����ڐ��ӭh���µ����ޏ� 2023-04-07
