�ڼ���p����spinal cord injury, SCI���IJ��������^(gu��)���д��ڃɂ�(g��)��Ҫ���،�(d��o)������(j��ng)�ޏ�(f��)���y��һ�Ǔp�������ڵļ�(x��)���d�^�Զ��ԭh(hu��n)����(d��o)�µ��^�l(f��)�p����(j��)(li��n)����(y��ng)�����Ǔp���к��ڵ������z�|(zh��)��(x��)���^(gu��)�ȼ������ֳ��(d��o)�µ��z�|(zh��)��������(g��u)������(j��ng)���������ϡ��о��@ʾ����SCI�����ڣ�������(x��)��ጷŵ��d�^�����ጧ(d��o)��������(x��)����N-��-D-���T���������w��NMDAR���^(gu��)�ȼ����(j��ng)NMDAR�錧(d��o)�ļ�(x��)���}��(n��i)�����ӣ���(d��o)���}���d�������d�^�Զ��Լ�(x��)����������������Ԃ������^�l(f��)�ԓp����ȱ������(x��)�����x�a(ch��n)������Խ��|(zh��)����e߀��(hu��)��(d��o)�¾ֲ�pH�½�����(d��o)�¾ֲ��M�����ж���ͬ�r(sh��)���ҹ�Ĥ��(x��)����ijЩ��Ⱥ��SCI���D(zhu��n)������(j��ng)�ɼ�(x��)����neural stem cells, NSCs�������M(j��n)һ�����z�|(zh��)��(x��)���ֻ����γ��z�|(zh��)�ۡ��M���z�|(zh��)����SCI���������˼�(x��)�����Է��Ӻ��װY���ӵĔU(ku��)ɢ��Ȼ�����к��������ɞ����Sͻ���������ϡ���ˣ���༚(x��)���^�l(f��)�ԓp������(y��ng)��ͬ�r(sh��)��(du��)��(n��i)Դ��NSCs�ķֻ��M(j��n)���{(di��o)���Ǵ��M(j��n)��(j��ng)�ޏ�(f��)���P(gu��n)�I��
���о��@ʾ���V�x�ӣ�Mg2+�����Ը�(j��ng)��(zh��ng)����� NMDAR ��늉��T���}ͨ�����p�ټ�(x��)���}��(n��i)�����Ķ��p���d�^�Լ�(x��)�����������R���У��V�ѱ��V�����ڶ�N��r�µ���(j��ng)���o(h��)�������ӰB����(chu��ng)�����X�p�����XȱѪ�����L(f��ng)������ɭ�ϲ���Ȼ����Ѫ-�������ϵ�Mg2+�D(zhu��n)�\(y��n)�������ޣ���(j��ng)�o�}���m(x��)ע��߄���Mg2+�H��ʹ�X��Һ�е�Mg2+�p�����ߡ��R���Ͻ�(j��ng)�o�}��(y��ng)���V���ί�SCI��δȡ��һ����Ч�ĽY(ji��)������ˣ�ͨ�^(gu��)ֲ����������ڼ���ֲ�ጷ�Mg2+�l(f��)�]��(j��ng)���o(h��)���ÿ�����һ��(g��)����Ч�IJ��ԡ�
�������ϱ������K�ݴ�W(xu��)�ǿ��о���ِ�������n�}�M������n�}�M�����Ƃ��˽��MgO�w����ؓ(f��)�d��(j��ng)�ΑB(t��i)�l(f��)����Purmorphamine��PUR����Retinoic acid��RA����Ȼ���c�ۣ�L-������-co-��-����(n��i)������PLCL��ͨ�^(gu��)�o늼��z���g(sh��)�Ƃ��˶����w�S֧�����ޏ�(f��)����p�����D1������(sh��)�(y��n)�ɹ�����Magnesium Oxide/Poly (L�\lactide�\co�\�ũ\caprolactone) Scaffolds Loaded with Neural Morphogens Promote Spinal Cord Repair through Targeting the Calcium Influx and Neuronal Differentiation of Neural Stem Cells�����}�l(f��)���ڡ�Advance Healthcare Materials���ϡ�
�о������u(p��ng)���˲�ͬ��ȵ�MgO/PLCL֧�ܵ��^��ò�����W(xu��)���ܡ��Hˮ�ԡ�Mg2+ጷ������ͼ�(x��)��ճ�����ܺ��x��MgO:PLCL = 25:100��ȵ��w�S֧���M(j��n)�к��m(x��)ԇ�(y��n)��
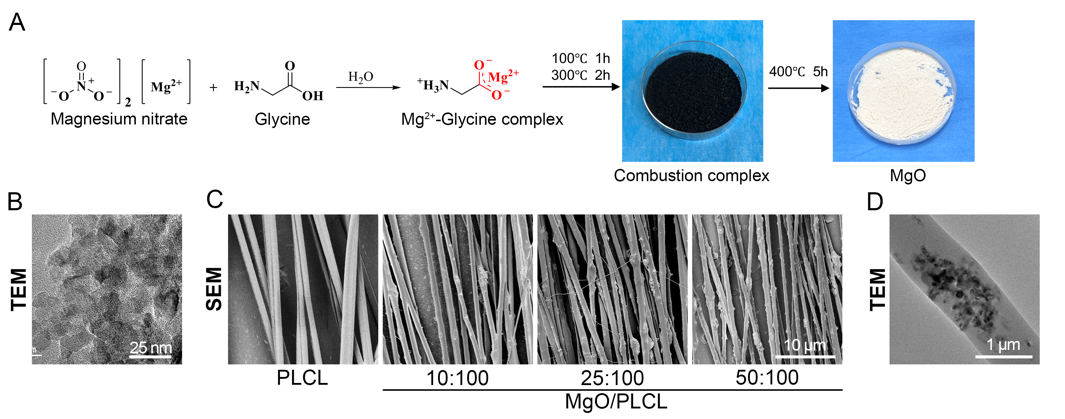
�D 1 ���MgO�ĺϳ��c��ͬ���MgO/PLCL�w�S���Ƃ䡣
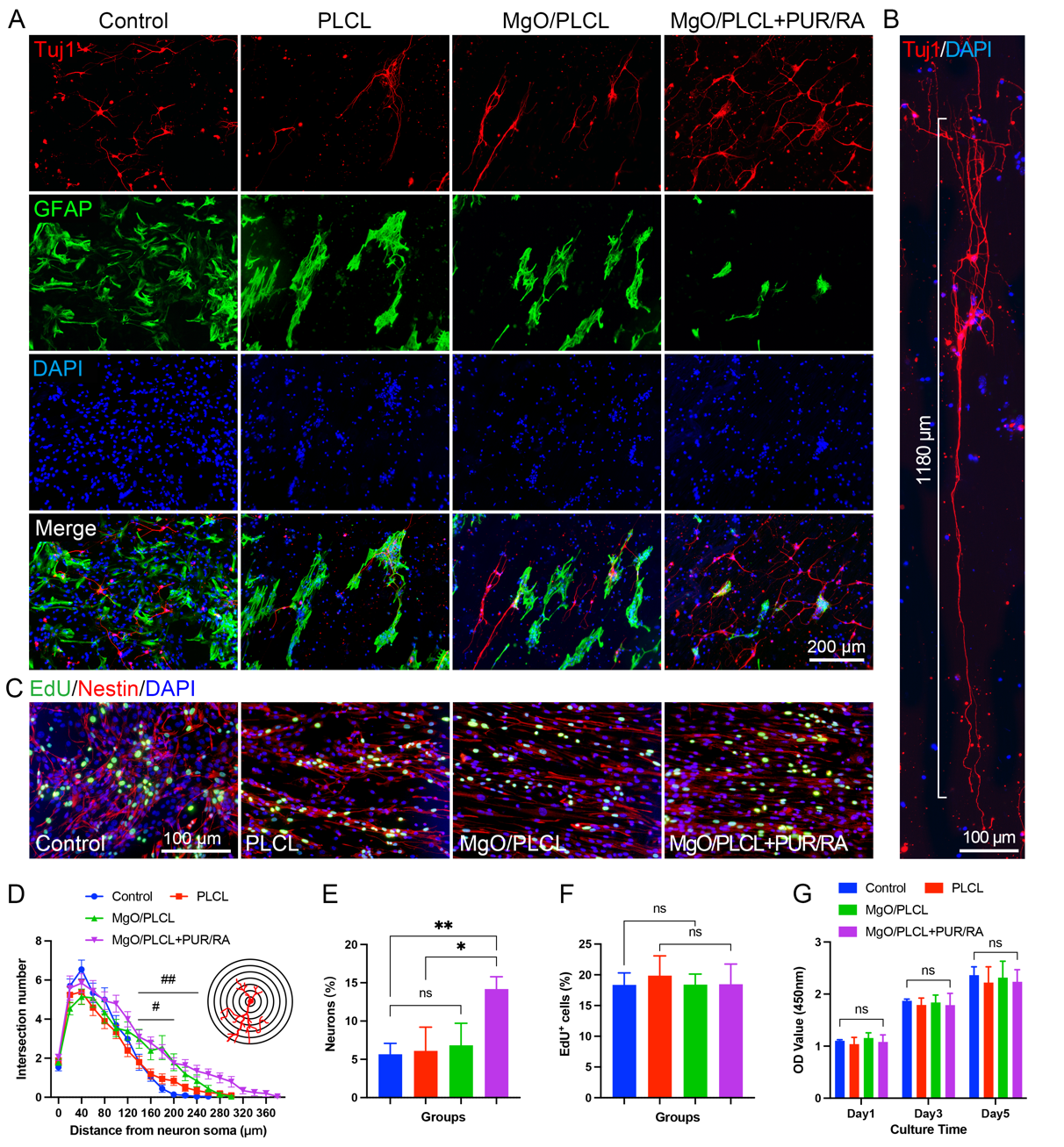
�о������w��ģ�M�˼���p��������ԭh(hu��n)�����d�^�Զ��ԭh(hu��n)�����l(f��)�F(xi��n)MgO/PLCL֧���@�ɷN�l���¾��ܱ��o(h��)��(j��ng)��(x��)���Ĵ��D2���D3�������⣬ؓ(f��)�dPUR/RA��MgO/PLCL֧���@�����M(j��n)��NSCs����(j��ng)Ԫ����ķֻ����p�����z�|(zh��)��(x��)�����γɣ��D4����ͬ�r(sh��)����(du��)��(j��ng)Ԫ�Sͻ�ΑB(t��i)���M(j��n)һ�������@ʾ��ؓ(f��)�dPUR/RA��MgO/PLCL֧���@�����M(j��n)���Sͻ�����L(zh��ng)��

�D 2 MgO/PLCL֧�ܵļ�(x��)��ճ�������Լ������ԭh(hu��n)���Ќ�(du��)��(j��ng)��(x��)���ı��o(h��)���á�

�D 3 MgO/PLCL֧���p����NMDA�T��(d��o)����(j��ng)Ԫ�}��(n��i)������(j��ng)Ԫ������
�о����M(j��n)һ����(g��u)����С����T9���Гp��ģ�ͣ���ֲ��֧�ܡ��Y(ji��)���@ʾ��2�ܺ���M�ļ����(n��i)Դ��NSCs����Ҋ(ji��n)�����MgO/PLCL+PUR/RA�M�ļ���������п�Ҋ(ji��n)����Nestin+��(x��)�����c֧���γɼ�(x��)��ͨ·���������@ʾ��Nestin+ NSCs ͨ�^(gu��)������������w�S֧�ܵ��w�ơ�ͬ�r(sh��)��MgO/PLCL+PUR/RA�M�p���܇��ĵ�����(x��)���@���p�٣���(x��)�����ࣨ�D5������֧��ֲ��8�ܺ�MgO/PLCL+PUR/RA֧���@���p���˓p���^(q��)��������z�|(zh��)��(x��)����GFAP��(bi��o)ӛ���ļ�������M(j��n)�˴�����(j��ng)Ԫ���γɣ��D6����

�D 5 MgO/PLCL+PUR/RA֧�����w��(n��i)���M(j��n)��(n��i)Դ��NSCs������w�ƣ��p�ټ�(x��)��������

ԓ�о���SCI�IJ�������C(j��)�Ƴ��l(f��)��ͨ�^(gu��)��(f��)�ϲ���ͬ�r(sh��)���A(y��)��SCI����^�l(f��)�ԓp����(j��)(li��n)����(y��ng)���z�|(zh��)����������(j��)Ϥ���@�Ǻ��V�������ֲ���ޏ�(f��)SCI���״��о����K�ݴ�W(xu��)�ǿ��о���ِ��������������ڞ鱾��ͨӍ���ߣ��xӋ(j��)��(l��)����ҷf��ʿ���鱾�ĵ�һ���ߡ�
- �������/˾һ�����۳Ǵ����ɏ Adv. Mater. �C����Janus�o늼��zĤ 2025-07-08
- �Ї�(gu��)�r(n��ng)��Ժֲ�����������о��T Small����(y��u)���Ŀɇ�ʩ���w�S�d�w���ڸ�Ч�r(n��ng)ˎ�f�� 2025-06-13
- �Ї�(gu��)Ӌ(j��)����W(xu��)�l(w��i)��(gu��)Ӣ/����Ƽ Adv. Sci.���������o늼��z���g(sh��)�Ƃ��Ч���ޏ�(f��)���ܵķ����gͿ�ӷ���ȡ����Ҫ�M(j��n)չ 2024-12-31
�\(ch��ng)���P(gu��n)ע�߷��ӿƼ�

- CPHI����չ��(sh��)�(y��n)�҃x���c�O(sh��)��...
- ���ܹ��A��朆���������22��...
- ����(b��o)���C(j��)��(hu��)��500+ˎ��...
- ��(gu��)�HƷ�ơ�ǰ�ؕ�(hu��)�h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c(di��n)������...
- ��(gu��)�a(ch��n)������٣����(gu��)���^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��(hu��)
- �Ј�(ch��ng)��300�|��PMEC China ɫ...
- ����ע��(c��)��2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �Ĵ���W(xu��)���A���ڈF(tu��n)�(du��)��Adv....
- �Ĵ���W(xu��)���������ڈF(tu��n)�(du��) Ang...
- �A��������W(xu��)���ָ���ڈF(tu��n)�(du��)...
- �칤����x/�R�w�R/���ƽ� S...
- �A���r(n��ng)�����/������...
- �Ʊ��ҽ���/�֘s�I(y��)���ڈF(tu��n)�(du��)...
- ��ӿƴ����|��/�������F(tu��n)�(du��)...
- �A������������� Angew: ...
- �Ĵ���W(xu��)������ AFM������ʯ...
- ��۳��д�W(xu��)�����n�}�M CEJ...
- �Ї�(gu��)�ƴ����d���n�}�M���邐...