�Ĵ���W�����h�����n�}�M��Adv. Mater.���� ��̫����B�����l�Ļ��������w��ܺ��������푑���miRNA�f��ϵ�y
2022-08-01 ��Դ���߷��ӿƼ�
miRNAĿǰ���C�����c�����������w�ȵ������{�������miRNA�ں���ˎ���I��ľ��о�đ��Ý�����miRNA�ί�������ɞ���miRNA�I���о��ğ��TԒ�}��Ȼ������miRNA�IJ������ԘO��������miRNA�ί��đ���ǰ�������yˎ���f��ϵ�y���s���Ƃ��^�̣��^�ߵ����ﰲȫ�L�U���^����DȾЧ��Ҳ�o��miRNA�ί��l�]���ĝ��ܡ�
�Ĵ���W�����h�����n�}�M�ڡ�Advanced Materials���ϰl�����о����¡�A Tetrahedral Framework DNA-Based Bioswitchable miRNA Inhibitor Delivery System: Application to Skin Anti-Aging���� 10.1002/adma.202204287����ԓ�F��ܵ����A�Ļ��z�a��־��̫����B���Ć��l���OӋ��һ�N�����l��ͬmiRNA�����B����β��ӭh�@����Ǽܣ�̫ꖣ��Ļ��������w��ܺ��������푑���miRNA�f��ϵ�y��BiRDS�������^�ڂ��y�\�dϵ�y��BiRDS�����������w��ܺ��ᣨtFNA�������S���ͱ��F�����^�����������������ԓ�Y����С�ߴ�����ʹ����к��ĽM���B�ԡ�BiRDS�o���˱��D�\miRNA��ֱ��o���oՓ���ڸߝ��ø��Ѫ��l���¾����F����ɫ�ķ����ԡ�����֮�⣬��ԓ�Y���Ȳ��OӋ�ˡ����͡�β��̎��Ҫ�Y�����Ķ����FBiRDS������푑��Լ����D�\miRNA�Ĺ����ԡ�ԓ�о�ͻ���˂��y��ܺ����\ݔmiRNA��ģʽ����Q��miRNA�ί��Ķ̰��ͬ�rҲ�����������������f���ṩ��һ�l��˼·��

ԓՓ�ĵ�һ����λ�Ĵ���W�A����ǻ�t�WԺ��ʿ�о������ɺ����Ĵ���W�A����ǻ�t�WԺ�����h���ں�����Ȼ���о��T��ԓ��ͨӍ���ߣ��Ĵ���W���һ��Ɇ�λ��ԓ�о��õ��ˇ������c�аlӋ����2019YFA0110600���͇�����Ȼ�ƌW����81970916��81671031��81800947)���Ŀ��֧�֡�
ԭ��朽ӣ�https://onlinelibrary.wiley.com/doi/10.1002/adma.202204287
�Ĵ���W�����h�����n�}�M�ڡ�Advanced Materials���ϰl�����о����¡�A Tetrahedral Framework DNA-Based Bioswitchable miRNA Inhibitor Delivery System: Application to Skin Anti-Aging���� 10.1002/adma.202204287����ԓ�F��ܵ����A�Ļ��z�a��־��̫����B���Ć��l���OӋ��һ�N�����l��ͬmiRNA�����B����β��ӭh�@����Ǽܣ�̫ꖣ��Ļ��������w��ܺ��������푑���miRNA�f��ϵ�y��BiRDS�������^�ڂ��y�\�dϵ�y��BiRDS�����������w��ܺ��ᣨtFNA�������S���ͱ��F�����^�����������������ԓ�Y����С�ߴ�����ʹ����к��ĽM���B�ԡ�BiRDS�o���˱��D�\miRNA��ֱ��o���oՓ���ڸߝ��ø��Ѫ��l���¾����F����ɫ�ķ����ԡ�����֮�⣬��ԓ�Y���Ȳ��OӋ�ˡ����͡�β��̎��Ҫ�Y�����Ķ����FBiRDS������푑��Լ����D�\miRNA�Ĺ����ԡ�ԓ�о�ͻ���˂��y��ܺ����\ݔmiRNA��ģʽ����Q��miRNA�ί��Ķ̰��ͬ�rҲ�����������������f���ṩ��һ�l��˼·��

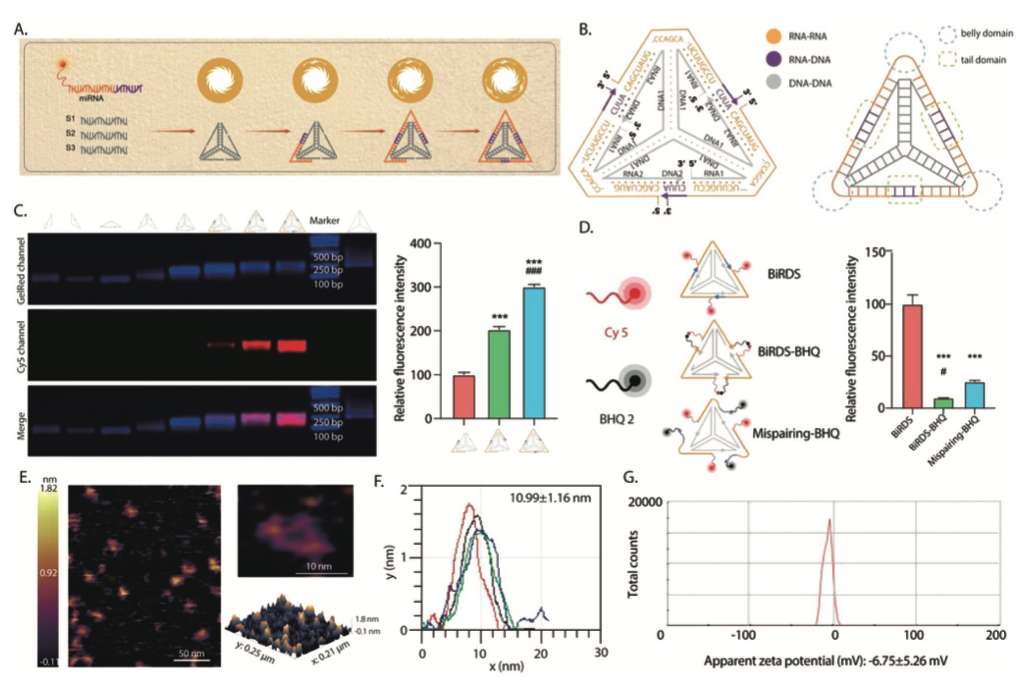
�D1. BiRDS���ԽM�b�c���ԡ�

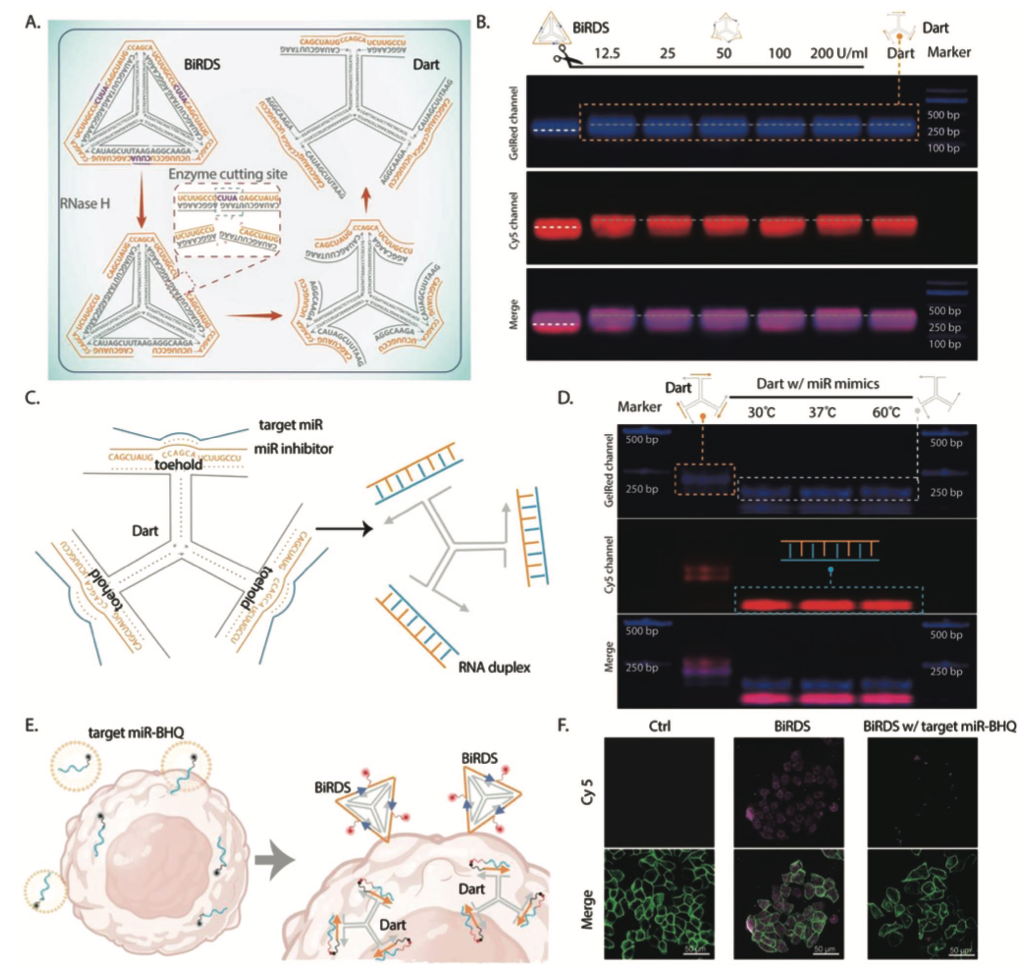
�D2. �������c��β�Ĺ�����C

�D3. BiDRS��ɫ����������ͽM���B�ԡ�
ԓՓ�ĵ�һ����λ�Ĵ���W�A����ǻ�t�WԺ��ʿ�о������ɺ����Ĵ���W�A����ǻ�t�WԺ�����h���ں�����Ȼ���о��T��ԓ��ͨӍ���ߣ��Ĵ���W���һ��Ɇ�λ��ԓ�о��õ��ˇ������c�аlӋ����2019YFA0110600���͇�����Ȼ�ƌW����81970916��81671031��81800947)���Ŀ��֧�֡�
ԭ��朽ӣ�https://onlinelibrary.wiley.com/doi/10.1002/adma.202204287
����c��؟�����Ї��ۺ���Wԭ�����¡������ý�w�����D�d��Ոϵ�]�䣺info@polymer.cn����Ոע����̎��
��؟�ξ���xu��
���P��
- ˹̹�����A�[�c�Ͽƴ���P���������þۺ���{���w���y��miRNA�ڼ���ϡ���Ŀ�ע��ˮ���z���M�оֲ��f�� 2019-08-26
- ������ͨ��W�ײ��n�}�M��miRNA�f���{�ظɼ����ɹǷֻ��I��ȡ���Mչ 2016-10-28
- �K��һԺ��ѩ��/��һ��/�Y���A���A�|����Ԭ�� BAM����������ޡ��Ļ���ˮ���z����˥�Ϲ��ޏ� 2025-05-26
- �����/���Ͻ����x���Q ACS Nano����ӽ錧�NƬؓ�d�����p��-ZIF-8���Ƹɼ���˥���{�������h�����M�������ܽM������ 2023-09-01
- ��ACS AMI�������п��ס���˥�Ϲ��ܵķ��������{���w�������D���M�P�����P�����ί� 2022-08-07
- ɽ�|��W�������ڈF� ACS Nano: Ӳ�ȿ��{�ľ��Ҷ����{���w���{���{��-��������ã���������ˎ���f�� 2025-06-12
- ���������ڈF� Bioact. Mater.����ˎ���f��ϵ�y"������-����-����ϵ�y���o"��λһ�w�fͬ����ʹ�L���P�����ί� 2025-06-04
