�܇��p���������^�ߵĄ������Ɍ��»���֫�w���ع����ϵK���܇������������ޏ�����δ��Q���R���y�}���܇��p���ֲ��l�������������^���װY��ȱѪ���������������ϵ�з���������څ�������L����ȱ���ʹ����������������خa�������������y���ؽ��p������h�������������P��Ҫ���Ԍ��ܞ��d�wͨ�^�ڲ���^���ˎ���ѱ��C���Ǹ��������h������Ч�ֶΣ������w�͓p���̶ȵIJ���º��mˎ���{�ؕr�g���A���Բ����_�����⣬�F���ί�ˎ�﹦�܆�һ��Ѫ-������Ҳ�Ƽs��ˎ������Ч�zȡ����ˣ����ᘌ������h���M�в����Ч�oˎ�����F�h���ӑB�{�����ؽ��������h�����P�I��


��������PNI�ޏ͵�ROS푑�H2S������ʾ��D

��ע�����m��H2S���ϵ�y�Ŀ�ע���ԡ����������ã��Ҿ����^�ߵĻ�����푑��`���ȣ�������ļ��������PCL���Hˮ�Ժͽ������ܣ����܇����ޏ��ṩ�˻��w���ϡ�


��������_�����M��GO��KEGG���������l�F��H2S̎��������NF-��B��TNF��IL-17��̖ͨ·�������}��̖ͨ·��cAMP��̖ͨ·���Ķ��p���װY���w�S��������������̖��
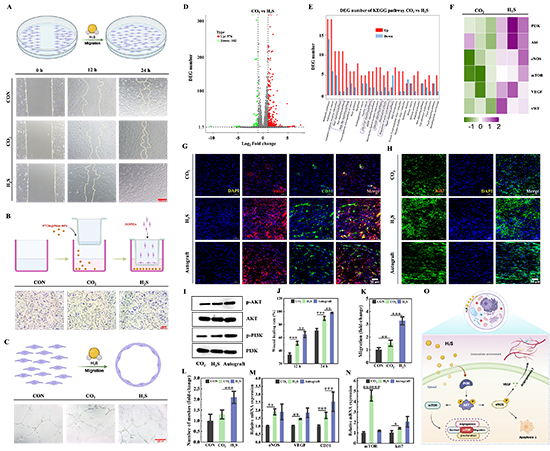

H2S���M�����ܻ֏͡�

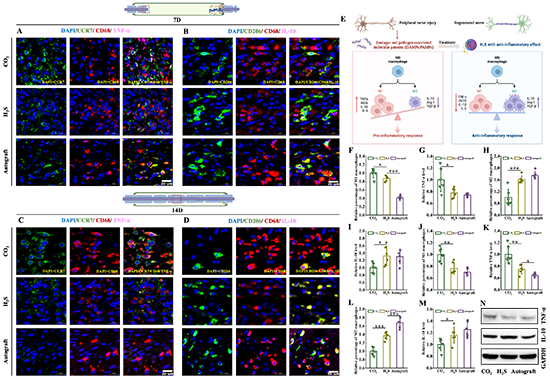
H2S���M�������C�ƣ����m�����H2S��������Ч�҄ӑB�{���˲��λ���װY������������ȱѪ�����������������}�����o���ܓp��������ֲ���������h�����ܡ����⣬��ע��ˮ���z�γ������S��Y��������������𤸽����ֳ���w���Լ��������������γɣ��S��H2S���M����Ѫ�ܘO�����Ķ������Sͻ���L��SCs���w���ṩ��·�����������������ܻ֏͡�
ԭ��朽ӣ�https://www.science.org/doi/10.1126/sciadv.adi1078
- ���u��W�ڱ�/���ƈFꠣ�������푑��;ۺ���ǰˎ���z���f�ͼ��������{�������ڻ������� 2023-10-09
- ���T��W����·�n�}�M��Adv. Sci.�����Խ���{�����zͨ�^ˎ�������ò��������[���h�������¼���CD8? T���� 2023-05-11
- ����وFꠡ�Ӌ���Fꠡ�Adv. Funct. Mater.�������������m��Ϳ�Ӿ����{���װY�������FѪ���٪Mխ���� 2023-05-01
- ���ϴ�W��ӡ���� Angew���ξ��w���Ȳ��^�Y���Ŀ��g�{�� 2025-05-05
- �|�A��W�����ΈF� Macromolecules��ܛ�{���������w��׃��ʾ���p�Y��ԭ���͘O�� 2025-04-17
- �㽭��W����Fꠡ�Adv. Sci.��������ʽ�{�������T�������~�������ڸ�Ⱦ�Է����ί� 2025-02-27
- �V�|ʡ�ƌWԺ������/�V�ݼt���tԺ���h���ַf MTB���h���{�ؿ�ע��ˮ���z���ж�-��ͻ����ȱ�p�ޏ��I������� 2025-05-17
