���ڣ�����W(xu��)/��(f��)����W(xu��)�����½��ڡ��Ϻ���ͨ��W(xu��)�������ں�����W(xu��)Ҧ�ظ�����������DNA�����x���[���ί�����ȡ�����Mչ���l(f��)չ��Ó�����Ǻ��ᣨDNA��/���D(zhu��n)�Q�{���w����UCNP����(f��)���(g��u)���²��ԣ����F(xi��n)�˻���CRISPR-Cas9ϵ�y(t��ng)������ί�ԇ���Ŀɿع��f�ͣ��_���˅f(xi��)ͬ������ί���Ч�������P(gu��n)�ɹ��l(f��)���ڇ��H��(qu��n)���ڿ�Advanced Materials�����M���ϣ�����Ҫ���߰�����ʿ���μ{�����Tʿ������������С����ʿ���о��õ�������Ȼ�ƌW(xu��)�����Y��֧�֡�
������ί���һ�N�������Ե��[���ί���������ه�ڹ���PS���Ĺ��T��(d��o)����M���a(ch��n)����������ROS�������F(xi��n)���[�������������p�������y(t��ng)�Ĺ�����ί����R������(zh��n)��������������㡢�[���M���h(hu��n)�������Լ��[�����������������{(di��o)��(ji��)�ȣ������������ί�Ч����ᘌ��@Щ����(zh��n)���о��F����������DNA���Ϙ�(g��u)������ϵ�y(t��ng)������ί�ԇ�����f���d�w���²��ԣ�����DNA���σ�(y��u)�������пɾ����Ժͷ����R�e�������_�l(f��)����DNA�{��(f��)������Ϙ�(g��u)���^���У�����UCNP��Ԫ��ʹ�øߴ������Ľ��t��⼤�l(f��)������^�̣������ȸ��FѪ�t�أ�Hemin����Ԫ�������[���������������CRISPR-Cas9��Ԫ��Cas9 RNP�������{(di��o)���������Ӻ�����E2���P(gu��n)����2��Nrf2���������[�������������{(di��o)��(ji��)�������f(xi��)ͬ����������ί�Ч����
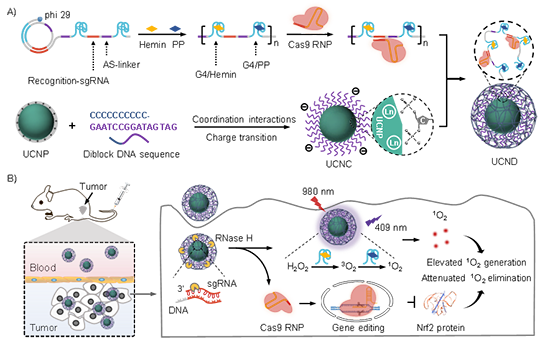
�D1. DNA�{��(f��)�������ڻ���ϵ�y(t��ng)������ί�ԇ���ɿع��f�͡�
ԭ��朽ӣ�https://doi.org/10.1002/adma.202309534
- ����W(xu��)/������W(xu��) Sci. Adv.�����ڹ����������ĸ�����DNA��(sh��)��(j��)�惦�S�C�L�����g(sh��) 2025-06-21
- ����ճ�؈F� Adv. Mater.��ģ��DNA��(g��u)��(n��i)�������F(xi��n)��ϩ�N�������ܡ��M���� 2025-06-18
- �������̴�W(xu��)���������ڈF� AFMs���߂���`���ȵķ�DNA�p�����ް������w�S���W(xu��)�������������w�\�ӱO(ji��n)�y 2025-05-19
- ���ݴ�W(xu��)�����ƽ��ڈFꠡ�Acta Biomater.����ˎ����;ۺ���{���z�������[���LЧ�ί����о��ɹ� 2025-07-08
- ��ɽ��W(xu��)�Ƕ�ؔ/�S�ſ�/������/���x�F� Adv. Mater.�������L�v���ԵĿ�ע����̿�{��øˮ���z���F(xi��n)�[���ąf(xi��)ͬ�ί� 2025-07-04
- ���д����ڣ��w�� / �Ʊ��҈F� ACS Nano �����AIE�{���R�_ͻ���[������ - ���F(xi��n)���ʹ��\�� 2025-05-29
- ����������W(xu��)�����x���ڈF� Adv. Mater.��������ˮ���z���F(xi��n)3D��ӡ�w��(n��i)���� 2024-01-16
�\���P(gu��n)ע�߷��ӿƼ�

- ��ӿƴ����|��/�������F�...
- �A������������� Angew: ...
- �Ĵ���W(xu��)������ AFM������ʯ...
- ��۳��д�W(xu��)�����n�}�M CEJ...
- �Ї��ƴ����d���n�}�M���邐...
- �A��������W(xu��)���V�ա����ݴ�...
- �A�ώ����� Small���w�S��...
- �K���־�h/�������K��һ...
- ���������W(xu��)�����¡��S�؈F...
- �㽭��W(xu��)�߳����ڈF� ��Nat...
- ���д����ڣ��Ʊ��ҡ�����...