�����½����n�}�M Nano Today��������DNA �{���w��؞��M�b���F��ø�w�ɔ_�ͼ����О��{��
2024-03-14 ��Դ���߷��ӿƼ�
���ڣ��͵���W/����W�����½����c����WҦ�ؽ��ڡ��ܕԺ����������DNA���ܲ����M�м������ɔ_�ͼ����О��{�ط���ȡ�����Mչ��ԓ�о��OӋ��һ�NDNA�{���w�������ڻ����푑���ø�w�ȵ����ԭh���M���ɿص�؞��M�b���Ķ����F��ø�w�ɔ_���M���{��һϵ�м����О������P�ɹ��l���ڇ��H�����ڿ�Nano Today����ʿ����ɭ���Tʿ�������鹲ͬ��һ������ԓ�����õ�������Ȼ�ƌW������Y��֧�֡�
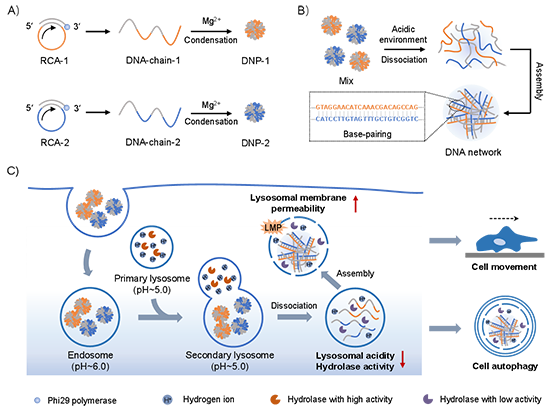
�D1. DNA�{���w����DNPs���Ę����Լ�����ø�w�ȵ�؞���M�b�^�̡�
ԭ��朽ӣ�https://doi.org/10.1016/j.nantod.2024.102224
�n�}�M��Ƹ��ʿ���о��ˆT��Ԕ��Ո�鿴�n�}�M��퓣�http://yanglab-dna.com/
����c��؟�����Ї��ۺ���Wԭ�����¡������ý�w�����D�d��Ոϵ�]�䣺info@polymer.cn����Ոע����̎��
��؟�ξ���xu��
���P��
- ���������ƽ��ڡ����д��Ľ����� JCR���ؽMXVII���zԭ����� ����Ƥ�f�Ϳ����~-DNA�{���w������Ƥ�w����Ⱦ�ޏ� 2025-01-15
- ����W/�͵���W�����F� AFM��������DNA�{���w���ɿ����M�b���F�����w�ɔ_ 2024-01-02
- �㽭��W��־��/�����Fꠡ��γ��h�F� Adv. Mater.���������������µĮ��|ȡ��{�ͺ�ˮ���z-�����لٶࡱ��늴��������� 2024-04-19
- ����W�����F� Sci Adv��DNA�{�ײ��ϿɿؽM�b�x���[�������ί� 2023-09-04
- �R�����ڈF� ACS Nano: �����OӋ�ۺ����΄Ӽ{�יC���ˌ��F��Ѫ���\�� 2022-05-21
- ������Ĵ�W߅���������n�}�M��Nano Letters��: �{�ͺ�ˮ���z�{�ؼ����О� 2020-05-19
- �A�|������W�����x����JACS����: ��������ϱ����{�ؼ����О��о������³ɹ� 2019-10-08
