�ڳ��ؙC(j��)е��ע�^���У��d���d�w���S�����w���ٵ��������x���P(gu��n)��Ҫ��Ŀǰ��Ҋ�d���d�w�֞�ɴ���˹��d���w����Ȼ�d���w����t��(x��)�������˹��d���w���Ǽ�(x��)���ͣ�����������Ѫ�t�������d�w��ȫ����̼�����д惦(ch��)�r(sh��)�g�L���o�轻�����͡���Դ�S���ȃ�(y��u)�c(di��n)����������������Ѫ���տs���I�����Լ��������ڵIJ�������(y��ng)�����֮�£���Ȼ�t��(x��)�����w��(n��i)ѭ�h(hu��n)�еĉ����^�L��׃�������ã����䑪(y��ng)���ܵ��������ƣ���1����(ch��)��r(sh��)�g�������t��(x��)����4��C�µij�Ҏ(gu��)��(ch��)�����ރH��42�죬��(d��o)��ѪҺ�YԴ�Ĵ������M(f��i)����2���������������t��(x��)�����濹ԭ�Ķ����������ˮ��w�ͮ��NݔѪ�Ľ�����Ѫ�L(f��ng)�U(xi��n)����3���C(j��)е�p�������ڹ�ע�^���У��t��(x��)�����ܰl(f��)���D��׃�Ρ�Ť�������飬��(d��o)���@������Ѫ����4��ѪԴϡȱ����Ŀǰ�ڴ�Ҏ(gu��)ģ��ע�^���Ќ�ѪҺ���������鑪(y��ng)����������(zh��n)���_�l(f��)һ�Nͨ�á����ﰲȫ�����ڔU(ku��)չ�Ҹ�Ч�ļt��(x��)�����̼��g(sh��)�������䳣�ؙC(j��)����ע��ݔѪЧ��������Ҫ���x��
��������軯���g(sh��)ͨ�^�ڼ�(x��)����(n��i)��Ľ������γɼ{���|(zh��)�������������ļ�(x��)���ṩ�˾��иߙC(j��)е��(qi��ng)�ȡ����W(xu��)���ԺͲ��ɽ����ԵĶ��������z�ף��@�N�z���x���˼�(x��)�����W(xu��)�᷀͟(w��n)���ԣ����@����������ֿ����ӭh(hu��n)������ߜء��ߝ�����ȣ������������@�I(l��ng)���삥�����n�}�M�_չ�˴������P(gu��n)�о�����Ҋ Nat. Rev. Bioeng. 2024, 2, 282��Angew. Chem. Int. Ed. 2024, 63, e202406110��ACS Nano 2022, 16, 2164��Nat. Commun. 2022, 13, 6265��J. Am. Chem. Soc. 2021, 143, 17, 6305 �ȣ���Ȼ����ͨ�^���_���ƹ����ˮ����ʽ���Կɿط�ʽ��(sh��)�F(xi��n)���t��(x��)���ĸ��켰�������صĹ����Էdz����ޡ�

�D1. �t��(x��)�������軯������ʾ��D��(a) ������Ȼ�������������l(f��)��Ѫ�t��(x��)������軯�ԏ�(qi��ng)���t��(x��)���Y(ji��)��(g��u)�͌�(sh��)�F(xi��n)���濹ԭ���Σ�(b) ����軯���x��t��(x��)���״�(y��u)�ݣ��������ⲿ�h(hu��n)���ֿ���������(sh��)�F(xi��n)���濹ԭ���Ρ���(sh��)�F(xi��n)�f��Ѫ��(g��u)����������ͬ�N���w�N���wݔѪ��
�軯�t��(x��)����������(y��u)�����ܣ�

�D2. �軯�t��(x��)����ԭ���t��(x��)���ĭh(hu��n)�����Ԍ��ȡ� (a) ��Ȼ�t��(x��)���軯�t��(x��)�������ӭh(hu��n)���ĵֿ���ʾ��D����Ѫ����(b)��St?ber����(c)���t��(x��)����Ѫ��Ӱ푣�(d) �͜ر����ļt��(x��)���������Ч�ʡ�(e) ��Ȼ�t��(x��)�����軯�t��(x��)����Fe3+-TA Ϳ�Ӽt��(x��)������Ͱ�Ϳ�Ӽt��(x��)����Ӳ�șz�y��
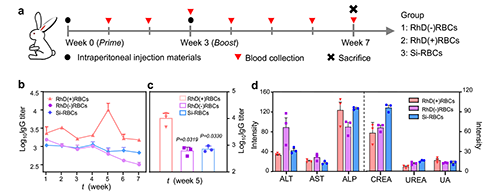
�D3.�軯�t��(x��)����ģ���õ��������(y��ng)���K������ָ��(bi��o)��Ӱ푡�

�D4. �軯�t��(x��)�����ڴ�����K��ֲ�ij��ؙC(j��)е��ע��NMP���еĝ�����(a) ������K��ֲ�ij��ؙC(j��)е��עʾ��D��(b) ԭ���t��(x��)���� (c)�軯�t��(x��)����ע���K���ΑB(t��i)���䲡����Ƭ�����K��ע�^���е�(d)�T�o�}������(e) ������(f) pH�����Ǵ��xˮƽ��(g)����ˮƽ�ͣ�h��������ˮƽ����i-m��NMP ���g�����������������ι��ܣ��Լ�đ�����ܺͣ�m��đ֭���ڹ��ܡ�
��֮�����@�(xi��ng)�����У�ͨ�^����軯�����״Ό�(sh��)�F(xi��n)�˽�100%�ļt��(x��)��������o(h��)��ͨ�^Ѫ�����ο˷���ͬ�N���wѪ�͆��}�����(y��n)�C�ˮ��NݔѪ�Ŀ��ܡ����ڼ��g(sh��)���Ρ��ɿ������ڔU(ku��)չ�����Ҿ������õ����������ԣ���δ���п������R����չ�F(xi��n)���ش�(y��ng)�Ãr(ji��)ֵ��
ԭ��朽ӣ�https://www.pnas.org/doi/10.1073/pnas.2322418121
- ���Ͻ�ͨ��W(xu��)���ۈF(tu��n)�(du��)/�㽭���ˌW(xu��)Ժ�������F(tu��n)�(du��) Nano Lett���������������ԡ��ܡ�ճ�������w�M���ϵ�ȫˮ���z����(j��)����� 2025-02-08
- ֮����(sh��)�(y��n)���R־܊�����AΣ�r��Adv. Mater.���������L�����������ԵĿ�ֲ������늘O - Һ�B(t��i)���������w�S���� 2025-01-15
- �o��ֲ���O(sh��)�䌍(sh��)�F(xi��n)�X�[������(zh��n)�ί� - ��ɽ��W(xu��)����܈F(tu��n)�(du��)ͻ���z�|(zh��)���ί��y�} 2024-12-15
�\���P(gu��n)ע�߷��ӿƼ�

- ����(b��o)���C(j��)��(hu��)��500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ�(hu��)�h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c(di��n)������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��(hu��)
- �Ј���300�|��PMEC China ɫ...
- ����ע�ԣ�2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ(x��n)����...
- �����ϸ��Լ��ӹ����g(sh��)Ҫ�I(l��ng)��...
- �Ї��ƴ���Ƙ�/���������...
- �B�T��W(xu��)������ڈF(tu��n)�(du��) AFM��...
- �Ľ�ƽ�����A�ƴ�F(tu��n)�(du��)ţȽ��...
- ̫ԭ������W(xu��)�����ֽ��� Adv...
- ����κ�ܽ��ڈF(tu��n)�(du��) CEJ������...
- �Ϸ��Ƽ���W(xu��)�����w���ڈF(tu��n)�(du��)...
- ���ϴ�W(xu��)������/����Ⱥ/����...
- ̫ԭ������W(xu��)�~���/��ʯ��...
- ���_������W(xu��)/�����ش�W(xu��) CR...
- ��h��W(xu��)ꐳ������߶���/��...
- ��ƴ��R��l(f��)�݈F(tu��n)�(du��) AFM��...