�����wDNA��mtDNA�������Դ�Լ��ӄ�������ȱ���S���ĽM���ױ��o�������ڑ������ܓp���Ķ�����mtDNAƬ��ͨ�^��N;�����Mһ��ጷŵ��[���h(hu��n)����TME���У��ɞ鼤��h(hu��n)�����B��-���պϳ�ø��cGAS-STING��ͨ·���P�I�|�l(f��)���ء���ˣ��о��O��ͨ�^�ί��ֶμӄ�mtDNA�p�������M�[����Դ��mtDNAጷŵ�TME�н錧cGAS-STING��̖��ه�������
�����������PDT���������ض����L�Ĺ⼤�l(f��)�����F����S�w�Ԯa�������Ļ�������ROS����ͨ�^��ͬ������w������F�����ڃ��H�Ծ��Ҷ����������Ծ��_���ھ����w�Ȍ��FmtDNA�p����ͬ�r�Mһ����૽Y�����뾀���w������F��������IJ��ϣ����ϘO�������Ե�DNA��g��(ICLs)���Թ�ͬ�ӄ�mtDNA�p����ԓ�Y���ɴ_����ֱ������w����PDT�a����ROSԭλ��������Զ��ʻ��Y�����M���cmtDNA���ٸ�Ч�ذl(f��)�����W����ͬ�r���n�}�M��ǰ�ڻ���TME푑����i�x�ӣ�Mn2+��-��Ӽ{�ײ��ϵĹ��������C����������f��Mn2+�ɏ�Ч�@�������p�DNA��dsDNA���ccGAS�ĽY�ϻ��ԣ�����cGAS-STING��̖ͨ·����ˣ�����ӽY������������ܻ��F��ľۺ�����������Mn2+��mtDNAƬ�Σ�ͨ�^��TME�Џ�Ч����cGAS-STINGͨ·������TME���������[�����߷�����
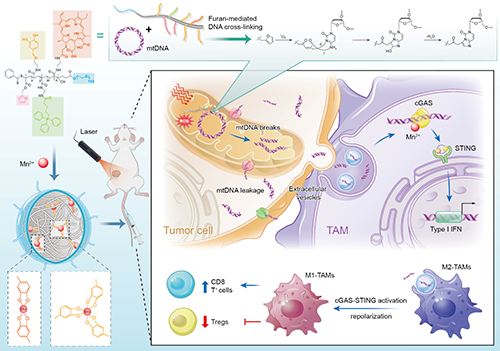
�D1. ���ٶ�Ӽ{�ײ��ϵĽM�ɣ�ͨ�^���T���������p���cDNA���p���ąf(xi��)ͬЧ�������M�����mtDNAƬ�Ώľ����w��ጷţ���cGAS-STING��ه�ķ�ʽ���MM2�;��ɼ�����M1�͵ĘO�������ӿ��[�����߷�����
ԭ��朽ӣ�https://onlinelibrary.wiley.com/doi/10.1002/anie.202411498
- �������WGilles S��be���A�ώ����� Carbohydrate Polymers��Ƥ������Һ����SI-ATRP�Ƃ���H���w�S�ؼ{�� 2025-05-19
- �|�A��W������/�����F� Angew: ��-���{���H�Ծ��x��Һ�w�����\��늳� 2025-03-18
- �͵�־��/�Sϼ�| Soft Matter�����ڃ��H�Ծ�늽��|��Janus̫��ܺ�ˮ�������� 2025-02-26
- ���������i���Z�c�r Sci. Bull.����Ӿۺ��:��ĤͿ�ӡ��������[�����F���x���f�������ί� 2024-02-18
- ���T��W����·�n�}�M��Adv. Sci.�����Խ���{�����zͨ�^ˎ�������ò��������[���h(hu��n)�������¼���CD8? T���� 2023-05-11
- ���������ѡ������T��W����·�F��аl(f��)�����ͷů�ˎ�� 2023-03-20
- ���д����ڣ��w�� / �Ʊ��҈F� ACS Nano �����AIE�{���R�_ͻ���[������ - ���F���ʹ��\�� 2025-05-29
