�S���˿����g���ļӄ����Ӿ�˥�ϳɞ鼱���Q���ش��}���Gͪ��ȱ��������������Ⱥ�w��Խ��Խ��Ҋ���Gͪ�������Ԃ��w����Ҫ���Լ��أ��Gͪȱ����Ӱ푲G�蹦�ܣ����Ұ��S���Թ����ϵK��֬���ѷe�� ���|���ɡ�����ή�s���J֪�ϵK�Ȳ��l�Y���Mһ���ӄ�ȫ��˥�ϡ�Ŀǰ���R���ί��ֶ��Ծ�������Դ�ԵIJGͪ�a�䣬�@�N�������S�ั���ã���t�������࣬�ι����ܓp��ǰ�������������ؕ��Ɖ������X-���w-���ٵ� (HPG) �S���{�������²G�辫�Ӱl���̓ȷ��ڹ��ܜp�ˡ����ؽ������һ�N����ȫ����Ч���ҳ־õ��ί���ʽ�������ί��Gͪȱ���Y���������������|�����Ҹ��С�
����, �A��������W���ϿƌW�c���̌WԺʩѩ�������F��ڇ��H�ڿ�Advance Science�l���� Reconstructing the Stem Leydig Cell Niche via the Testicular Extracellular Matrix for the Treatment of Testicular Leydig Cell Dysfunction ��������Փ�����@헹����аl��һ�N�����ԡ������ԺͿ�ע���ԵIJG��Ó��������|ˮ���z (TdEC)���ϲG���g�|�ɼ��� (SLC) �ί��Gͪȱ���C������SLC���g�|���� (LC) ǰ�w������������ֳ�ֻ���LC���a���Gͪ���о��l�F˥�ϵIJG���g�|�h��������SLC����ֳ�ͷֻ���LC�������½���Ó��������|���ǽY��֧�ֵ����W֧�ܣ����Ǽ������L����̖�����Ĺ��ܻ��|����һ�N�߂����õ��������ݵIJ��ϡ�ԓ�������F��ĽM��Ó������������ᘌ��G��M�����خ��ԃ������ɹ��Ƃ��˲G��M��TdECM����Ó����ǰ��ĽM���WȾɫ��Elisa�z�y�C����������Ч�����ͬ�r�����˼�������|�Ļ��Y����SEM������ˮ���z���zԭ�w�S�ı��^��ò�����M�W�����Mһ�������˲G��Ó��������|����Ҫ�ɷֽM�ɺ����P����̖���_���w��ļ��������ߟɹ⡢qPCR��RNA�D䛽M�y���C��TdECM�܉���Ч���MSLC��ֳ�ͷֻ���LC���Ķ��@�������Gͪ�ķ���ˮƽ��
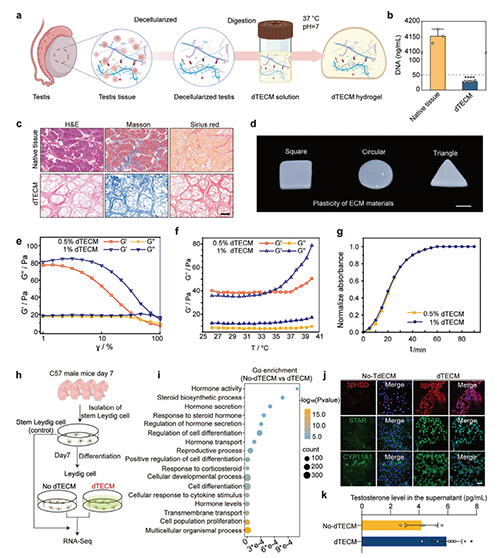
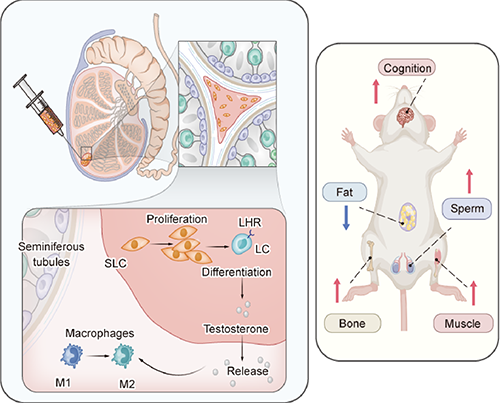
���о�ᘌ����ԲGͪȱ���Y���_�l��TdECM-SLC�ĽM�������ί��wϵ��ͨ�^ԭλע��TdECM-SLC���@�������˲Gͪȱ���Y���w��Ѫ��Gͪˮƽ���Ķ������˲Gͪȱ����ȫ���Y��@�Nԭλע�会������|�����ɼ������ί��ֶξ߂�Ч���@�������m�r�g�L�����Ɖ�HPG�S���{���C�Ƶȃ��ݣ����R���IJGͪȱ���Y���ί��ṩ��һ�Nǰհ�Եķ�����������Ҫ���о��rֵ�͏V韵đ���ǰ����
ԭ��朽ӣ�https://onlinelibrary.wiley.com/doi/10.1002/advs.202410808
- ���o���P��
