��ˣ���I(y��)��W(xu��)���x���ڈF(tu��n)�����Ȼ����֬�����¹���������c����(g��u)��֬�|(zh��)���ӎ죬��12�N֬�|(zh��)�кY�x��S12���¹���������������F(xi��n)�x���Ԛ���Fn����Ӱ����������������Cb����S12�܉��Ɖ�Fn��(x��)��Ĥ��֬�ӣ���Ĥ+��(n��i)Ĥ����ͨ�ԣ����l(f��)Ĥȥ�O����DiSC3-5�z�y���̓�(n��i)����й©��PIȾɫ��������Cb�ĺ��ľ��DZڟo�p����SEM/CLSM��C����S12�ԽM�b�γɼ{��֬�|(zh��)�⚤��ʹCb��ģ�Mθ����ģ�M�cҺ��С���w��(n��i)�c�������о����^�õ��f��Ч����
��Fn����DSS�T��(d��o)�ĽY(ji��)�c��ģ���У�Cb@S12�ί��MС��ĽY(ji��)�c�L��څ���ڽ����MС�����͌��սMС�����@���ԅ^(q��)�e��Cb@S12�ί��M�܉����Cb�Ķ�ֳ���Լ�����ڵĶ����}���ӣ����x���Ԛ���Fn���Ͳ�ԭ�w�ĺ������S�����c����Ⱥ�Ķ����ԣ��M(j��n)����ʹ�װY����TNF-����IL-6��IFN-��ˮƽ�½������M(j��n)�c���Ĥ���ޏ�(f��)�����⣬��Fn��Ⱦ��CRCԭλģ���У�Cb@S12�ί��Mͬ�����Cb�Ķ�ֳ�Ͷ����}���ӣ����x���Ԛ���Fn���S�����c����Ⱥ�����M(j��n)һ��������[����(n��i)CD8+ T��(x��)������ˮƽ��M1�;��ɼ�(x��)��ռ��������IFN-��ˮƽ���ߣ��γɿ��[�������h(hu��n)�����Ķ����ˌ��[�����ί�Ч����ͨ�^IVIS������Կ�����Cb@S12�ί��MС����[�����@�pС��

�D1. ���о�ʾ��D��A) ���¹��ᣨLA������������֬�|(zh��)���кY�x�����ߺ���U����Fn�������x���Կ������ԣ�ͬ�r�����������������Cb���o����֬�|(zh��)��B)�ڷ��f�ͽ�(j��ng)�Y�x��S12������������Cb��Cb@S12���������ί�С����Fn���P(gu��n)���c��������Cb@S12ͨ�^����(qi��ng)Cb��θ�c����(w��n)���Ժ��c��������������Ч��Cb�f�����c����׃��λ������S12���w�x���Ԛ��粡ԭ��Fn�����p��Cb�Ļ��ԡ����w���f��ͨ�^����;���֏�(f��)Fn���ص�DSS�T��(d��o)���ԽY(ji��)�c��С���װY���Ӝp�١��Y(ji��)�c��Ƥ�����ޏ�(f��)�Լ��c�����ﷀ(w��n)�B(t��i)�S�֡����⣬Fn��Ⱦ�ĽY(ji��)ֱ�c��ԭλ�[��С��ͨ�^�c����Ⱥ����(zh��n)�{(di��o)�غͼ��l(f��)���[�����߷���(y��ng)�����F(xi��n)��CD4+ T��(x��)����CD8+ T��(x��)����M1�;��ɼ�(x��)�����ӣ����F(xi��n)���[�������L���ơ�

�D2. ᘌ�Fn�x���Կ���֬�|(zh��)�ĺY�x���C(j��)��̽����A)֬�|(zh��)S8-S16�ķ���ʽ��ͨ�^��12�N���W(xu��)�Y(ji��)��(g��u)���ӵ�֬�|(zh��)���кY�x���l(f��)�F(xi��n)�¹�����������S12��Fn�����خ��Կ������ԡ�B, C) ֬�|(zh��)S8-S16��Fn��B����Cb��C��������־���ȣ�MIC������͚�����ȣ�MBC���б����Y(ji��)���@ʾ��S12��Fn��MIC��10 ��g/mL��MBC��25 ��g/mL������Cb�o���@�������á�D-G)������R��SEM�����۽��@�R��CLSM���^�켚(x��)���ΑB(t��i)�� H-J)S12����(x��)��Ĥ�����Ե��u����n=3����H)���|(zh��)Ĥȥ�O����Fn��(j��ng)S12̎����DiSC3-5�ɹ���̖�@������(qi��ng)��Ĥȥ�O������Cb�o׃����I) ���|(zh��)Ĥͨ�ԣ�Fn��(j��ng)S12̎����PI�ɹ���̖�@�����ӣ�Ĥ���ף���Cb�o׃����J) ��Ĥͨ�ԣ�S12��MIC����¿��Ɖ�Fn��Ĥ��NPN̽ᘙz�y����K) S12�x���Կ����C(j��)��ʾ��D��S12ͨ�^����Fn�^���ĸ��m�������Ĥ�̓�(n��i)Ĥ��֬�ӣ����l(f��)Ĥȥ�O������(n��i)����й©�������p������Cb����m����Ժ��ľ��DZڵı��o(h��)������S12�Ɖġ�

�D3. Cb@S12���䷽�O(sh��)Ӌ��θ�c����(w��n)�����c��������(qi��ng)�C(j��)����A)ͨ�^��������ԽM�b���Ԙ�(g��u)��Cb@S12��S12֬�|(zh��)ͨ�^�o������c����������Y(ji��)�ϣ��γɼ{�ױ��o(h��)�ӡ�B)Cb@S12�p�ع��ܣ��ֿ�θ�c�����ӭh(hu��n)�����x���Ԛ���Fn��C)�y��Cb��Cb@S12�������ֲ��cZeta�λ��D)��ʽ��(x��)���g(sh��)����FITC��(bi��o)ӛ��Cb��δ��(bi��o)ӛCb���錦�ա�E-F)����R��TEM���c������R��SEM���^��Cb@S12���^��ò��TEM�@ʾS12��Cb�����γɾ���{��Ϳ����SEM�@ʾCb@S12����⻬���ܡ�G) ���L�����@ʾCb@S12��BHI���B(y��ng)����37�����B(y��ng)�r��OD 600ֵ������S12�Ě��w��Ӱ���������ֳ���ԡ�H-I) ģ�MθҺ��SGF�������Ԝyԇ��SEM�@ʾCb@S12��SGF�з���0.5С�r���Ա��������Y(ji��)��(g��u)��J-K) ģ�M�cҺ��SIF�������Ԝyԇ��SEM�@ʾCb@S12��SIF�з���1С�r��4С�r����(x��)���Y(ji��)��(g��u)��(w��n)����L)ģ�Mθ�c��������Cb�cCb@S12�Ļ��Ϳ��ƽ����C��M)IVIS�z�y�ɹ��(bi��o)ӛ��Cb@S12С���c���������ڷ���ͬ��(sh��)����1×10? CFU����Cb��Cb@S12��Cb@S12��С���c����(n��i)�Ĝ���Ч��������n=3����

�D4. Cb@S12��Fn������DSS�T��(d��o)���ԽY(ji��)�c��С����ί�������A) С��ģ��ʾ��D��B) �ί����gС���w��׃����C) ��ͬ�ί��M�Y(ji��)�c�M��������Ƭ��D) ��ͬ�ί��M�Y(ji��)�c�M���L�ȡ�E-G) �Y(ji��)�c�M����TNF-����E����IFN-����F����IL-6��G��ˮƽ��n=5����H) ��ͬ�ί��M�Y(ji��)�c�M����H&EȾɫ����ɫ���^���ܰͼ�(x��)���������tɫ���^���[�C�p������(bi��o)�ߣ�200 ��m����I) ��ͬ�ί��M�Y(ji��)�c�M�������߽M��Ⱦɫ��J) ���M�Y(ji��)�c�M������W(xu��)�u�֡�K) ��ͬ�ί��M���^������ø��MPO����Լ�(x��)������������
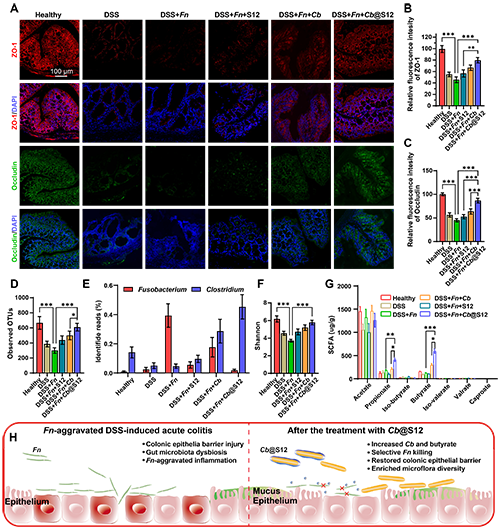
�D5. Cb@S12�����c���װY���ί��C(j��)����A) �Y(ji��)�c�M���оo���B�ӵ���ZO-1��Occludin�����ߟɹ�D��Cb@S12�ί��M�У�ZO-1��Occludin��Ĥ��λ�@���֏�(f��)�������c�������������ޏ�(f��)��B, C) ZO-1 (B)��Occludin(C)�������ɹ⏊(qi��ng)�ȶ���������n=5����D-F)16S rRNA�y������c����Ⱥ��D)�^�쵽��OTUs��(sh��)����Cb@S12�M����������@�������װYģ�ͽM��P < 0.01����E) Fusobacterium��Clostridium���S��F)�c����ȺShannon������ָ��(sh��)��Cb@S12�M�����Ի֏�(f��)������ˮƽ��P < 0.001����G)GC-MS�����S�������֬���ᣨSCFA��������H)�ί��C(j��)��ʾ��D��

�D6. Cb@S12��Fn���P(gu��n)��ԭλCT26�[��С��ģ�͵Ŀ��������u����A) С��CRCԭλ�[��ģ�͌�����̈D��B) ͨ�^H&EȾɫ�u�������٣��ġ��Ρ�Ƣ���Ρ��I���[�����ĽM���W(xu��)׃������C�ί������ﰲȫ�Ժ��[���M���IJ�����B(t��i)��C) IVIS�O(ji��n)�y�[�����L�ӑB(t��i)���@ʾCb@S12�M���[�����Ʒ�����@��Ч����D) �[���M���е�Fn�خ��ԟɹ�ԭλ�s����FISH���c����TUNELȾɫ(li��n)���u�����_�J(r��n)�䌦�²������Ƽ��T��(d��o)�[����(x��)��������Ч����E) ӛ��ί��^���е�С���w��׃����F) ���MС�����������������Cb@S12�M���F(xi��n)�����@�����惞(y��u)�ݡ�G, H) �[����(n��i)T��(x��)���;��ɼ�(x��)������ʽ����I) �[���M���иɔ_������IFN-������ˮƽ���ߣ��f���ֲ����ߑ�(y��ng)������(qi��ng)��J, K) �S�����c����Ⱥ�M�ɷ��������^�˲�ͬ�M��Fusobacterium��Clostridium�������S�ȼ���OTUs��(sh��)������ӳ������Ⱥ������Ч����L) GC-MS�����S�������֬���ᣨSCFA��������
���о��״Θ�(g��u)����һ�N���������������ܼ{��ƽ�_��Cb@S12����ͨ�^������-����-�����������ؙC(j��)�ƣ����F(xi��n)��Fn���P(gu��n)�c�������ĸ�Ч�ί���ԓ���Բ��H�����˿����صďV�V���������ã�߀ͨ�^�������Ĵ��x���������c����Ⱥ���B(t��i)����IBD��CRC��(li��n)���ί��ṩ�˝��ڵ��ί����ԡ��о��C����Cb@S12�ڄ���ģ���а�ȫ��Ч�����Н��ڵ��R���D(zhu��n)���rֵ��
�����о��ɹ�����Oral delivery of Clostridium butyricum using selective antibacterial lipids for enhanced treatment of Fusobacterium nucleatum-associated intestinal diseases�� ���}���l(f��)����Nano Today��2025�� 62�� 102742. DOI��10.1016/j.nantod.2025.102742������I(y��)��W(xu��)���x���ں�����t(y��)�ƴ�W(xu��)�[���t(y��)Ժ�������ʿ��ͨӍ���ߣ���I(y��)��W(xu��)��ʿ�о����wʥ������I(y��)��W(xu��)���ƽ��v���鹲ͬ��һ���ߡ��@헹����õ��˿Ƽ������c�аl(f��)Ӌ����������Ȼ�ƌW(xu��)�����������Ȼ�ƌW(xu��)�������c�Ŀ��֧�֡�
����朽ӣ�https://doi.org/10.1016/j.nantod.2025.102742
- ���ϴ�W(xu��)������/����Ⱥ/���� Adv. Mater.����������ʿ�{(l��n)�{��ܷ�������(qi��ng)�ݶȿ���Ϳ�� 2025-07-01
- �K�������һԺ������Ժ��� IJBM: ��߿����Ϳ��Mխ���ܵ��dˎ�ɽ���ݔ���֧�� 2025-06-29
- ���u��W(xu��)�ڱ����ڈF(tu��n)� Small�����п���ֹѪ�͏V�V�������ԵĹ���ˮ���z���ڼ��ق������� 2025-06-03
- ���Ƽ���W(xu��)犳ɽ��ڈF(tu��n)� Small����ܲ����Q��(x��)���w�S���ڷ��� 2023-08-23
- ���r(n��ng)��וԷf������(f��)��W(xu��)���M(j��n)��/������ AFM�����������ϵ�y(t��ng)ͨ�^�����[�����P(gu��n)���w�S��(x��)�����ҹ⯟���w��(n��i)���[��Ч�� 2024-02-20
- �ӱ������ϳɷ��n�}�M��Nano Lett.�������ڽ��t���푑�(y��ng)��ܗ�ۺ���{�����ӵ������������� 2022-12-27
- ��(f��)����W(xu��)ꐇ��-�����n�}�M��ԭλ��Ó���o(h��)���l(f��)������ò�D(zhu��n)׃���������о���ȡ����Ҫ�M(j��n)չ 2018-06-27
�\���P(gu��n)ע�߷��ӿƼ�

- �������C(j��)����500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ��h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��
- �Ј���300�|��PMEC China ɫ...
- ����ע�ԣ�2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ(x��n)����...
- �����ϸ��Լ��ӹ����g(sh��)Ҫ�I(l��ng)��...
- �Ї��ƴ���Ƙ�/���������...
- �B�T��W(xu��)������ڈF(tu��n)� AFM��...
- �Ľ�ƽ�����A�ƴ�F(tu��n)�ţȽ��...
- ̫ԭ������W(xu��)�����ֽ��� Adv...
- ����κ�ܽ��ڈF(tu��n)� CEJ������...
- �Ϸ��Ƽ���W(xu��)�����w���ڈF(tu��n)�...
- ���ϴ�W(xu��)������/����Ⱥ/����...
- ̫ԭ������W(xu��)�~���/��ʯ��...
- ���_������W(xu��)/�����ش�W(xu��) CR...
- ��h��W(xu��)ꐳ������߶���/��...
- ��ƴ��R��l(f��)�݈F(tu��n)� AFM��...