��(sh��)�w�[���h(hu��n)����TME��ͨ�������������������[�����P(gu��n)���w�S��(x��)����������(d��o)�´����(sh��)�[�����m(x��)̎��������������B(t��i)����ʮ������⯟���[���о��C��(sh��)����������ṩ�ğ�������������/���Ե������ɻ��ɴ��M(j��n)�[�����P(gu��n)��ԭ�ķ��ڣ����M(j��n)��(x��)�������p�������{(di��o)����ԭ�Լ�(x��)�������ͼ�(x��)�����������ˣ��⯟�c�����ί�����Ч�Y(ji��)��������(sh��)�F(xi��n)���[���ί�Ч���ąf(xi��)ͬ�Ŵ�Ȼ����ͨ�^�������Լ��⯟�л��Է��Ӽ��������ϵ�y(t��ng)�Ƿ�ֱ�Ӆ��c�[����(x��)���Ĺ���߀��Ҫ�M(j��n)һ�����C��(j��)�C��(sh��)�����˽�ʾ�⯟�^��������ϵ�y(t��ng)�Ŀ��[�����ã��б�Ҫ��TME���P(gu��n)�ĽǶ�̽ӑ���������ϵ�y(t��ng)�Ƿ�ֱ�Ӆ��c�⯟�Ŀ��[���ί��^�̡�


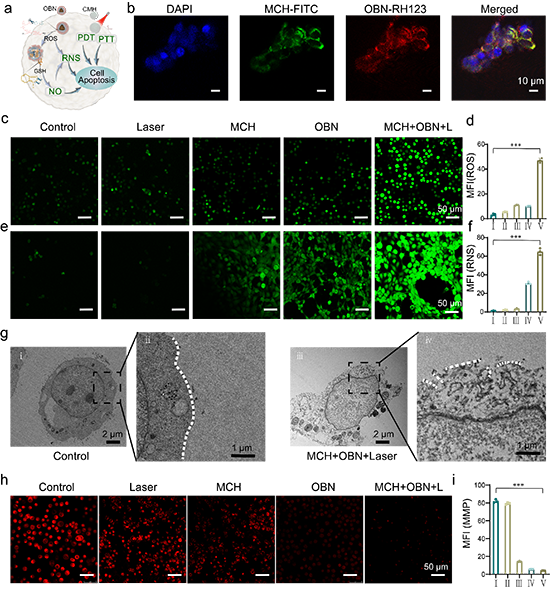
�D1. ��ͬ���ߠ�B(t��i)��MCH-OBN�⯟�{��ƽ�_���[��Ч��ʾ��D��


�D4. MCH-OBN�{��ƽ�_�w�⿹�[��������DCs����


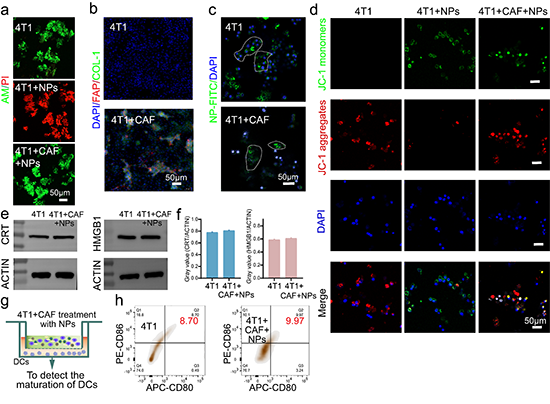
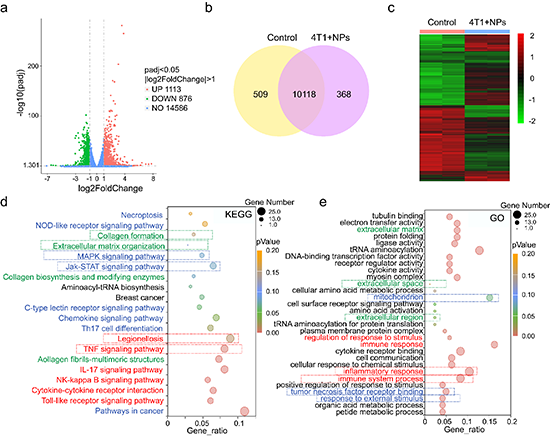

��֮��ԓ�����״��P(gu��n)ע�����ߠ�B(t��i)���⯟���[��Ч���ěQ�������á�MCH-OBN�{��ƽ�_��Ұ���ͺ�����ȱ��С����[����Ч��C��(sh��)�˹⯟���������B(t��i)�ď�(qi��ng)����ه�ԣ��ڴ˻��A(ch��)�ϣ��о����M(j��n)һ���C��(sh��)�˹⯟������ϵ�y(t��ng)ͨ�^�Ɖ�CAFs���[����(x��)�����������ϴ��M(j��n)�[����(x��)�������������{(di��o)�ؙC(j��)�ƣ����R���_�l(f��)��CAFs����c(di��n)�������o���⯟���[�����Ծ�����Ҫ���x��
ԭ��朽ӣ�https://doi.org/10.1002/adfm.202315551
- �칤����x/���ƽ��F(tu��n)�(du��) Nano Today���x���Կ���֬�|(zh��)�f�Ͷ����������(qi��ng)�ߺ���U�����P(gu��n)�c�������ί� 2025-04-10
- �ӱ������ϳɷ��n�}�M��Nano Lett.�������ڽ��t���푑�(y��ng)��ܗ�ۺ���{�����ӵ������������� 2022-12-27
- ��(f��)����W(xu��)ꐇ��-�����n�}�M��ԭλ��Ó���o(h��)���l(f��)������ò�D(zhu��n)׃���������о���ȡ����Ҫ�M(j��n)չ 2018-06-27
- ���д����ڣ��w�� / �Ʊ��҈F(tu��n)�(du��) ACS Nano �����AIE�{���R�_(d��)ͻ���[������ - ��(sh��)�F(xi��n)����(zh��n)���\�� 2025-05-29
- ɽ�|��W(xu��)����ϼ���ڈF(tu��n)�(du��) Nat. Nanotech.���l(f��)�F(xi��n)��QCAR-T��(x��)��������(sh��)�w����Ч������Ч���� 2025-05-20
- ����ꐌW(xu��)˼Ժʿ���O�o���ڈF(tu��n)�(du��) JACS��������o�����Ӿ���(zh��n)�{(di��o)���ܹ��������{���w�Sԭλ�ӑB(t��i)�M�b��(sh��)�F(xi��n)�f(xi��)ͬ�[����Ч�ί� 2025-05-13
�\���P(gu��n)ע�߷��ӿƼ�

- ����(b��o)���C(j��)����500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ��h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c(di��n)������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��
- �Ј���300�|��PMEC China ɫ...
- ����ע�ԣ�2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ(x��n)����...
- �����ϸ��Լ��ӹ����g(sh��)Ҫ�I(l��ng)��...
- �Ї��ƴ���Ƙ�/���������...
- �B�T��W(xu��)������ڈF(tu��n)�(du��) AFM��...
- �Ľ�ƽ�����A�ƴ�F(tu��n)�(du��)ţȽ��...
- ̫ԭ������W(xu��)�����ֽ��� Adv...
- ����κ�ܽ��ڈF(tu��n)�(du��) CEJ������...
- �Ϸ��Ƽ���W(xu��)�����w���ڈF(tu��n)�(du��)...
- ���ϴ�W(xu��)������/����Ⱥ/����...
- ̫ԭ������W(xu��)�~���/��ʯ��...
- ���_������W(xu��)/�����ش�W(xu��) CR...
- ��h��W(xu��)ꐳ������߶���/��...
- ��ƴ��R��l(f��)�݈F(tu��n)�(du��) AFM��...