�������t�W������оƬ��ˎ��Y�x�Ƚ����I���У��������s�Ĉ�����Ѫ�ܾW�j�������g�����Խ��Խ�ߵ����m���ԣ�adaptability����Ҫ���HҪ����߀ԭĿ�˽Y���c�ߴ磬߀����ݶ�N�����wϵ�Ԍ��F�����m�䣬�Դˁ�M�㲻ͬ�đ���Ŀ�ġ�Ŀǰ������ģ�巨��sacrificial templating�����乤ˇ���㡢�m�����V���ɞ阋��ͨ���W�j�ij��ò��ԡ�ԓ����ͨ�^�A�ȴ�ӡ���Ƴ��Ġ������ϣ�sacrificial materials��������Ƕ���������У������Ĺ̻����ܽ�ģ�壬�Ķ��γ�ͨ���Y����Ȼ�����F�Р��������ڌ��H�������ձ��������}��1����ӡ�������д����ƣ��y�Ԙ����༉��֧�Y���������z����2���ܽ�r�װl�����g׃�Σ�����ͨ��������½���Ӱ푳ߴ�߀ԭ����PVA��Pluronic F-127����3�����ϼ����Բ��ѣ�ֻ���x���һ���Hˮ����ˮ�Ի��ģ�����ه�ض��Ĵ�ӡ�wϵ����Ƕ��ʽ��ӡ����
���T��W���������ڈF������ͨ�^���܄���nonsolvent�����ƚ��Iȡ���������������Ͻ������IJ��Խ�Q������������Ƕ���^���н��治�����������m���Ե���ԭ�����治���������»����е��܄��ڹ̻�ǰ���ٝB��ģ��Ȳ���ʹ���ڱ��Ƴ�ǰ���F���ɿص���Û���Hˮ�Ի��ģ���Óˮ׃�Σ���ˮ�Ի��ģ�����K�Ɖ��A�O��ͨ���Y�������܄���ָ���cˮ���ܵ��o���ܽ�������ϵ��ЙCԇ������ǰ���F��������P�о�����������܄����nonsolvent quenching, NSQ������ӡ����(Adv Sci 2022, 2203236)��ͨ�^�T�����ϱ������Ӳ�����ڽ����γ����ܱ��o�ӣ���Ч�����Y������ȡ��ڱ��о��У��F��Mһ���Ɯyԓ�^�̿��Ӳ��ϱ�����I����ָ���ⲿ�܄����D׃�������σȲ����B�����M������������ⲿ���g�ķ������ϣ�������������ģ����Ƕ����ĺ����Û�c׃�������ڴ�������I�ض�����ԣ�Hydrogen Bond Re-Orientation, HyBRO����ͨ�^�����I�����������D��������������F���������Ч���o���D1����
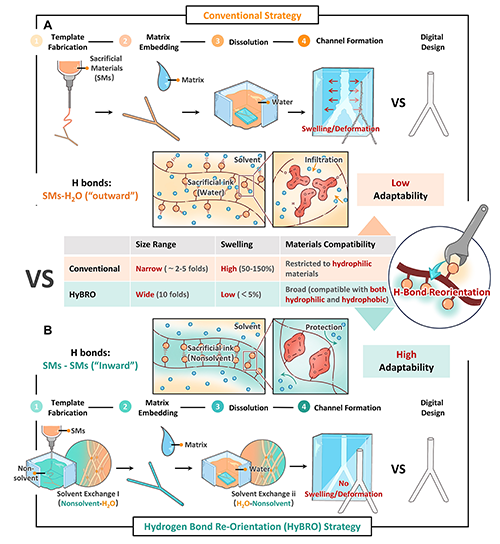
�D1. ���y���� vs HyBRO��ͨ�^���I�����{�أ����F���m���Ե�Ѫ�ܾW�j������ˇ
����CHyBRO���Եķ��әC�ƣ��n�}�M��ģʽ�����ϸʾ�����GM����ģ�ͣ�ϵ�y�о��˷��܄�DMF�ڴ���^���еĚ��I�ض���Ч�������l�F���ڼ�����I�ɔ_�����غ�����x�@�����t���������I��������������P�I��SAXS�Y���@ʾ��NSQ̎������ʹGM�γɸ������������ľۼ��w��ATR-FTIR�����Mһ���_�J������@��������GM��g���I������ͬ�r������GM�c�ⲿ�܄���ˮ��֮�g�Ě��I�γɣ���C�˚��I���������������Ⱦ����Ķ����D׃��
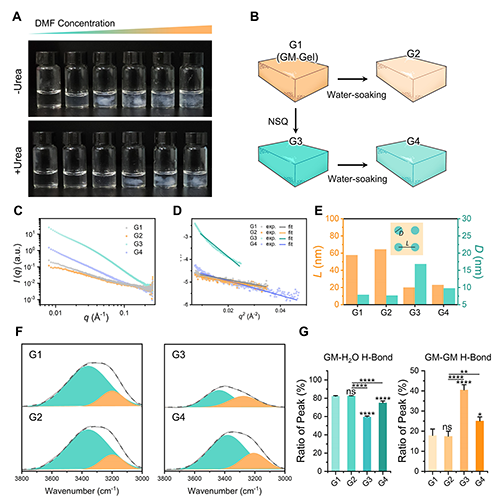
�D2. NSQ���FGM���I�ض���
�����_�@һ�C�ƺF��Mһ����C��HyBRO�����Č��HЧ������������δ��̎���ĉK�����z��ˮ���װl��������Û����Û׃�����^320%������HyBRO̎������Û�������ڼs131%���Y���������@������������Ҫ���ǣ�HyBROģ�����ɵ�ͨ���ߴ��c�OӋֵ�߶�һ�£��`���������10%�ԃȣ���Ч������ͨ���Y���ı�����cһ���ԡ������@һ���ԣ��F������z�ͺ������c�wϵ�гɹ����������ηֲ�ČӼ�Ѫ�ܾW�j��ͨ��ֱ�����w40��400 ��m�����ʌ��F��Ѫ�ܵ�С���}��ʮ���߶ȿ�Խ�����չʾ��HyBRO��ͨ�����ȡ��ߴ�ɿ��Ժ͏��s�Y���٬F����ľC�σ��ݡ�
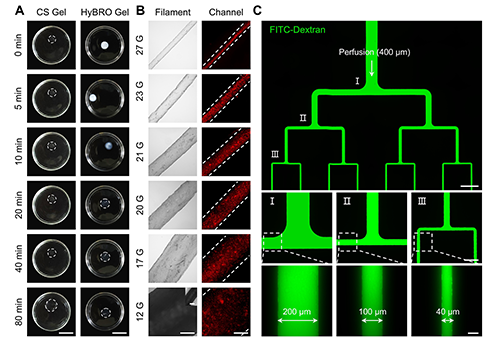
�D3. HyBRO�@��������Û�����F�������ͨ������
�b�ڂ��y�������H��ˮ�����g���x���������n�}�M�Mһ����HyBRO���ԔUչ�����ڶ�N�����Բ��ϣ�����C��V�V�����������Y���@ʾ��HyBRO���ں������c�����z����֬�Ǻ�GelMA�ȳ�Ҋ�Hˮ�������з�������ͨ���Y����ͬ�r�����������ϸʾ��ǡ��ۼ������;�����-�u�����Ṳ�������ˮ�Ի�����ͬ�ӱ��F�����ó������������⣬HyBRO���H�m����GM��������ϣ����ڂ��y��PVAģ��Ҳ���@��������Y������ȣ��Mһ��ӡ�C��ԓ�����ڲ�ͬ����ƽ�_�µ��m���ԡ�
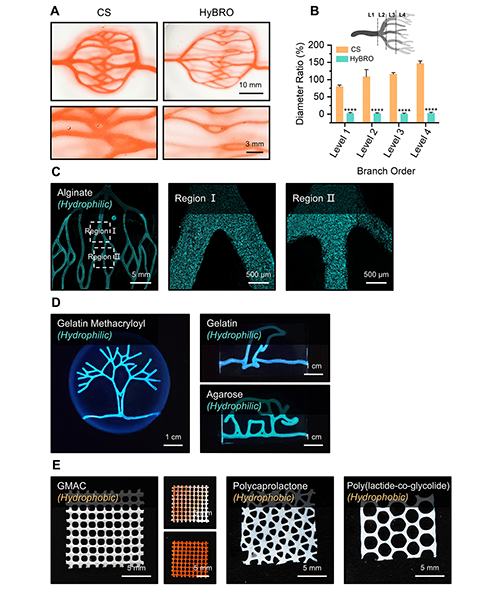
�D4. HyBRO���c��N�H/��ˮ���ļ���
HyBRO�������H���Ѓ�Խ���m������߀��֧�փ�Ƥ�������L���ܱ��_������������Ƥ������ͨ���ȿ����������İ��g�B�ӣ��@���������|�ĝB��չ�F�����͵�Ѫ�����Ϲ��ܡ�����Ҫ���ǣ�ԓͨ��ϵ�y�܉�ģ�M�������Б������T����Ƥ����ͨ�^TRPV4��֪���w�̼��������}��̖ͨ·�����Mһ������ጷţ��ʬF���c�挍Ѫ�����Ƶ����W�����c�����{�����ԡ��@һϵ�нY��������HyBRO���H�Ɍ��F�Y���������ߴ�ɿص�Ѫ�ܾW�j���������߂��ؽ��߹��ܻ���Ѫ��ϵ�y�ĝ�����
���о������HyBRO����ͨ�^�����I�ض��C�ƣ���Ч��Q�˂��y����ģ�巨�ڡ��m���ԡ��ϵ�ƿ�i��ԓ���Բ��H�ɾ��ʘ����߱���ȣ�>90%������߶ȣ�10����Խ��ͨ���W�j��߀�V�����ݶ���Hˮ�c��ˮ���ϣ���֧�փ�Ƥ�����Ĺ��������L��������푑������F�˽Y���c�������ܵąfͬ�ؽ����������t�W���I���Ѫ�ܻ������ṩ��һ��ͨ�ü��ݵ��¼��gƽ�_�����P�ɹ��� ��A Highly Adaptable Hydrogen Bond Re-Orientation (HyBRO) Strategy for Multiscale Vasculature Fabrication�� ���}�l���ڡ�Advanced Materials����Փ�ĵ�һ�����ǰ��T��W��ʿ�����F��ʿ���ε��\��ʿ����Ҳ��ǰ���OӋ���܄�����ӡ���g��Փ�ĵĵ�һ���ߡ��о��@�ð��T�Ƽ��lչ���𡢇�����Ȼ�ƌW���𡢽��Kʡ��Ȼ�ƌW�����T��W���л�������Y�����gӭ�L���n�}�M�Wվ��https://sklqrcm.um.edu.mo/chun-ming-wang/���_չ����������
ԭ��朽ӣ�https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.202417734?af=R
