ͬ��(j��)��W(xu��)�Ž��ҽ�������˸�Ч���d���ͺ���ĸ߷������ݘ�(g��u)��ԭ���������T��(d��o)��������Acid-induced adsorption, AIA���͡��H�͏�(qi��ng)����������Affinity-enhanced attraction, AEA�����D 1���D 2����
��������d�w��ȫ��Ч���f���������ӣ��ǵ��ׯ������M���ޏ�(f��)�������������t(y��)���I(l��ng)���һ��(g��)���Ć��}��Ȼ�����y(t��ng)�d�w��������늺ɣ��wѭ�h(hu��n)�r(sh��)�g�^���Ҵ��ڰ�ȫ���}���mȻ����x���d�w���Ա����@��(g��)���}�����ǰ��dЧ���^�͡��߷������ݿɌ�����Ӱ��d�ڿ�ǻ�У���ȫ�Ժã����L���ԁ�ͬ�����R���dЧ���^�͵��y�}����ˣ���Θ�(g��u)����Ч���d�������ӵķ���x���߷���������һ��(g��)��Ҫ������(zh��n)����Ҫ����Փ��(chu��ng)�·������Q���}��
�Ž��ҽ��ڈF(tu��n)�(du��)�L���ԁ�һֱ���¸߷������ݰ��d�������ӵ��о������˹���Ĥ�����ݣ�ACS Nano 2014, 8, 5022���������ǿ��ǡ����ݣ�JACS 2017, 139, 7640�������p�T�ء����ݣ�Nano Lett. 2018, 18, 5562�������������룬Ҫ��(sh��)�F(xi��n)�������ӵĸ�Ч���d�����������{(di��o)�������c��������֮�g������á�����Һ�У���������ͨ�^����(d��ng)�U(ku��)ɢ�������ݡ�ͨ����r�£����ڶ���֮�g��������^���������(sh��)����ӕ�(hu��)�x�_���ݡ�����(d��ng)����֮�g�����������^��(qi��ng)�r(sh��)���Ϳ��Ԍ������(sh��)���������������Ĥ�ϣ���(sh��)�F(xi��n)����Ӳ��@��������(w��n)�����d��������(j��)ԓ���룬���������AIA��AEAԭ���Ը�Ч���d���ͺ��ᡣ
����?c��)O(sh��)Ӌ(j��)��һ�N�µĸ߷����������(y��n)�C����ԭ������(sh��)�(y��n)������ͨ�^AIAʹѪ�t���װ��d���_(d��)����79%��ͨ�^AEAʹRNA���|(zh��)��DNA���d�ʷքe�_(d��)����85%��75%���@Щ�Y(ji��)������������ͨ�ĸ߷������ݵİ��dЧ�ʣ�һ��С��20%������Ҫ����?y��n)�AIA��AEA�� ������(d��ng)���d�����ã��D 1����
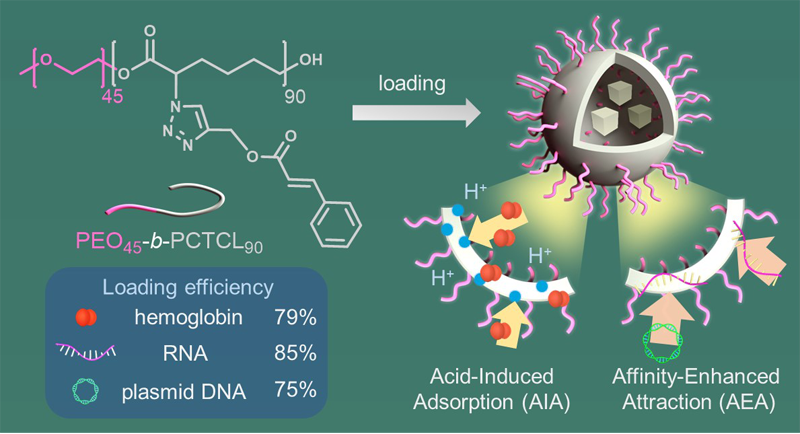
�D 1. ��Ч���d���ͺ����ԭ�������T��(d��o)������AIA�����H�͏�(qi��ng)��������AEA��
AIA����������ˮ�a(ch��n)�����|(zh��)�ӿ��Ա�������F(tu��n)�е�ԭ�ӵĹ�(du��)����������M(j��n)��������Ĥ�ӵ����I���ѣ����γɵ��Ȼ����u������ͨ�^�o����û���I�������������ӣ��M(j��n)����(sh��)�F(xi��n)���ĸ�Ч���d(�D 2)��
AEA���߷��ӂ�(c��)��ϵ�������F(tu��n)������������F(tu��n)����ͨ�^���ШC��x�����á��͡��ШC�жѯB��������ؓ(f��)��Ҹ�������ӵĺ�����ӡ����⣬�߷��ӂ�(c��)��c������؏�(f��)��Ԫ��һ���ĽY(ji��)��(g��u)�����ԣ��M(j��n)һ���ӏ�(qi��ng)�˶���֮�g���������á��@Щ���ض������ں���ĸ�Ч���d��

�D 2. ����ͨ�^��I��AIA�ͣ�II��AEA�քe���d���ͺ����ʾ��D
�ڰ��d���a�оGɫ�ɹ⵰������|(zh��)�������ݿ��Ԍ��|(zh��)����Ч�f������(x��)����(n��i)�M(j��n)�б��_(d��)������۽��y(c��)ԇ������AEA��Ӱ푴���ӵİ���(n��i)ጷ��c���_(d��)���c��(du��)�սM�����|(zh��)���M����ȣ��ɹ⏊(qi��ng)����߃ɱ����ϣ��D 3�����M(j��n)һ����(sh��)�(y��n)�C��(sh��)�����d�|(zh��)��������(du��)���˸ΰ���(x��)����HepG2�����D(zhu��n)ȾЧ����95%���ϣ�72С�r(sh��)�����ɴ˿�֪��AEA�ڻ����f���I(l��ng)����Б�(y��ng)��ǰ����

�D 3. ���dpEGFP-N1�|(zh��)����������Ч��(sh��)�F(xi��n)�˻����f�ͺͱ��_(d��)���Gɫ���ɹ⵰�ף��{(l��n)ɫ����(x��)���ˣ������ߣ�20�ף�
AIAԭ�����ԔU(ku��)չ���߂����ׂ�(g��)���c(di��n)���d�w�wϵ��1���wϵ�����|(zh��)��Դ�Դ��߷�������������I�Ľ��⣻2���d�w�а������й�(du��)����Ҿ���ֲ����������������|(zh��)�ӵĂ��f�ͷ�ɢ��3���d�wĤ�о��������еĻ��W(xu��)�I���ڔ��Ѻ�¶���Ļ��F(tu��n)���܉��c��؛����Ӯa(ch��n)�����I���o����á�
AEAԭ���m���ھ߂�������һ���c(di��n)���d�w�wϵ��1���d�w��Ĥ�Y(ji��)��(g��u)������(du��)��؛������еĸ���ӻ��F(tu��n)��ؓ(f��)늺ɻ��F(tu��n)�����H�����õĻ��F(tu��n)��2���d�w��Ĥ�Y(ji��)��(g��u)���и�������ӵĻ��F(tu��n)�����Դ��M(j��n)�d�wĤ�c��؛�����֮�g�a(ch��n)�����ШC�жѯB�����á����⣬��(d��ng)�ۺ����к����c����ӡ�؛��؏�(f��)��Ԫ���ƵĻ��W(xu��)�Y(ji��)��(g��u)�r(sh��)��AEAЧ��(y��ng)�����M(j��n)һ������(qi��ng)����ˣ��Ɍ�AIA��AEA�ƏV�������I(l��ng)��
ԓ�ɹ��ԡ�Two Principles for Polymersomes with Ultrahigh Biomacromolecular Loading Efficiencies: Acid-Induced Adsorption and Affinity-Enhanced Attraction�����}�l(f��)��(Macromolecules 2020, DOI: 10.1021/acs.macromol.0c00252)��ͬ��(j��)��W(xu��)��ʿ��ꐎ���Փ�ĵĵ�һ���ߣ��ӱ���W(xu��)�ؽ���������ڶ����ߣ�ͬ��(j��)��W(xu��)�Ž��ҽ�����ͨӍ���ߡ�ԓ�о��õ����ҽܳ�����ƌW(xu��)����21925505���Y����
Փ��ԭ�ģ�
Chen, S.; Qin, J. L.; Du, J. Z.* Two Principles for Polymersomes with Ultrahigh Biomacromolecular Loading Efficiencies: Acid-Induced Adsorption and Affinity-Enhanced Attraction. Macromolecules 2020, DOI: 10.1021/acs.macromol.0c00252.
https://pubs.acs.org/doi/abs/10.1021/acs.macromol.0c00252
�Ž��ҽ����n�}�M��퓣�https://jzdu.tongji.edu.cn/
- ���ϴ�W(xu��)��Adv. Sci.�����߷������ݏ��Ԍ�(du��)�X�[������Ӱ��о����M(j��n)չ 2021-09-02
- ͬ��(j��)��W(xu��)�Ž��ҽ����n�}�M���������h(hu��n)��(n��i)�����_�h(hu��n)�ۺ��T��(d��o)�ԽM�b(NCA-PISA)�·��� 2019-09-17
- ͬ��(j��)��W(xu��)�Ž��ҽ����n�}�M�����ǿ��ǡ��߷����������M(j��n)չ 2019-07-11
- �K�ݴ�W(xu��)����ڡ��������Ҙ�(bi��o)��(zh��n)�c���g(sh��)�о�ԺWai Cheong Tam��ʿ IJBM�����ܽM�����������о��M(j��n)չ 2025-05-22
- �K��������/�������w���� Int. J. Biol. Macromol.�������ޏ�(f��)�������Ӳ��ϵ��о��M(j��n)չ 2024-04-03
- ��(f��)����W(xu��)���������n�}�M ACS Macro Lett.�������z�ص��ס�Һ-Һ������x��Һ�ļ��й̻��C(j��)�� 2023-08-17
�\���P(gu��n)ע�߷��ӿƼ�

- CPHI����չ��(sh��)�(y��n)�҃x���c�O(sh��)��...
- ���ܹ��A��朆���������22��...
- ����(b��o)���C(j��)��(hu��)��500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ�(hu��)�h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c(di��n)������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��(hu��)
- �Ј�(ch��ng)��300�|��PMEC China ɫ...
- ����ע��(c��)��2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �Ĵ���W(xu��)���A���ڈF(tu��n)�(du��)��Adv....
- �Ĵ���W(xu��)���������ڈF(tu��n)�(du��) Ang...
- �A��������W(xu��)���ָ���ڈF(tu��n)�(du��)...
- �칤����x/�R�w�R/���ƽ� S...
- �A���r(n��ng)�����/������...
- �Ʊ��ҽ���/�֘s�I(y��)���ڈF(tu��n)�(du��)...
- ��ӿƴ����|��/�������F(tu��n)�(du��)...
- �A������������� Angew: ...
- �Ĵ���W(xu��)������ AFM������ʯ...
- ��۳��д�W(xu��)�����n�}�M CEJ...
- �Ї��ƴ����d���n�}�M���邐...