��������|��ECM����һ���ӑB���ӾW�j�����{����ͬ�M�������ٵď��ȺͽY����ECM�h�����κμ�׃������������ʧ�⡣���@Щ��r�£����漰�ĽM���o���@����������zԭ���͏����w�S���S��ECM�ĄӑBƽ�⣬�Ķ����½M�������ٵ�֧�������^����ه��������ø��LOX���������Ǵ��zԭ���͏��Ե���֮�g���r�����P�Iø������M�zԭ���͏����w�S�İl���ͳ��죬�S��ECM�еķ��B�����͵�LOX����ˮƽ�����µ����|���Ƚ��ͣ��Ķ��ɔ_ECM���������W���ܡ�����ECM���ص�����W�������ί�ʹһ�Nʮ�־���ǰ�����ί�������Ȼ����Ŀǰ�����d�w���f�ͷ������������������ʵ��¡����ßo�������ھֲ��Ȇ��}����ˣ������ί�������ͻ�ƣ�Ҫ���_�l�µľֲ�������fϵ�y�������ֲ�ECM�h����
���ڴˣ��Ϻ���ͨ��W�t�WԺ��������tԺ/�Ϻ��Ђ��ǿ��о������ć����ڈF��Ϻ���ͨ��W���ه��H��ƽ�D�ױ���Ժ����������F�ͨ�^���ؽM��LOXL1�|����pLOXL1���b��{��֬�|�w��Ȼ��ͨ�^���z늼��z������b����-���{���w�S�ĺˌ��У��Ԍ��FLOXL1�ľֲ��e�ۺ�����������öȣ��Ķ����F���ٵ�ECM푑���ԓ�о����}�顰Rapid Extracellular Matrix Remodeling via Gene�\Electrospun Fibers as a ��Patch�� for Tissue Regeneration����Փ�İl���ڇ��H�����ڿ�Advanced Functional Materials (2021, 2009879)�����gӭ���P���I��ʿ������ć��Fꠏ��²�ʿ���о�����ע���D��·�����t�W���ϡ����t�������о���

�D1 �{��ECMƽ��Ļ���늼��w�Sϵ�y�Ę������������h����
�ڱ����У�������һ�N���Ԍ��z�����|���f����M���ĸ�Ч늼��w�Sϵ�y�����f��ϵ�y�b�dpLOXL1�����Դ��M�zԭ���͏��Ե��ĺϳɡ����Ե���߀�����L�������w�S�Ľ��ԣ��ԾS��ECM�н����c����֮�g��ƽ�⡣�w�⌍������pLOXL1-Lipo@PLCL-HA��������30���Ќ��F��pLOXL1�ij��mጷţ��������DȾЧ�ʱ�����50�����ϡ�pLOXL1-Lipo@PLCL-HA�M��HVF���zԭ�w�S�͏����w�S���P���ı��_ˮƽ�@�����������M���෴�����|���ٵ���ø�ı��_ˮƽ���@���͡����|���ٵ���ø���Ƅ��ı��_ˮƽ���{���w���о����ü��ø�����ģ�ͣ��c���սM��ȣ�pLOXL1-Lipo @ PLCL-HAֲ��M���h���zԭ�����ܶ������90�����ϡ�ECM����COL1A1��COL3A1��Elastin��Fubilin5���ı��_ˮƽ�@�����ӣ��Ķ����M�zԭ���͏��Ե��ĺϳ��Լ����r��������朽��������w�S���Ķ����M����M�����ޏͲ��֏���ĽY��֧�Ρ�
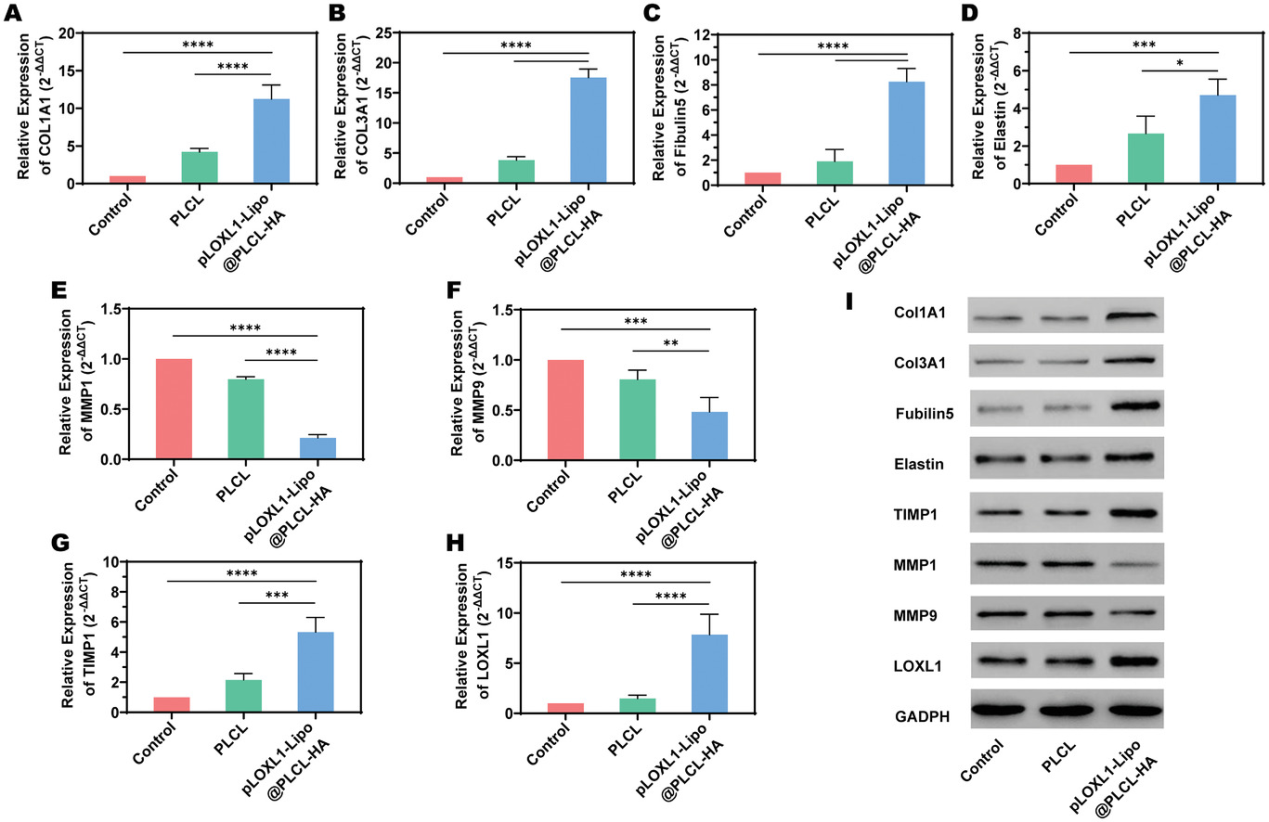
�D2 ����ˮƽ��ECM���P���ӵı��_

�D3 ���ø��ڲ�ͬ�zԭ���ܵ���r�u�r
�C�����������@��о��У��ɹ�������һ���µĻ���-늼��w�S�f��ϵ�ypLOXL1-Lipo@PLCL-HA�����U�������^�ߵ����������ʡ����⣬���{����LOXL1�錧��ECM���e�ͽ���֮�g��ƽ�⣬�Ķ����M��֧�Ώ��ȵIJ��ֻ֏ͺ��ؽ�����ˣ�pLOXL1-Lipo @ PLCL-HA�Ĺ�����ʽ����һ�����a��������ECM�����c�t��һ����©���������������о����������_�l�a�����ޏ��e�`��ԓ�F��_�l�Ļ���-늼��w�S���a��������MECM�����ؽ����ί������ṩ���¸��
���µ�һ���ߞ������R������·ِ����ͨӍ���ߞ����ć�����������������t����ԓ�о��õ��ˇ�����Ȼ�ƌW����ί�͇������c�аlӋ�����Ŀ��֧�֡�
ԭ��朽ӣ�https://onlinelibrary.wiley.com/doi/abs/10.1002/adfm.202009879
���ߺ��飺
���ć�������/�������Ϻ���ͨ��W��������tԺ/�Ϻ��Ђ��ǿ��о�������Ҫ�����D�������t�ò��ϣ����¹ǡ��P���ȽM���ޏ��ؽ����о����Ե�һ/ͨӍ���߰l��SCIՓ��140��ƪ��IF>10��40��ƪ��������7200��Σ�H=46������50��헣��D��2헣�������Elsevier����1��������9�����H�����¹����౾�s־�ľ�ί�Ϳ������������@���Ҽ������˲�Ӌ�������և�����Ȼ�ƌW�������c�Ŀ���Ƽ������c�аlӋ���n�}������Ȼ�����Ŀ���Ϻ��п�ί�ȸ���n�}10��헡��нM���f��Ӌ������μ��˲š��Ϻ����˲Űlչ�����֧�֡����Ї�������όW�����¡������t��������ϸ�����ί�T�ȡ����gӭ�����������t�W�����о����R���ͮa�I���ĸ����I��ʿ�����ԓ�Fꠣ�50555736@qq.com��
- �|��������W�w�J�ȡ�ACS AMI�����Bͨ���ͨ�������ۺ���/MOFs�ͺ��o늼��w�S���١���Ч���@ˮ�п����ط��� 2020-12-31
- �K��ʩ�ڽ��ڡ��Ϻ�������ć����ںͺՠ�������WHelder Santos���ڹ�ͬ�_�l���߹��ܻ����o늼��z�w�S֧�����ƚ����[���Ͱl 2018-08-30
- �A��������W߅�������ڈF�Nature Chemistry����ģ�M��������|ҺҺ����x�錧�ĽM�b���������������ĺ��sģ�� 2025-06-10
- �Ͽƴ����˾������n�}�M Nat. Commun.: �������п�Ҋ��푑��ĕr�ՄӑBճ����ˮ���z����̽���������c��������|����� 2025-02-07
- �{�����IJ���������܊���tԺ������Ф���������tԺ���r���Ͽƴ��Y�d�� ACS Nano�����٘����������|���ڟo�MխѪ������ 2025-01-17
