��ǻ���������g����ǻ�[���Ļ����ί������������g�����d�w�p����ɵIJ������ϵK��CNI-ED���Ȳ��l�Y������Ӱ푻����g�������|�����R���ϣ�ED���ί�������Ҫ�漰�������ø5���Ƅ���PDE5is��ʹ�á��w��ע�䯟����ICIS������ղ����b�ã�VED������ȣ����@Щ������CNI-ED���ί���Ч����ԓ�����£���o���wֲ�����g�ɞ�CNI-ED���ߵ��R���x��Ȼ��������һ�N�������ί����ԣ���o���wֲ�����g���F���ί��M�úʹ��ڵęCе����/��Ⱦ�ȝ����L�U���������R�����õ��ƏV����ˣ�����һ�N���ͷ�����ġ��ί�Ч���@����CNI-ED�ί��������зdz���Ҫ���R���rֵ��
��������ɼ������������������w���V������CNI-ED�ί��������C���g�|�ɼ�����MSC�������������w��MSC-Exo�������Н��������������Լ�����������ˣ�MSC-Exo�ί������Դ��ڰ�˥�ڶ̡��ױ�����ϵ�y��������Ⱦ����ԡ��b���܂��M���ޏ͵ď��s�^�̣������������w�w�ȵķ����Ժ����ó־��Գɞ��ޏ��p�����P�I���}��

�D1. HG@Exo�����ί�CNI-EDʾ��D��
1.������ˮ���zHG�Ƃ乤ˇ���Ρ����z���ض�/�r�g�m��

�D2. ��A-B�������w��ò�������ֲ�����C�������w��־����CD9��CD63��TSG101�ı��_����D-F��HG�ĺϳɣ�FTIR���V�̓Ȳ���ò����G��HG�ڲ�ͬ�ضȺ͕r�g�µ���׃���W����H��HG��ע���ԡ�
2.������ˮ���zHG������ADSC-Exo�ľֲ���ጺ����ó־���

�D3.��A��HG@Exoˮ���z������BCNI�����p��ģ��ʾ��D����B��DiR��ӛ�������w�w�Ȍ��r�O�y��
3.HG�����������w��CNI-ED���ί����á����BCNI����IJ�����
����HG@Exoˮ���z�ί�ģ�ʹ���IJ����ܣ�4�ܺ�l�F�����g�M��BCNI�M��HG@Exo�M��PBS-Exo�M��HG�M������B�ȉ�/ƽ�����}����ֵ�քe��0.87 �� 0.04��0.39 �� 0.02��0.65 �� 0.05��0.44 �� 0.03��0.52 �� 0.04���D4A-F�����@���H�f��BCNI������ED��Ҳ�C��HG@Exo���@�����BCNI����IJ����ܡ�

�D4. HG@Exoˮ���z�ί�ģ�ʹ���IJ������u������A-E��ICP�������t�l��ʾ��60 s�Ȍ�CN�M��늴̼��ĕr�g����F�����ICP�cMAP���ʡ�
���˙z�yHG@Exoˮ���z�ί�CNI-ED��Ч�Ե�ԭ���о��M�����w�⼚�������]��HG@Exoˮ���z�QҺ���Ҝ��^��IJ����ԣ����о�ֱ���x����ADSC-Exo�M���w�����B���A���D5A-C�Ǻ��d�w��/��ǻ����CN/MPG���Ľ��ʽY�����w�����B���E�����ί���24��48��72С�r��CN/MPG�Kĩͻ�����L�Ĕ�Ŀ���L���M�Мy�����D5D�����C��ADSC-Exo�@�����M���Sͻ�����L���D5E-F����������ADSCs��ADSC-Exo����4�ܺ�CN/MPG��nNOS�ı��_��r��Ҳ�l�FADSC-Exo̎���M��nNOS���_���@���ڌ��սM��ADSCs+GW4869�M���D5G-H����

�D5. ��A��CN/MPG���ʽY�����w�����B����B��CN/MPG���ʈD����C�����B0��i����24��ii����48 h��iii������Ԫ�����L��r��iv��v��iii�ķŴ�D����D����Ԫ��ֲ�w����E-F�������w��ADSCs����Ԫ���L��r����G��CN/MPG��nNOS�ı��_��r����H��nNOS�c��-���ӵ��ı�����
4.ADSC-Exoͨ�^���MSCs�Ĵ�������p�����ޏ�
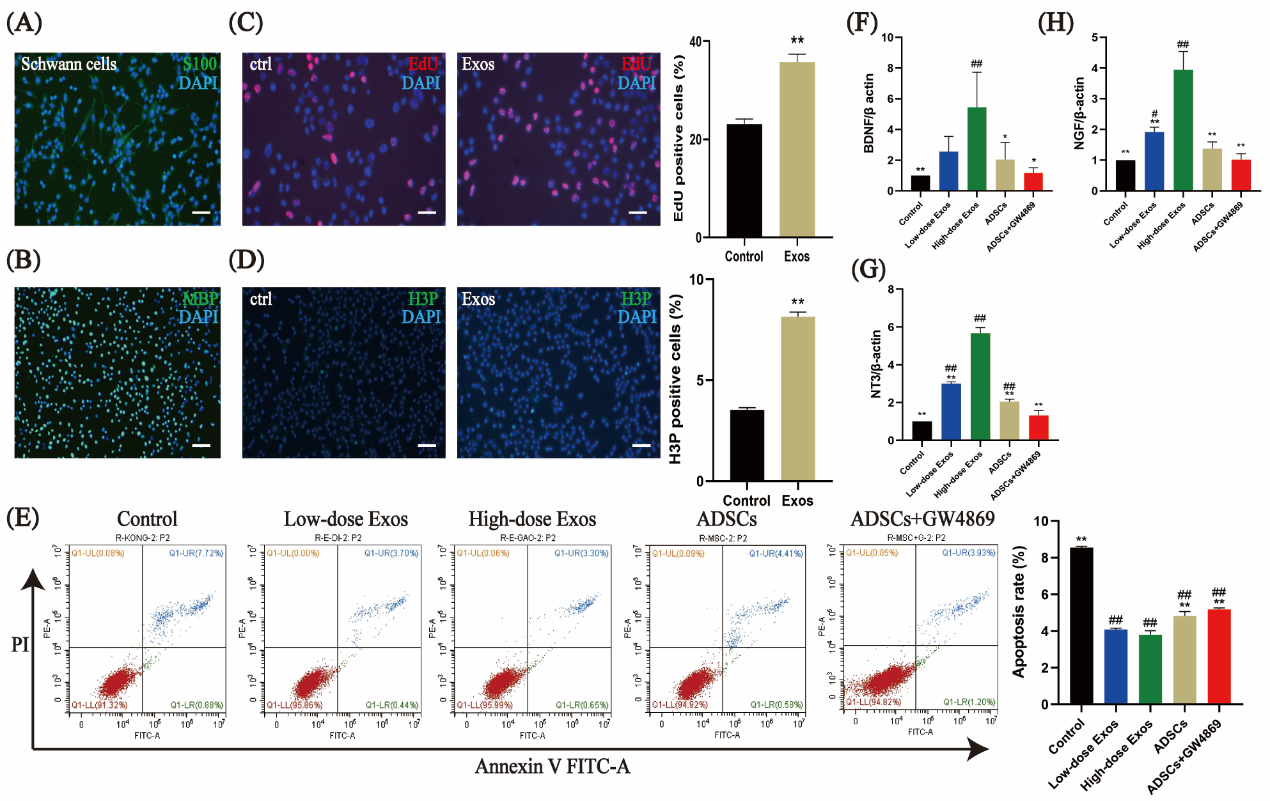
�D6. ��A-B��SCs��C��S100��MBP����C-D�������w���A24h��EdU��H3P�ı��_����E�������w����SCs������r����F-H��������_��r��
5.HG@Exo���ƴ���CN/MPG�ĽY������
���⣬��ȼ����g�M��BCNI�MCN/MPG�@ʾ���Sͻ�[Û���Sͻ���ݻ��͵��ܶ��z����HG@Exo�M�����zȾɫ���ܶȺ�Ҏ���Եõ��@�����ƣ��D9��������HG@Exo�@�������CN/MPG�ĽY�����ܡ�

�D7.��A��MassonȾɫ����B��ƽ�����������zԭ��������ֵ��

�D8.��A��������nNOS���_����B��nNOS�붨����������C�����d�w��nNOS���_����D��nNOS�c��-���ӵ��ױ�ֵ��

���Ϲ����ԡ�Injectable thermo-sensitive hydrogel containing ADSC-derived exosomes for the treatment of cavernous nerve injury�����}�l���ڡ�Carbohydrate Polymers���ڿ��ϣ��п�Ժ���һ�^��IF��10.723�������ĵ�һ���ߞ�ɽ�|ʡ���tԺ�������t��������ɽ�|��W�Tʿ�о�����������ͨӍ���ߞ����u��W�D���t�W�о�Ժ��������Ƹ���ڣ��n�}�M�Wվ��https://www.x-mol.com/groups/BMTMers, �n�}�M�Ź���̖����������c�D���t�W�n�}�M����ɽ�|ʡ���tԺ��������������ڡ�
ԭ��朽�:https://doi.org/10.1016/j.carbpol.2022.120226
- �|�ϴ�W���������ڈFꠡ�ACS Nano�������b֬���ɼ��������w�aƬ�����{���װY�ʹ��M�M������ 2025-06-09
- �|�A��Wʷ��ꖽ��ڈFꠣ������w������푑��Ԙ�����Ӽ{�����z�Ɍ��F���ԷΓp���������{���Ϳ��������ί� 2025-05-15
- ���_��W��������ڈF� JACS������ˮ���z�����f�������w - ����������ˎ����Ⱦ���������y�} 2025-05-06
- �|�ϴ�W���������ڈF� JCR: �_�l�d�g���|�ɼ�������ģ�K���ڸ���ȱ�p���ޏ� 2025-04-03
- �п�Ժ�������MԺ�ŌW��F� Matter�����Խ�����Ͼ����{�������w���ڴ�Ѫ���fͬ�ޏ� 2024-11-22
- �㽭��W�����ҽ��ڈF� Adv. Sci.����������|ˮ���zǶ��֬����Դ�g���|�ɼ��������w���ڴ��M�������������Ϻ�Ƥ�w���� 2023-09-19
- �V�t��Ժ���١��V���T��ܰ Nat. Commun.����ע���V-�p�����}MOF����ճ�τ�ͨ�^�����^���w�S�����M���|�����Թ������� 2025-07-07
