��������Ɯ����о�Ժ�����о��T�����t��һԺ��A�P��ʿ�����t�ٿ�ǻ�tԺ���s�h���ڈF������ó������M�b�ķ�ʽ������һ�Nȫ�µij����ӹ�Ἁ�{�������������ﱻĤ���P��Ⱦ���_���Ԃ��ڵ��ί��ṩ��һ�l���ڵ��ί�������ԓ�о��ɹ��l���ڇ��H피��ڿ���Advanced Materials�������Ɯ����о�Ժ��ʿ��������о������T��������һ���ߡ�
�_���Ԅ�����m������Ⱦ�nj��������ϕr�g���L����Ҫԭ������Ⱦ���ڵ��R���ί������������ί��̈́��汣�o��Ȼ�������������R���ďV��ʹ�Þ鼚���ṩ�˫@����ˎ�Ե��x���������⣬����߀����ͨ�^�ɵ����|�����⼚��DNA��������Ǻ�ø�M�ɵ�����Ĥ�����o�Լ����ܐ��ӗl����ˎ��Ĺ��������ﱻĤ����ˎ����ă���죬���M����ˮƽ�D�ơ���ˣ�������Ĥ��ʽ���L�ļ�������Ҏ�����ص���ˎ���Ǹ��μ�����10-1000����60%~80%�ļ�����Ⱦ�c��������Ĥ�γ����P�����o�Ɇ���������Ҫ�_�l��Ч�ķǿ����ز��ԁ푪����������Ĥ��Ⱦ�Ą��档
��������S����Ч�ķ����������ڿ����ί����绯�������������/������������߯�������������������ᯟ���������ù�ᄩ��ͨ�^�o���Ĺ������T���ֲ��ᯟ���M���ƉIJ�ԭ�����������_��������Ŀ�ġ����⣬�ߜ�߀����ͨ�^ʹ���ﱻĤ���е�������Ե�������͵����|��ʧ����Ɖ����ﱻĤ�ķ����Y����Ȼ������ᯟ�����خ��Բ��㣬�������������c�������ڿ����I��İlչ��������ᯟ���c���W�����W������Y�ϵąfͬ�ί�����������Q�����Ć��}�����W�����W��������ͨ�^���D����D�����a�������u�����ɻ���ͨ�^�Ɖ�DNA�������|�ͼ���Ĥ�T���������������⣬���W�����W�����a���Ļ������������Ӽ���Ĥ��ͨ�Ժ͌���������ԣ��Ķ��_���fͬ�������á�
���ڴˣ����������Ú���������Z�{��������CPNC��������������ø��GOx���́��F�x�ӣ�Fe2+��֮�g�Ķ��ؚ��I����λ����ã�ͨ�^�����Ӳ��������˹�Ἁ�{��������CPNC@GOx-Fe2+������D1��ʾ�����˷������������Ϲ���ί��ͻ��W�����W�����������M�Ѕfͬ���磬���ҿ���ԭλ���l�������F�����ڵı��o��

�D1. �����ӹ��{��������CPNC@GOx-Fe2+���Ƃ估���ڴ��M�������������еđ��á�
ͨ�^�M�b�ij��������{���������ʬF�{���K�Y�������ҳߴ��s��247.9�{�������еĸ��M��ͨ�^����R��X�侀������V�M����Ԕ�����������D2��

�D2. �����ӹ��{��������CPNC@GOx-Fe2+�IJ��ϽY��������
��808 nm�Ľ��t������£�CPNC@GOx-Fe2+չ�F�����õĹ��Ч�����ʬF�����ه�ԣ����Ҿ������õ�ѭ�h�����ԡ�ͨ�^�yԇ���ϳ������Ե�֪���M�b���^�̌�GOx��ø���Բ��]���@����Ӱ푡�������l���£�GOx�f���ļ������^��ͨ�^3,3'',5,5''-�ļ��������@ɫ�����M���˜yԇ���Үa���Ļ�������Nͨ�^���혴Ź���yԇ�Mһ���C�����u�����ɻ������D3��
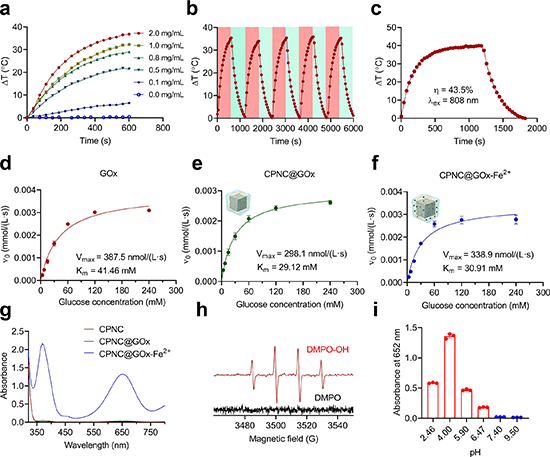
�D3. �����ӹ��{��������CPNC@GOx-Fe2+�Ĺ�����ܺ�GOx�o���ļ��������ܱ�����
�����ӹ��{��������CPNC@GOx-Fe2+����׃��������S. mutans��չ�F�����õąfͬ����Ч�������Ҍ���S. mutans�γɵij������ﱻĤҲչ�F�����õĽ��xЧ�������D4�͈D5��

�D4. �����ӹ��{��������CPNC@GOx-Fe2+���w�⿹��Ч���u����
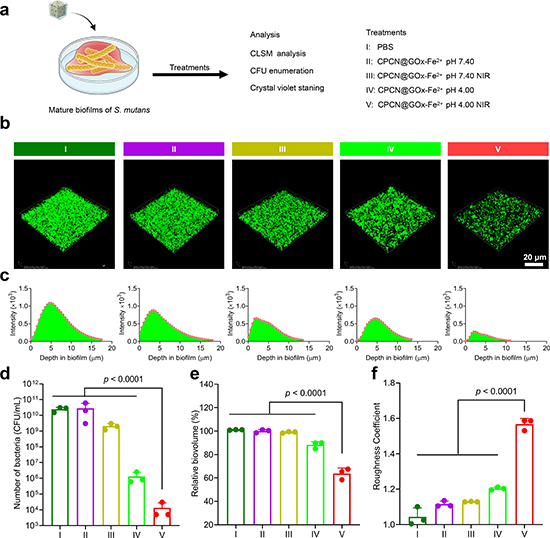
�D5. �����ӹ��{��������CPNC@GOx-Fe2+���ﱻĤȥ��Ч�����w���u�r��
ͨ�^���M�W��ȫԭ��ģ�M̽���˳����ӹ��{���������fͬ�����ĝ��ڙC�����Y�������������ӹ�Ἁ�����wϵ�ĝ��ڿ����C�ư����ɂ����档���ȣ��������^�̮a����·OH��������Ĥ������֬�p���ӌӣ�����������������ܵ��ɔ_������Ĥ�Y������������Σ���Ч�������˼���Ĥ�������Ժ�ȱ�ݣ��Ķ��fͬ�����ˌ�����Ĥ��·OH���Ɖġ����D6�͈D7��

�D6. ��ͬ̎����S. mutans�ĵ����|�M�W�ʹ��x�M�W������

�D7. �fͬ�������Ì���Ĥ������Ӱ푵�ȫԭ�ӷ��ӄ����Wģ�M��
��S. mutans����Ĥ���P��Ⱦ��������ģ���У��������^�̮a�����u�����ɻ����Ԇ������ɻ��ۺ��^�̣�������ԭλ�γ�ˮ���z�M�Є��ڱ��o���w�Ȍ���C����CPNC@GOx-Fe2+�ąfͬ����Ч���̈́��ڱ��o���ܣ��������ڲ�Ӱ푿�ǻ������Ⱥ����r�¼ӿ��Ⱦ�����������ϡ����D8��

�D8. �w�Ț����Ϳ�ǻ����Ⱥ���u����
�˹����õ�������Ȼ�ƌW���� ������̖52003184, 22103088, 82204940, 52203184�� 22275043�����Ї���ʿ��ƌW���𣨻���̖2022M723108�����Ɯ����о�Ժ���ӻ��𣨻���̖WIUCASQD2021022��WIUCASQD2021019�����㽭ʡ�R���z��\���c�D���о����c����ң�����̖2022E10022�����Y��֧����
�īI朽ӣ�https://doi.org/10.1002/adma.202301664
������F�B��
�����ۺ���M�b�c���ܻ��n�}�M��������о��I������������Եĸ߷��Ӳ����OӋ���ϳɼ��ԽM�b�����ڿ˷�����/���Y��ˎ�Է���đ��á����䌣ע��1������푑��߷��Ӿۺ�����OӋ���ϳ��c�������{�M�b�w�Ƃ䡢���x����ܻ�����2�����ڿ˷����������Y��ˎ�Ե����ܸ߷��Ӿۺ���{���wϵ�����R������錧����3���������ܿ����Ƅ��аl�c�a�I�����n�}�M���������Chem. Soc. Rev., Adv. Mater. (2), Adv. Funct. Mater. (4), ACS Nano (3), Nano Today���s־�ϰl��һ�^����30��ƪ������Ӱ����Ӵ���10������25ƪ��
�n�}�M�WվԔҊ��http://wiucas.ac.cn/group/liuyong/
- �|����W���ɽ��ڡ��������о��T�F� Angew�����ﱻĤ��������ĽY�����m���������۷���Ϳ�� 2025-04-14
- ����������W���d���ڈFꠡ�ACS Nano�����ۣ�D-�����ᣩ�{������ͨ�^�ɔ_��������ľ��Ǻϳɽ錧���ﱻĤ�߽� 2024-03-13
- ����������W���d���ڈF� ACS AMI��GSH/pH��푑��{������ͨ�^�fͬ�Ĺ�ͻ��W���������ͼ������ֽ��Sɫ����������ﱻĤ 2024-01-29
- ���u��W�ڱ����ڈF� Small�����п���ֹѪ�͏V�V�������ԵĹ���ˮ���z���ڼ��ق������� 2025-06-03
- �����A����ǻ�t�WԺ��ѩ�������n�}�M CEJ: �����{�����߷������پ����w�D�Ƶ�����ˮ���z���M�������Ԃ������� 2025-05-21
- ���ݴ�W���Ӱ��о��T�F� AFM��һ�N�������������Ե���λ���u���V�V�������r�ЙC���ˮ���z���ڴ��M���������� 2025-05-06
