����������W���d���ڈFꠡ�ACS Nano�����ۣ�D-�����ᣩ�{������ͨ�^�ɔ_��������ľ��Ǻϳɽ錧���ﱻĤ�߽�
�������ﱻĤ��Ⱦ��ֲ����ʧ������Ҫԭ�����ﱻĤ���H���o������������ϵ�y����������ƿ����صĝB��߀�����˼����Ĵ��x���ԣ����¿����ص�Ч�����͡���ˣ���ʹ�]�п�������ˎ�Ի������ﱻĤ�еļ���Ҳ���J����и߶ȵĿ����������ԡ�
��ˣ�����������W���d�����n�}�M����ǰ�ڌ��۰������f��ϵ�y���аl��Polym. Chem. 2018, 9, 2733��Biomacromolecules, 2021, 22, 4871; Colloid. Surface. B 2021, 202, 111687�����Լ�����������Ⱦ����о����A��Adv. Mater. 2022, 34, 2109789��J. Mater. Chem. B 2023, 11, 2958; Macromol. Biosci. 2023, 23, 2200311����������þۣ�D-�����ᣩ�{���������С���Ӱ����ᣬ���ư������ڴ��x�^���е����ģ�����䌦���ﱻĤ�����Ч�����о������OӋ�ϳ���һ�N����D-�����������Ƕ�ι�������Mһ���M�b�ɼ{������FA NPs���D1�����о��l�F��FA NPsͨ�^�ľ��ǽY�ϵ���4��PBP4���錧�خ��Բ�����������ľ����У����Mһ���|�l�c�ľ����B�ӵĵ��ۘ��w�S���x��ͬ�r�p��EPS�Ķ��Ǻ͵����|�������Ɖ�EPS�ĽY�������ԣ���K�������ﱻĤ�߽⡣���⣬FA NPs�@�������˿�����������ﱻĤ��Ч�������F��С��ֲ�������ﱻĤ����ȫ���������ί��������ﱻĤ��Ⱦ������Б��Ý�����
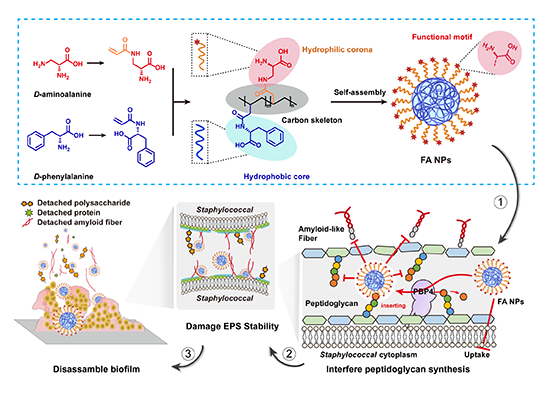
�D1.FA NPsͨ�^�ɔ_��������ľ��Ǻϳɽ錧���ﱻĤ�߽�Ĺ��ܙC��ʾ��D��
����Ҫ�c��
��1��FA NPs������ﱻĤ��Ч���о����о��l�F����FA NPs̎��������������ﱻĤ�γɴֲڡ���Ҏ�t���棬���ﱻĤ�ж��Ǻ͵����|�����@���p�٣��ҽY�������Խ��ͣ�����FA NPs�܉���Ч�Ɖ�����������ﱻĤ�������ﱻĤ�е��ۘ��w�S��Ӱ��о����D2��������FA NPs�܉����ﱻĤ�ȼ����g�ĵ��ۘ��w�S�������M���Ɖ������ﱻĤ�ĽY�������Ժͷ����ԣ���K�������ﱻĤ�߽⡣
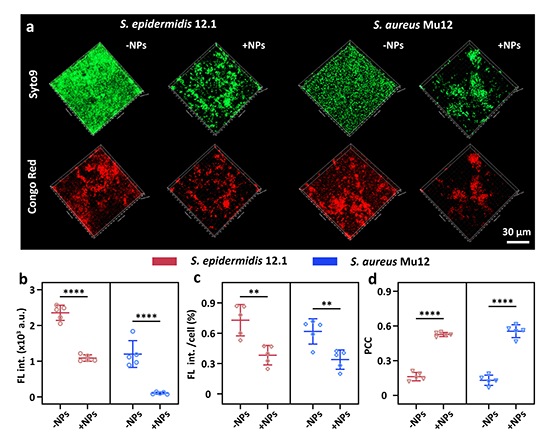
�D2. FA NPs̎�팦����������ﱻĤ���ۘ��w�S�ɷֵ�Ӱ푡�
��2��FA NPs������ﱻĤ�ęC���о����D3�������ۘ��w�S�c��������������ľ��Ǿo�����B��FA NPs��ͻ׃�ͽ��Sɫ�������USA300��������о����D3���l�F����USA300�����pbp4�����ó��r��?pbp4����FA NPs��ʧ�ˌ������ľ��ǵĽY������������USA300�����PBP4���ܱ��֏͕r��?pbp4+complement����FA NPs���ľ��ǽY������Ҳ���֏ͣ��Y��Ч���cҰ���ͣ�WT����pbp3����ȱ���ͣ�?pbp3��USA300�����ஔ���C����FA NPs�܉�ͨ�^PBP4���錧�خ��Բ�������������ľ����С�
����о��Mһ���l�F��FA NPs�܉���Ч�Ɖ�Ұ���ͣ�WT��USA300��������ﱻĤ������?pbp4�������ﱻĤ�oЧ����Ȥ���ǣ�������PBP4�����ܱ��֏��r��FA NPs�������ﱻĤ���Ɖ��������֏ͣ��C����PBP4�ڽ錧��Դ��FA NPs��������������ľ����������P�I���ã��Ķ��Ɖ���EPS�ĽY�������ԣ���K�������ﱻĤ�ķֽ⡣

�D3.PBP4���錧FA NPs������������ľ��ǣ��|�l���ﱻĤ�߽�C���о���
��3���w�ȼ������ﱻĤ������������D4����С���w�Ȍ������ﱻĤ��Ⱦ�ί��о��l�F��FA NPs�܉���Ч���������،����ﱻĤ��������������x������Sita�����ﱻĤ������÷dz����ޣ�< 103 CFU������ͨ�^FA NPsؓ�d�f�ͺ���ͬ�Ȅ����£����܉���ȫ������ﱻĤ����δ�z�������������Č��յ�>107 CFU�½���0�����о��Y��������FA NPs�����ﱻĤ�߽���܉��@����߿����ص��ί�Ч�ʡ�

�D4.FA NPs��С��Ƥ��ֲ�������ﱻĤ��Ⱦ���ί�Ч���u�r��
�C��������ԓ�о������һ�N���ڸ�Ч�߽����ﱻĤ�ľ۰�����{������FA NPs��FA NPs������PBP4�������D�����ò�����������ľ������ɔ_�ľ��Ǻϳɣ����Mһ���|�l�c�ľ����B�ӵĵ��ۘ��w�SÓ�x���p��EPS�ж��Ǻ͵����|�������Ɖ�EPS�Y������������K�������ﱻĤ�߽������о����Q����������ﱻĤ��Ⱦ�ṩ��һ��Н����ľ۰�����{�������¼��g��
���P�о��ɹ������ԡ�Poly(D-amino acid) Nanoparticles Target Staphylococcal Growth and Biofilm Disassembly by Interfering with Peptidoglycan Synthesis������}�l���ڌW�g�ڿ�ACS Nano�ϡ���Փ�ĵ�һ���ߞ鱱��������W�����ƌW�c���g�WԺ��ʿ���I���T�������x���������ں���ʿAO�о���Marco Chitt����ʿ������������W���d���ڡ�����h�����ں�AO�о���T. Fintan Moriarty�о��T��Փ�ĵĹ�ͬͨӍ���ߡ�ԓ�о��õ�������Ȼ�ƌW���𡢱���������W-�����Ѻ��tԺ�����t�W�D�������о����ġ�AO Trauma���Ї���W������Y���c֧�֡�
����朽ӣ�https://pubs.acs.org/doi/10.1021/acsnano.3c10983




