�܇��p�������l�����Ɍ����\�ӻ���X�����ϵK��Ӱ푻������w�����|���������������������ޣ����������R����һ�����ˮ���z����һ�N���Sܛ���ϣ��������������M���ļ����ԺͿ��{�����������|���ڽM�������I����ЏV���đ���ǰ�����M������늂����ԣ���Ҫ���ˮ���z���ρ��{���������О飬�����������Ч�ʡ���ˣ��_�l��һ�N�������ޏ͌�늶��ˮ���z����ʮ����Ҫ�����x��
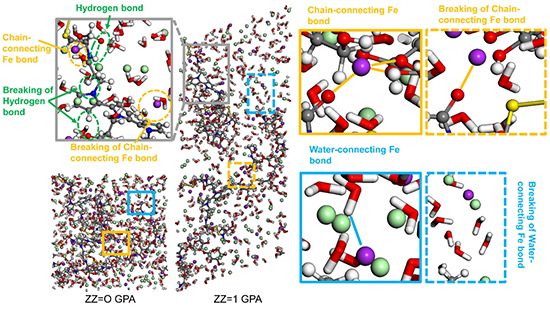
�D1 HASPyˮ���z�ķ��ӄ����Wģ�M
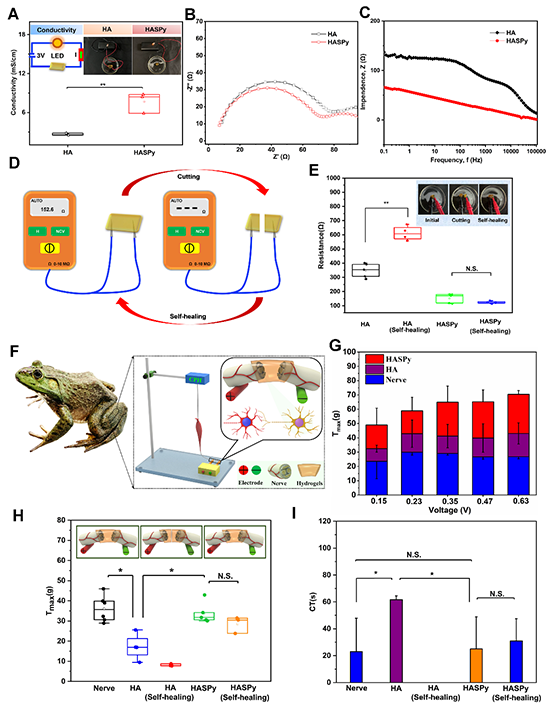
�D2 ˮ���z�����ޏ͌���Լ�HASPyˮ���z�w�����ţ��������

�D3 HASPy�cѩ����������ÙC�Ƶ���C

�D4 ���ӄ����W(MD)ģ�MHASPyˮ���z�Y��IL-17��IL-17���w
ԓ�����LjF����P�����ޏͶ���ˮ���z�ڽM���������P�о��������Mչ֮һ�����ޏͶ���ˮ���z�����W���ܲ������������ڽM�������еđ��á���ˣ��F꠰lչ�˼{���w��������Materials Science & Engineering C, 2021, 128: 112264����ø������Materials & Design, 2022, 217:110669�����������ޏͶ���ˮ���z�������䑪����Ƥ�w�M���ēp���ޏ͡�
ԭ��朽ӣ�https://doi.org/10.1002/advs.202302519
- ��ɽ��W�Ƕ�ؔ/�S�ſ�/������/���x�F� Adv. Mater.�������L�v���ԵĿ�ע����̿�{��øˮ���z���F�[���ąfͬ�ί� 2025-07-04
- �V�|ʡ�ƌWԺ������/�V�ݼt���tԺ���h���ַf MTB���h���{�ؿ�ע��ˮ���z���ж�-��ͻ����ȱ�p�ޏ��I������� 2025-05-17
- �����t���ǻ�tԺ�Մ�/�贺��/����Fꠣ�����ROS�|�lˎ��ጷ����ԵĿ�ע��ˮ���z���F�������Ϳ��{���w���fͬ�f�������������ί� 2025-04-15
- ���ϴ�W����/�S�M�F� AFM: �ڄӑB��ܗ�Y���{�ص��pɫ�Ҝ������ޏ͏����w���������W���ܷ��Α���ȡ�����Mչ 2025-06-25
- ����W�₥���ڈF� Macromolecules�����ޏͿ���Û�������õ��x�ӌ��ˮ���z 2025-06-17
- �V����W�w�x�n�}�M CEJ �C�����ߏ������ޏ߷��Ӳ��ϵ��о��Mչ - �Cе�����c�ޏ�Ч�ʵ�ƽ�� 2025-06-12
- �A�ƴ��x���ڈF� ACS Nano�����ˮ���z���l�������������Ⲷ�@���������ڼ�����Ⱦ 2025-03-07
