
����mRNA�Ĺ���ȱ�ݣ�������������Ч�Ͱ�ȫ���f��ϵ�y��mRNA���g�đ������P��Ҫ��Ŀǰ���е��f��ϵ�y�У�֬�|�{���w��(LNPs)̎���R���D������ǰ�ء�Ȼ����LNPҲͬ�r�����������Է������y�Ԍ��F�ǸνM���f���Ȳ��㡣���֮�£����ھۺ����mRNA�f��ϵ�y�����`��Ļ��W�Y�������ڹ��ܻ��ă��ݣ����F���O��đ��Ý�����������Ŀǰ�ľۺ����f��ϵ�y���ڼ������Դ���DȾЧ�ʵ͵���K�����ؽ���Mһ�����M��
��֬������Ĥ�ͼ��������P�I�ɷ֣��ڼ����\ݔ;����������Ҫ���á������������ϵ���Ȼ����Ĥ�Ё��������ϵăȺ��w���ݣ��Ķ��˷���ǰ�{���d�w�����ơ������ھۺ����`��Ļ��W�Y��������֬�c�ۺ���Y�ϵõ�����֬���ۺ�����������@�ɷN���|���p���ݡ���֬β���x���˾ۺ������Ĥ������������x�Ӿۺ��{��֬���������ﰲȫ�Ե������������H��ˣ��ۺ�����ϵ��H��ˮ�ԡ�pKaֵ����������Ҳ�����`���{�����ԝM�㌍�H����

�D1. PLG-PPs�Ď�ľۺ����OӋ�ͻ��W�ϳ�·����
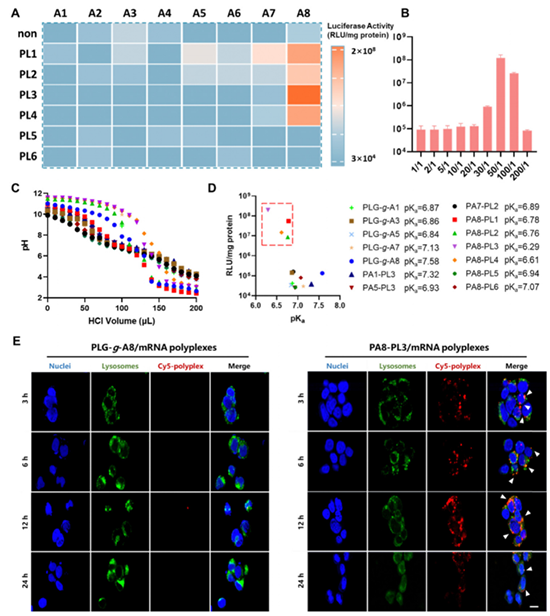
�D2. PLG-PP���ϵ��w��Y�x����C��

�D3. PLG-PPs/mRNA���w������ֲ���

�D4. PLG-PPs/mRNA���w���DȾ������
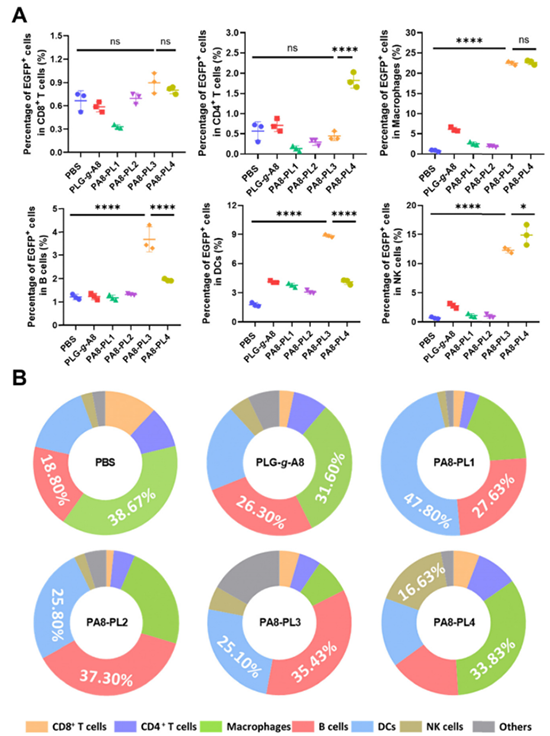
�D5. PLG-PPs/mRNA���w���DȾ������
���Y��
�����о��ɹ���������A polyamino acid-based phosphatidyl polymer library for in vivo mRNA delivery with spleen targeting ability�����}���l���ڡ�Materials Horizons���ϣ�DOI: 10.1039/d3mh02066e�����L�����û��W�о�����ʿ�о����w�h�������µĵ�һ���ߣ����fͨ�о��T��ꐌW˼Ժʿ��Փ�ĵĹ�ͬͨӍ���ߡ�ԓ�����õ��Ƽ�����������Ȼ�ƌW����ί������ʡ�ƌW���g�d���Ї��ƌWԺ���ꄓ�´��M�������fͨ�о��T����ٕ���ʮ�����T���Ȼ����֧�֡�
ԭ��朽ӣ�https://pubs.rsc.org/en/content/articlelanding/2024/mh/d3mh02066e
- �Ͼ����I��W�����ڡ���ɯ���ں��������аl���ɴ����۰�����ˮ���z���� 2019-11-01
- �п�Ժ�L��������ꐌW˼�о��Tϵ�y�u�����۹Ȱ����֦���Ҷ������[��ˎ�����ݔ��ϵ�y�ęC���c���� 2019-05-22
- �|�A��Wʷ��ꖽ����n�}�M�ھ۹Ȱ����s���{�����z���\��������ȡ�����Mչ 2018-04-17
- �A�|�������������/���������ڈF� Angew�����ٰ���mRNA�f�͆νM��Janus��֦�������d�w 2025-04-11
- �пƴ�������/����F� Nat. Biomed. Eng.: �OӋ������ԭ��mRNA�f���d�w���w���ؾ���������APC 2025-04-01
- ������W�̽�܊���ڈF� ACS Nano���U�֬�|�{���w����LNP����PEGylation����ڸ��KmRNA�f���еĘ�Ч�Pϵ 2025-02-05
- ɽ�|��W�������ڈF� ACS Nano: Ӳ�ȿ��{�ľ��Ҷ����{���w���{���{��-��������ã���������ˎ���f�� 2025-06-12
