�����߳�Ҋ(ji��n)�ć�(y��n)���R����(w��n)�}֮һ����ˎ��(x��)����Ⱦ�������w��(n��i)Ѫ��ˮƽ���m(x��)ƫ�ߣ����߹����ܓp���y����Ч������ڲ�λ�ļ�(x��)������(d��o)���������ܵ���Ⱦ����Ѫ�ǭh(hu��n)���鼚(x��)���ṩ�˸��������ֳ�ęC(j��)��(hu��)����(d��o)������?c��)������ߵĂ��ڱ����γ�ճ��������Ĥ��ʹ����y������ϵ�y(t��ng)�Ϳ�������������ڸ�Ѫ���h(hu��n)�������Ѫ��ȱ�ݺ���ˎ��(x��)���ďV����ֳ����Ⱦ�����ڵ��ί����R����(y��n)��������(zh��n)��
ᘌ�(du��)��������(zh��n)�����ִ�W(xu��)�֙�(qu��n)�F(tu��n)�(du��)�ͼ��ִ�W(xu��)������ڶ��t(y��)Ժ������������F(tu��n)�(du��)�����_(k��i)�l(f��)һ�N�����p�����Ե�������푑�(y��ng)��ˮ���z����ϵ�y(t��ng)��CGH����������Ч�ί������ͼ������ֽ��Sɫ���������MRSA����Ⱦ�Ă��ڲ����M(j��n)�������ϡ�ԓˮ���z���������|(zh��)�ᣨHA-ALD��ԭλ��(li��n)���~�{�״أ�CuNCs���ϳɵģ���ؓ(f��)�d����������ø��GOx����GOxø������ڲ�λ�^(gu��)���������ǣ��a(ch��n)�����������H2O2������(y��u)�����D����(y��ng)���������ء�pHֵ���͕�(hu��)���� CuNCs �� HA-ALD ֮�g������ã���ʹ CuNCsጷţ�ͨ�^(gu��)���D����(y��ng)����H2O2��(l��i)���a(ch��n)�������� (ROS)���@��(g��)�^(gu��)�̿���������ˎ��(x��)�������⣬CuNCs�x��ˮ���z��(y��u)���Č�(d��o)��ԣ��Ķ��܉�ͨ�^(gu��)늴̼���ES�����M(j��n)Ѫ���γɣ��Ķ����M(j��n)������?ch��)��ĽM���ޏ�(f��)���@�(xi��ng)�о��������_(k��i)�l(f��)�����Ͷ�܂�������ϵ�y(t��ng)�����m��(y��ng)��Ҏ(gu��)�t�Ă����Π���͂��ڃ�(n��i)��������ˮƽ���������m(x��)�ğo(w��)���h(hu��n)������ͨ�^(gu��)늴̼����M(j��n)Ѫ���γɡ�


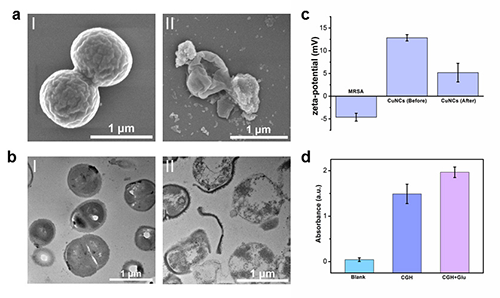
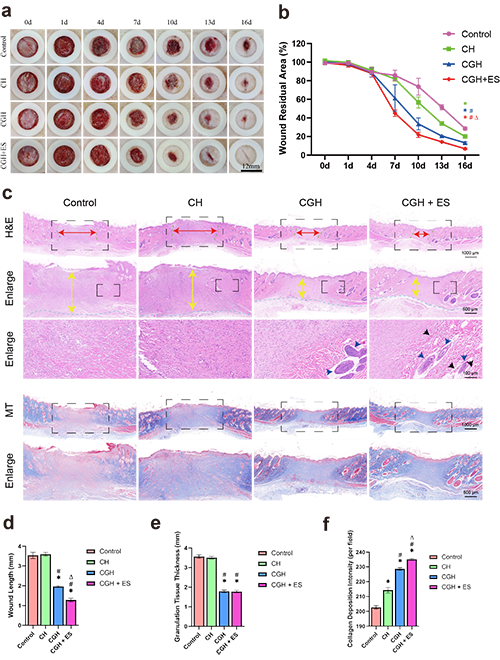
�D 3. CGHˮ���z�ڴ��M(j��n) �����ڸ�ȾMRSA������Ч����(a) TIDM�����Ⱦ���������^(gu��)���в�ͬ�r(sh��)�ڂ��ڵĴ�������Ƭ��(b) ���ښ�����e�ȵĶ����Y(ji��)����(c) H&E �� MassonȾɫ�Ĵ����ԈD��(d) HEȾɫ�y(c��)�������L(zh��ng)�ȡ�(e����ѿ�M����ȵĽy(t��ng)Ӌ(j��)��(sh��)��(j��)��(f���zԭ���e��ƽ���ɹ��ܶȡ�
ԭ��朽ӣ�https://doi.org/10.1016/j.cej.2024.150545
- ���������W(xu��)�����¡��S�؈F(tu��n)�(du��) AFM�����зӽY(ji��)��(g��u)�Ŀ�ע����Һ��ˮ���zָ��(d��o)�ɼ���(x��)������ - ���M(j��n)����ܻ֏�(f��) 2025-07-09
- �����ִ�Źٱ����ڡ������о��T�F(tu��n)�(du��) Nat. Commun.��̼���ۺ����c(di��n)�T��(d��o)�Y(ji��)����ȡ���{(di��o)�ؘ�(g��u)����(qi��ng)���͈�(ji��n)�gˮ���z 2025-07-07
- ��ɽ��W(xu��)�Ƕ�ؔ(c��i)/�S�ſ�/������/���x�F(tu��n)�(du��) Adv. Mater.�������L(zh��ng)�v���ԵĿ�ע����̿�{��øˮ���z��(sh��)�F(xi��n)�[���ąf(xi��)ͬ�ί� 2025-07-04
- �Ĵ���W(xu��)�A����ǻ�t(y��)Ժ��ٮٮ���о��T���n���������t(y��)�� ACS AMI���o�������w���������ݱ���Ķ��������ϵĿ������� 2025-05-06
- �����t(y��)ԺʯС�i���L(zh��ng)����W(xu��)�䛿� JCR�����г��m(x��)ጷų�������(qi��ng)�������ܲ����Ƃ������ϵ����ͳ���������Һˮ���z 2024-11-26
- ��h�������tɏ���ڈF(tu��n)�(du��) AHM����һʯ���B(ni��o)���� ���ڻǰ�����y�{(di��o)�صļ�߷�(w��n)���ԡ���(d��ng)�B(t��i)�ԺͿ����Ե�ˮ���z���ڸ�Ⱦ��(chu��ng)������ 2024-04-14
- ����f(w��n)�W(xu��)����ڈF(tu��n)�(du��)Nano Lett.�������|(zh��)ˮ���z늽��|(zh��)�~��Gɫ���õij���(j��)�����-����(qi��ng)��ȼ�ԡ��͜������ԡ���ճ�Ժ��L(zh��ng)ѭ�h(hu��n)��(w��n)���� 2024-10-01
�\(ch��ng)���P(gu��n)ע�߷��ӿƼ�

- CPHI����չ��(sh��)�(y��n)�҃x���c�O(sh��)��...
- ���ܹ��A��朆���������22��...
- ����(b��o)���C(j��)��(hu��)��500+ˎ��...
- ��(gu��)�HƷ�ơ�ǰ�ؕ�(hu��)�h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c(di��n)������...
- ��(gu��)�a(ch��n)������٣����(gu��)���^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��(hu��)
- �Ј�(ch��ng)��300�|��PMEC China ɫ...
- ����ע��(c��)��2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �Ĵ���W(xu��)���A���ڈF(tu��n)�(du��)��Adv....
- �Ĵ���W(xu��)���������ڈF(tu��n)�(du��) Ang...
- �A��������W(xu��)���ָ���ڈF(tu��n)�(du��)...
- �칤����x/�R�w�R/���ƽ� S...
- �A���r(n��ng)�����/������...
- �Ʊ��ҽ���/�֘s�I(y��)���ڈF(tu��n)�(du��)...
- ��ӿƴ����|��/�������F(tu��n)�(du��)...
- �A������������� Angew: ...
- �Ĵ���W(xu��)������ AFM������ʯ...
- ��۳��д�W(xu��)�����n�}�M CEJ...
- �Ї�(gu��)�ƴ����d���n�}�M���邐...