�������Լ�������������Ԫ�Y�����ܵ���ʧ�������J֪�ϵK����Ԫ���������z�|�������ʧ�⡣����ɭ������PD���ǵڶ���Ҋ����Ҫ�И��������Լ��������䳣Ҋ�������ˣ�����Ч�ί���Ȼ���˂��Pע�Ľ��c��PDͨ���Ժ��|�ͼy���w��Ͱ�����Ԫ��ȱʧ�ͼ�������-ͻ�|�˵��ף���-syn���ľۼ��������������漰��N;���͙C�ư����������������װY�������w�����ϵK��·���w���γɵȡ�ĿǰPD���ί���Ҫ��ه���{��(ji��)��Ͱ�ˮƽ��ˎ���đ�Aˎ�Ȱ������������Ɖĺ���X�̼������g���AҲ�������������Ȼ�������W��������Ѫ�X���Ϻ�ȱ������oˎϵ�y(t��ng)�����ƣ����g����Ҳ�������l(f��)�װY�͝����X�p�����L�U��
Ѫ�X���ϣ�BBB���Ǵ��X�ЄӑB(t��i)�Ҹ߶��x���ԵČ��w���ϣ����Ա��o���X����ѭ�h(hu��n)ѪҺ���ж����|��Ӱ푣��S���䷀(w��n)���ԡ�Ȼ����BBB�ı��o����ͬ��Ҳ�o�ί����X�����Ă��y(t��ng)ˎ������ش�����(zh��n)������BBB�Ĵ��ڣ������еĴ���Ӻ�98%��С�����M����X�ܵ��������ˣ��_�l(f��)�܉�BBB��ᘌ����X��׃��λ�oˎ���f��ϵ�y(t��ng)������Ч�ί��������Լ������P��Ҫ��
��PD�İl(f��)չ�^���У�BBB�������ԕ��ܵ��p���������u���ܼ��ľ��Ҷ�����ľ�����-����PAMAM��������ӱ��C���܉��^�ܓp��BBB��ͬ�r�����{��(ji��)С�z�|���������װYӰ푵ą^(q��)�l(f��)�]���Ϳ������ί����á����ט�����Ӳ��H���и߶ȷ�֧�����Q�ĽY���;�һ�ķ����������ں��е���Ԫ�ض����Ъ��ص�����W���ԣ��@ʾ�������f���d�w�ĝ����������ڵ��о��У���ͬ�����ĺ��ט�������ѱ���C����Ч������-synԭ�w�S���γɣ��������������-syn�ۼ����Ƅ��ĝ�����
�w�B���ף�FN����һ�N�Ƀɂ�����ͨ�^�����I�B�Ӷ��ɵĵ����|���V�������ڸ��N�M������������|���wҺ��ѪҺ�У����ж�N����W���ܡ�FN���ӹǼ��Ϻ��о�����-�ʰ���-�춬���ᣨRGD�����У�����������õ��װY����Ч����ǰ�ڹ����������Y�ϼ{���g��FN�İ����f�Ϳ�ͨ�^���M���ɼ���M2�͘O���Լ������������ְl(f��)�]FN�Ŀ��Ϳ��������ã�Biomacromolecules 2023, 24, 886-895��ACS Nano 2024, 18, 2195-2209; ACS Nano 2024, 18, 10625�C10641������ˣ��ٶ�ͨ�^�Y�Ͼ���ĩ���u���ĵʹ����ט�����Ӻ�FN�������B�ܓpѪ�X���ϲ���ְl(f��)�]���ߵ�����W�������Ķ�����PD���ί���

�D1. �Ƃ�AK123/FN NCs����(li��n)���ί�����ɭ����ʾ��D��ͨ�^�T��M2��С�z�|�����O�����������������������װY�����Լ�������-syn�ۼ��팍�F(li��n)���ί���

�D2.��A��FN�Ͳ�ͬ�|������AK123/FN NCs��ˮ�����W�ߴ硢��B��zeta늄ݺͣ�C��PDI����D��AK123/FN NCs��AK123/FN�|���Ȟ�4�r��TEM�D�����E���ߴ�ֲ�ֱ���D����F��BV2��������ͬ���AK123��AK123/FN̎��24 h��ļ�����������G����ʽ�����gֱ���D����H��BV2������PBS��FN��AK123/FN NCs̎��12 h��ğɹ⏊�ȶ�������I���A��̎����ͬ���Ƅ���BV2������AK123/FN NCs�ļ����zȡ;���u����
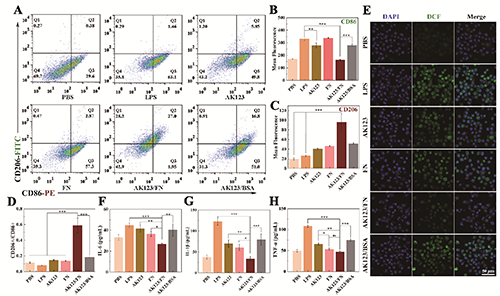
�D3.��A����ʽ�����g����AK123��FN��AK123/FN��AK123/BSA̎����LPS�����BV2������CD86��CD206�ı��_ˮƽ��BV2�����У�B��CD86�ͣ�C��CD206���_��ƽ���ɹ⏊�ȡ���D��CD206/CD86��ֵ����E����ͬ���Ϸ���24 h��BV2������ROS��CLSM�D��ͬ����̎����LPS�����BV2�����У�F��IL-6����G��IL-1���ͣ�H��TNF-�����_��ELISA������

�D4.��A����β�o�}ע�䲻ͬ���Ϻ�0.5��1��2��4��6 h����С���M�Пɹ����B��AK123/FN-Cy5.5 NCs��C��FN-Cy5.5ע���6 hС����Ҫ���ٺʹ��X���x�w�ɹ����D���քe��ע��FN-Cy5.5��AK123/FN-Cy5.5 NCs��6 hС����Ҫ���ٺʹ��X��ƽ���ɹ⏊�ȡ�ͨ�^�ɹ����y��ע���6 h��12 h��3���5�죨E����Ҫ���ٺͣ�F���X��AK123/FN NCs������ֲ���

�D5.��A��PDС����ί��͜yԇ�r�g����ʾ��D����B�����D��ƣ�ڃx�yԇ��С�������D���ĕr�g����C�������yԇ�еķ�ֵ��������D����β�yԇ�еIJ��ӕr�g����E��������Ӿ�yԇ�е�Ư���r�g�ͣ�F�����U�yԇ�еĿ��r�g����G���������в�ͬ�M��С��Ĵ�����·���ͣ�H���r�g��D����I�����ą^(q��)�ĕr�g�ٷֱȣ���J��ƽ���ٶȣ���K�����ӕr�g�ٷֱ��Լ���L���~���^(q��)�档

�D6.��A���X�ͺ��RCA1�^(q��)H&EȾɫ�D�����ԪNisslȾɫ����B����ͬ�MС��y���wGFAP����-syn�����ߟɹ�Ⱦɫ�ͣ�C����-syn�������ɹ⏊�ȡ���D��CD206+/CD86+�����ɹ⏊�ȱ�ֵ����E��TH�������ɹ⏊�Ⱥͣ�F����ͬ�MС����X�ж�Ͱ�������ˮƽ��
������֮���о��F����Ƃ��AK123/FN NCs��������(y��u)�ݣ�1�����Ƃ�����ˮ��Һ���ஔ��(w��n)������ɢ�����ã�FN�j�Ͽ���Ч���AK123��ˮ��ɢ�ԣ�2��AK123/FN NCs���ژ������ĩ�˵��u�����Դ��^�ܓpBBB������������ͨ�^FN��RGD���а�����_�����ص�С�z�|��������FN��AK123�����f�����XPD��׃��λ��3��AK123/FN NCs��ͨ�^(li��n)�ϵĿ��Ϳ��������ã����MС�z�|������M1��M2���͵ĘO��������NF-��B��̖ͨ·�Ԝp���װY���ӱ��_��������-syn�ľۼ����Ķ��l(f��)�]�f(xi��)ͬ�ί�PD�����á�ԓ�F꠵��о���PD�ί��ṩ��һ�Nȫ�µķ����@�����ί������������Լ����еõ����á�
����朽ӣ�https://doi.org/10.1016/j.bioactmat.2024.04.005
- �|�A��W�������о��T/ʷ��ꖽ��ڈFꠣ������Q���ט�������f�Ͳ��}����ø���ڹ��P��(ji��)�Ŀ���ܛ�DZ��o�ί� 2025-06-13
- �|�A��W������/ʷ��ꖈFꠡ�Acta Biomater.�������ט�����ӽ錧������V�����څf(xi��)ͬ���[������ί��c��������� 2025-04-28
- �|�A��Wʷ��ꖽ��ڈF� Nano Today�����ں��ט�����ӵ�ˎ���f��ϵ�y(t��ng)�f(xi��)ͬ�������ɡ����Ϳ������ί������ĺ�Ĭ�Y 2025-02-11
- ���������ڈF� Bioact. Mater.����ˎ���f��ϵ�y(t��ng)"������-����-����ϵ�y(t��ng)���o"��λһ�w�f(xi��)ͬ����ʹ�L���P��(ji��)���ί� 2025-06-04
- �����t(y��)���ǻ�t(y��)Ժ�Մ�/�贺��/����Fꠣ�����ROS�|�l(f��)ˎ��ጷ����ԵĿ�ע��ˮ���z���F�������Ϳ��{���w���f(xi��)ͬ�f�������������ί� 2025-04-15
- �A�S��Wꐐ������Ϸ��t(y��)�����f Compos. Part B������dECM���̻��M���f(xi��)ͬ�����ֻ��Ϳ������ô��M���P��(ji��)��ܛ������ 2024-12-13
- �|�A��Wʷ��ꖽ��ڈFꠣ������w������푑��Ԙ�����Ӽ{�����z�Ɍ��F���ԷΓp���������{��(ji��)�Ϳ�����(li��n)���ί� 2025-05-15
