�����صIJ�Ҏ��ʹ�Ì�����ˎ�����ӿ�F����ˣ��аl�ǿ����ؿ�����������ü�ޡ�������Ԛ��w�������⣨O2����һ��������NO����һ����̼��CO�����ѱ��_�l���ڿ����ί���NO�cCO�܉���һ�������ֱ�Ӛ�������O2�t��ͨ�^�γɆξ��B����1O2�����F������Ȼ�������w�ί��ڕr���ϵIJ��ɿ��ԇ����Ƽs���䚢��Ч����ͬ�r������������ɓp����
�����衱�������Գɞ��Q�������}����Ч;�����F�еġ����衱����������Ҫ���ڼ�����Ⱦ�h��������߀ԭ��B��pH���ضȡ�ø���M���OӋ��Ȼ�����@Щ������Ⱦ�h���������B���ܺܺõ��P������Ⱦ�ij̶ȣ��������ھ��_�{�ؚ��wጷż����m����Ч�����������ڵļ��������أ�Pore-forming toxins, PFTs���ڼ�����Ⱦ���M���а�����Ҫ��ɫ���Ǽ���������������Ҫ��������֮һ����PFTs����c������Ⱦ�M�̳��^�õ������P����ˣ����ü������ڵ�PFTs�{�ؚ��wጷŏĶ��{�ع��ί�Ч���ɞ��µ����ܿ������ԡ�

���ڴˣ������t�ƴ�W���ٵڶ��tԺ�һ���о��T���x�f�����Ϝ����t�ƴ�Wˎ�WԺ�w�������ڡ�ꐉ�����ʿ����������һ�N����PFTs����푑��ͷ����{�ך��ݣ�RBC(IR780)-PFC����ԓ�{�ך����ɼt����Ĥ�������t�����IR780�͚��w�d�wȫ����̼��PFC��������ʹ��ǰ�����������⣨RBC(IR780)-PFC(O2)�����Y���@ʾ��ԓ�{�ך����܉�������N�²����������ͼ������ֽ��Sɫ�������MRSA����˹�ؾ�LM��������Ѫ������GAS�����ڵ�PFTs������PFTs�܉��ڼ{�ך��ݱ����ף����M�Ȳ�O2��IR780ጷţ����ڽ��t��NIR�����®a���������壨ROS�����l�]���������Ч�����@��һ�N���ص������衱�������ԣ�����ͬһ�����{�ך��������£���ȾԽ���ء������۷eԽ�ࡢጷ�O2��IR780ҲԽ�ߣ���NIR���������®a����ROSҲԽ�࣬����Ч��ҲԽ�á�����˼���ǣ��о��Fꠘ������d�wҲ���ܽ�NO�γ�RBC(IR780)-PFC(NO)��ͬ��������PFTs�{��NO��ֱ�Ӛ���Ч�������о������������к��c�{�ع�����ί��ЙC�Y�����������҂�ͨ���J�鼚����Ⱦ�^���е����к��¼���������ͬ�r�����D���ɿ���Ч���ġ������¼������������õ��R�������ί�ǰ����

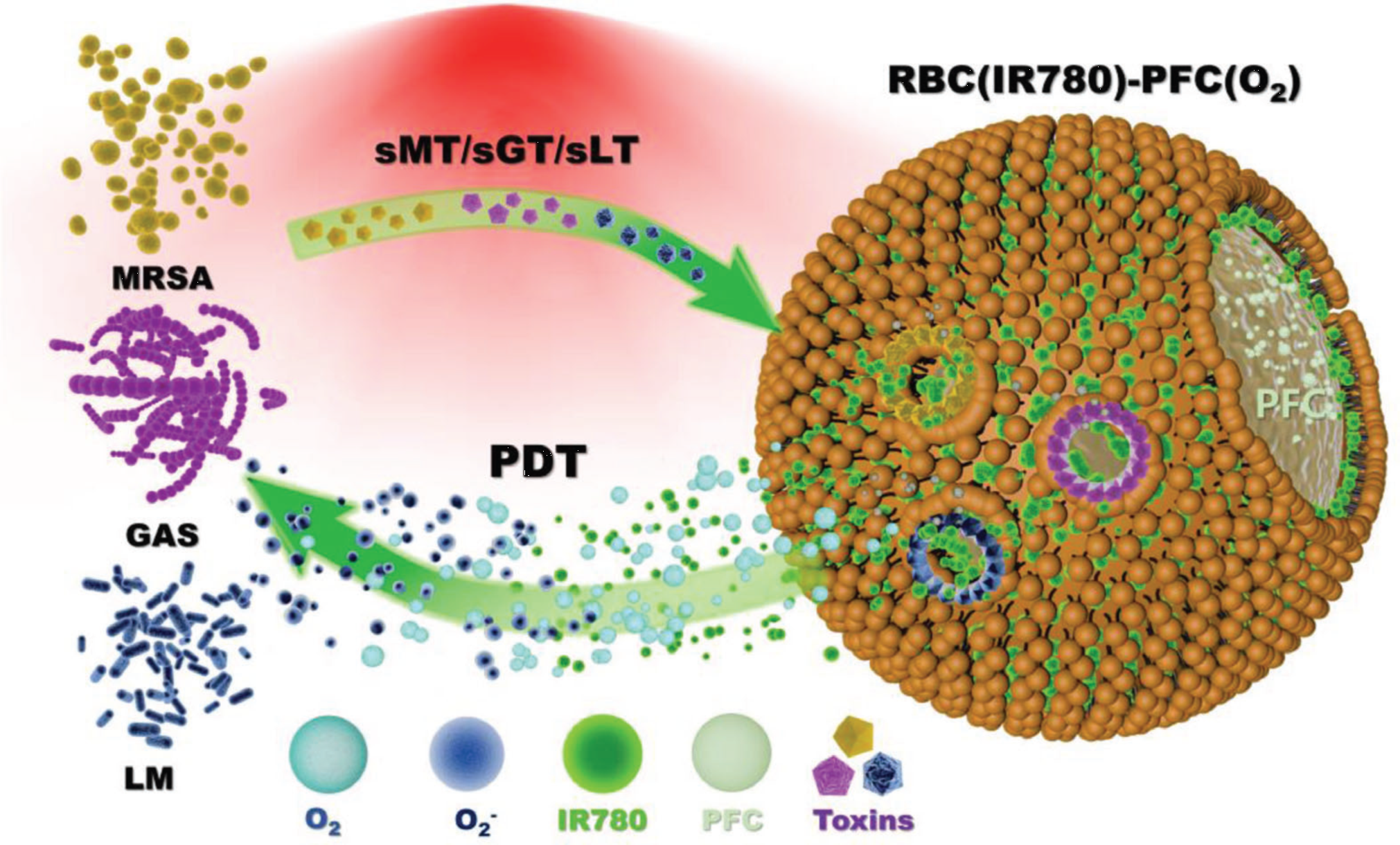
�D1. �����{�������ڰ��������ί�������Ⱦ
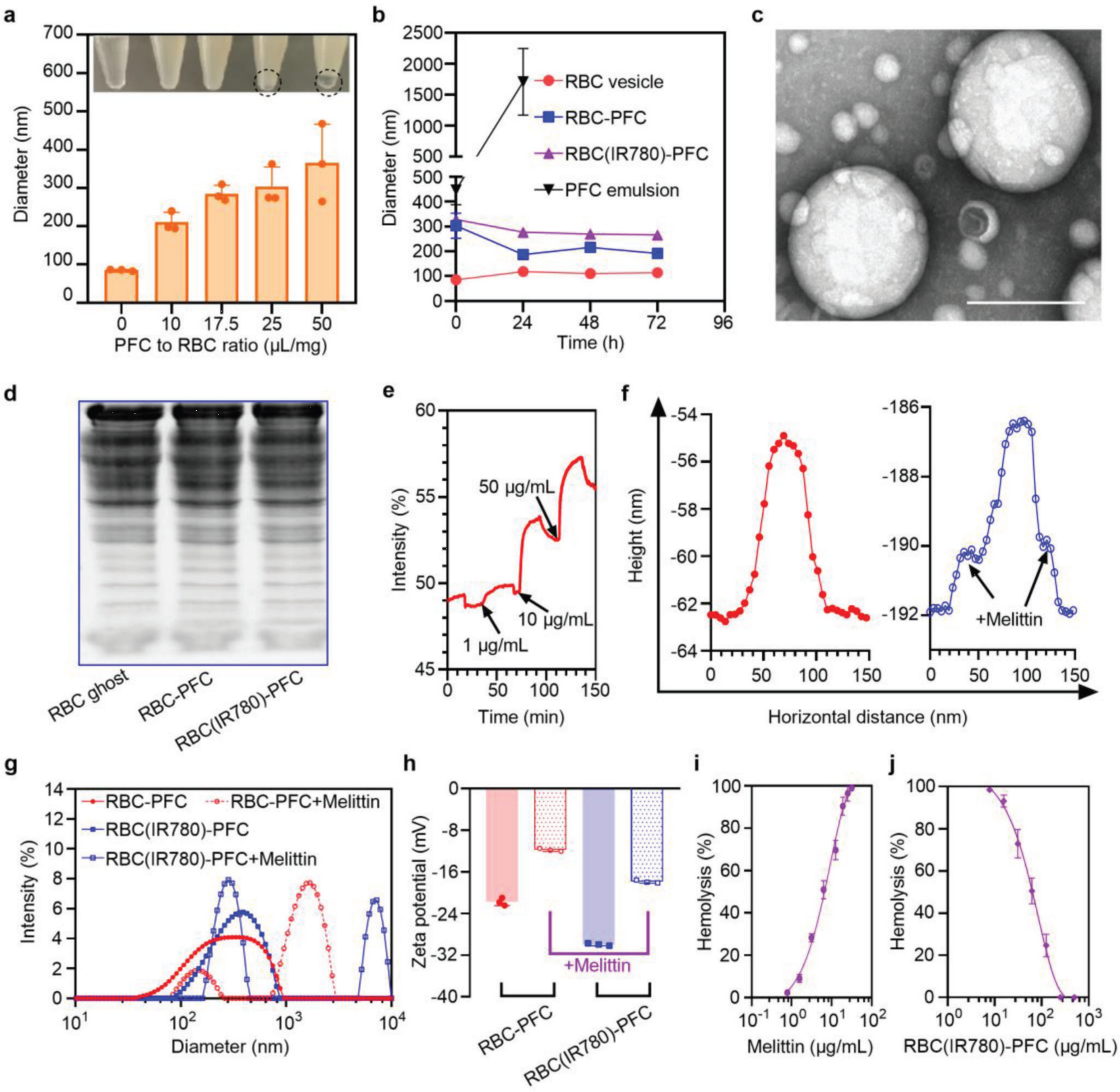
�D2. RBC(IR780)-PFC���Ƃ��c����

�D3. ��������������RBC(IR780)-PFC(O2) ���������������

�D4. PFTs ���MNO��RBC(IR780)-PFC(NO)��ጷŲ���������Ч��
ԭ��朽ӣ�https://onlinelibrary.wiley.com/doi/10.1002/adhm.202200698
