
����һ�����M�����������ޏͺ������Ĺ��������١��Ʉ������\�ӓp������������ɵĹ�ܛ�Ǔp�����漰�P��ܛ�Ǻ�ܛ���¹ǽM�������^�˹ǽM���������ޏ������������������ϣ�����Ӱ��P����������ӣ����H�o������ɾ�Ľ���������ؓ�����o����������صĽ���ؓ������һ험O�������Ե��R�����}��Ĥ�ȹǻ���Intramembranous ossification��IMO����ܛ�ǃȹǻ���Endochondral ossification��ECO���ǹ�������̥�l����ȱ�p�ޏ������ăɗl;����Ŀǰ�����ί���ȱ�p�����������Ҫͨ�^ IMO ���F�ɹ��ޏͣ�������Ѫ�ܻ��y�Խ��������¹����� �������Ĺǰl������W���R���Ƕȁ��v�����w�����l������������Ҫͨ�^ ECO �M�С�ECO ͨ�^�g���|�ɼ����ۼ��ɈF���ֻ���ܛ�Ǽ��������m����ȱ�p̎�����͵�Ѫ���ľֲ��h�������Mһ����ֳ�����ʴ�ܛ�Ǽ���������Ѫ�܃�Ƥ���L���ӣ�vascular endothelial growth factor��VEGF���T��Ѫ�������Q�ɹ����ą^��Ѫ������Ć��}����K�D����ɹǼ������ڹǻ��|�ޏ�ȱ�p����ˣ�����ECO �������������һ�N������Ĺ�ȱ�p�ޏͲ��ԡ����ǣ����R��������Ȼ������ ECO ���s�ļ����О���^�L���w�⼚���T�����ڡ�
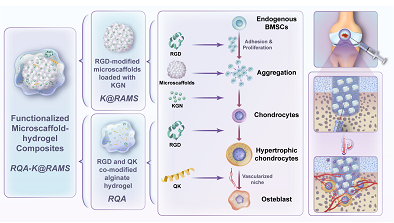
�D1. ���ܻ�֧��ˮ���z�ͺ��wϵ�{�ظɼ���ܛ�ǃȹǻ��О��ޏ�ܛ��ȱ�pʾ��D
�������c��

�D2. RQA-K@RAMS ����������
��2�����ܻ�֧��ˮ���zȫ�A���{�ز����� hBMSCs ܛ�ǃȹǻ��О���RGD �������֧��������^��ıȱ���e�� 3D ��Y�������جF��������ֳ���ۼ��О飬���������ڼ������ⲿ�h���M�����|���Q��ˮ���z�Ӳ���������֧�ܱ���ļ�����ʧ��ע���^��������Б������µļ����p�������Ҟ鼚���ṩ��ճ�����h�����Mһ�������˼�����𤸽���ۼ��О飬����������ܛ�Ǽ�����ֳ�ͷʴ��ܻ�֧��ˮ���zͨ�^����ጷ� KGN���� hBMSCs ܛ����ֻ��ṩ���m������ܛ���T���h�����γɸ����ܛ�ǻ��|�Mһ�����M��ܛ�Ǽ��� �ʴ�QK �������w����ֲ�rͨ�^��ļѪ�܃�Ƥ�����γ������ڷʴ�ܛ�Ǽ�����ɹǼ����D����Ѫ���h�������о�ͨ�^���ӷN�ڹ��ܻ�֧��ˮ���z�� hBMSCs ���M���w��ܛ�ǃȹǻ� 5 �ܵ��T�����l�F�w��ܛ���T�� 2 �ܾ����^�ߵ� COL10A1 �ı��_������ͨ�^����Ƥ�®�λ�ɹnj��l�F�w��ܛ���T�� 2 ��չʾ���˺��w��ܛ���T�� 3 �ܷʴ� 2 �ܵļ���-֧�ͺ��w����ijɹǵV����Ѫ����ļ�����������҂��������Ĺ��ܻ��������c֧��ˮ���zͨ�^�{�ؼ���ܛ�ǃȹǻ��О飬�����@��������ܛ�ǃȹǻ��M�̣�����ֲ���w�Ⱥ���F�����õijɹǵV����Ѫ����ļ������



�D5. ����Ƥ�®�λ�ɹnj��


�D7. ���ܻ�֧��ˮ���z���M��ϥ�P����ܛ��ȱ�p��ܛ���¹nj��ޏ�
ԭ��朽ӣ�https://doi.org/10.1021/acsami.2c12694
- ����W���ďV���ں��п�Ժ���L호��о��T: ֱ��3D��ӡ�ߏ����s���ݶ�ˮ���z֧�����ڹ�ܛ���ޏ� 2018-01-19
- �K�ݴ�W���f���ں��T���鸱�о��T�Fꠡ�Mater. Today�����ڷ��Ҵ������ΰ�������ί� 2022-04-09
- �Ї����|��W����h���ķ������n�}�M�ڔUչ�p�W�j��ˮ���z������ȡ�����Mչ 2020-11-30
- �Ͻ������/������ꐝh�x���������cˮ���z�{�����ɼ���Ƥ�w���� 2020-07-29
