��(d��o)�°��Y�ί�ʧ������Ҫԭ��֮һ���[����(x��)��ͨ�^Ѫ�ܺ��ܰܵďV���D(zhu��n)�ơ���������[��Ѫ������������ί���PTT���������ί����²����ڰ��Y�ί���ȡ�����@���M(j��n)չ��Ȼ�����@Щ��һ���ί�ģʽ���ڟo��������ԭ�l(f��)���[�����L��ͬ�r�����[���D(zhu��n)�ƣ���Ч�����M�����⡣�_�l(f��)�܉�ͬ�r�����[�����L���D(zhu��n)�Ƶļ{��ƽ�_��Ȼ��һ����(y��n)��������(zh��n)��
��Ѫ�������5��6-�����S����-4-���ᣨDMXAA���������Ѫ�������mȻ�܉������[�����ĽM����Ѫ�ԉ�������������ϵ�y(t��ng)�������ԟo����Ч�����������w�[�����b��PTT������Ч�����[��������(x��)��������PTT�T��(d��o)������ԭ�Լ�(x��)��������DMXAA�������{(di��o)��(ji��)���ÿ��ܹ�ͬ�����w��(n��i)���[������푑�(y��ng)����PTT�cѪ�������Y(ji��)�Ͽ�����һ�N����(qi��ng)�һ��a(b��)�IJ��ԡ�
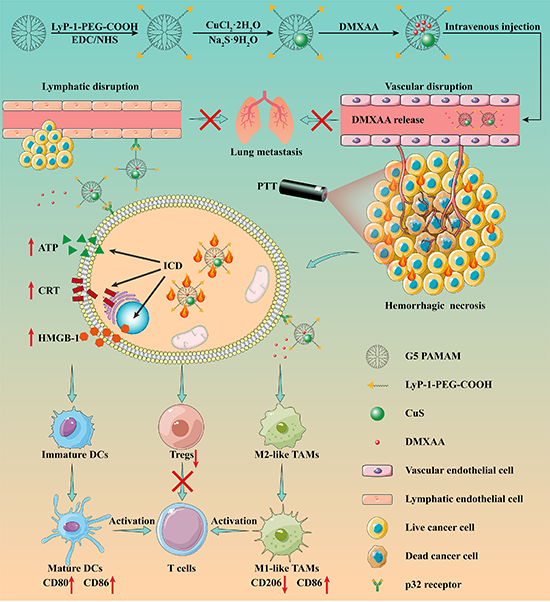
���ڣ��|�A��W(xu��)��ѩ�㸱�о��T/ʷ��ꖽ����F(tu��n)���(g��u)����һ�N�����͘�����Ӽ{��ƽ�_���������{(di��o)��(ji��)�錧(d��o)��(li��n)�Ϲ��/Ѫ���������о��F(tu��n)������ڵ����������-��������ӵı�������Ҷ������İ�����LyP-1�������Ⱥ������(n��i)����ǻ��ؓ(f��)�d���~�{���w����CuS NPs����DMXAA���õ������͘�����Ӽ{��ƽ�_G5-PEG-LyP-1-CuS-DMXAA NPs��GLCD NPs�����D1����
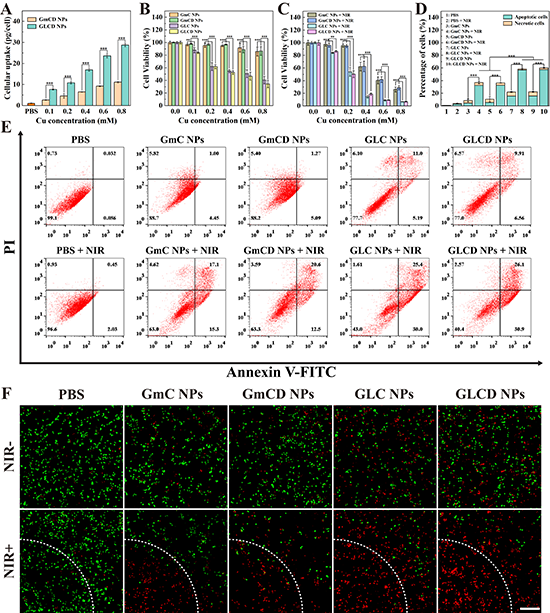
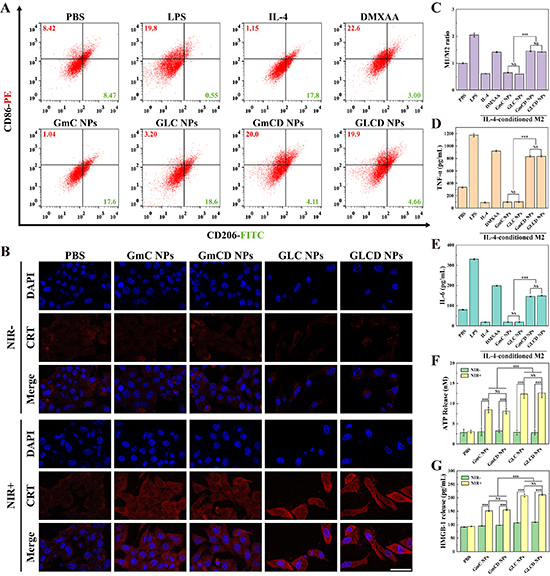
���ϱ����Y(ji��)�����������ϳɵ�GLCD NPs�ߴ��һ���������õĆη�ɢ�ԡ��z�w��(w��n)���ԡ���᷀(w��n)���ԡ��߹���D(zhu��n)�QЧ�ʣ�59.3%����pH���е�ˎ��ጷ����ܣ��D2�����w�⼚(x��)�����Y(ji��)��������GLCD NPs���Ѓ�(y��u)�����w�������������������������������������D3��4�����w��(n��i)����Y(ji��)��������GLCD NPs����ͨ�^����PTT�����[����ͬ�r�Ɖ��[��Ѫ�ܺ��ܰ��Է�ֹ���D(zhu��n)�ƣ�PTT�T��(d��o)������ԭ�Լ�(x��)��������DMXAA�錧(d��o)�������{(di��o)��(ji��)���w��(n��i)�f(xi��)ͬ�����˿��[������푑�(y��ng)���D5��6����



�D6 ��(j��ng)�^��ͬ�ί����2���[����Ƭ�ģ�A��CD31Ⱦɫ�ͣ�B��LYVE-1Ⱦɫ����(bi��o)�ߞ�100 ��m����C����(j��ng)�^��ͬ�ί����18��С��β�����Ƭ�ͣ�D������(y��ng)��H&EȾɫ����(bi��o)�ߞ�5 mm��
Փ��朽ӣ�https://doi.org/10.1002/smll.202301914
- ���A�x�m(x��)�������n�}�M ACS Nano����MXene�{��Ƭ���M(j��n)��(g��u)���ĸߏ�(qi��ng)�g�������졢�ߌ�(d��o)늺������Ͷ����I�W(w��ng)�j(lu��)����ˮ���z 2021-12-30
- ����������������Ռ�(d��o)늸߷��Ӽ{��(f��)�ϲ����c늴̼������T��(d��o)�M�����������g(sh��)�@��Ҫ�M(j��n)չ 2011-07-29
- �|�A��W(xu��)�������о��T/ʷ��ꖽ��ڈF(tu��n)ꠣ������Q���ט�������f�Ͳ��}����ø���ڹ��P(gu��n)��(ji��)�Ŀ���ܛ�DZ��o(h��)�ί� 2025-06-13
- �|�A��W(xu��)ʷ��ꖽ��ڈF(tu��n)ꠣ������w������푑�(y��ng)�Ԙ�����Ӽ{�����z�Ɍ��F(xi��n)���ԷΓp���������{(di��o)��(ji��)�Ϳ�����(li��n)���ί� 2025-05-15
- �|�A��W(xu��)������/ʷ��ꖈF(tu��n)ꠡ�Acta Biomater.�������ט�����ӽ錧(d��o)������V�����څf(xi��)ͬ���[������ί��c��������� 2025-04-28
- �|�ϴ�W(xu��)�����۽��ڈF(tu��n)� CEJ �C�������������{(di��o)��(ji��)���ԵĹ��̻��z���ڰ��Y���װY�����������еđ�(y��ng)�� 2025-04-09
- �Ĵ���W(xu��)��ٮٮ���о��T�����˸����ڡ����ڿƽ��� CEJ�������l(f��)�Ĺ��̻���������������Ϳ�����ڿ�ֲ���w��Ⱦ�������{(di��o)��(ji��) 2024-12-30
�\���P(gu��n)ע�߷��ӿƼ�

- ���ܹ��A��朆���������22��...
- �������C(j��)����500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ��h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��
- �Ј���300�|��PMEC China ɫ...
- ����ע�ԣ�2025����������չ...
- ���a���υ��^�A(y��)��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ(x��n)����...
- �㽭��W(xu��)�Ǿ�܊���������F(tu��n)�...
- �����ִ�Źٱ����ڡ�������...
- �п�Ժ�{����Դ�����ܡ�����...
- �V�t(y��)��Ժ���١��V���T��ܰ N...
- �������i�w/���������...
- ����炐�ȁ���W(xu��)���h����...
- ����������W(xu��)���s�����i�w...
- �Ї��ƴ���Ƙ�/�uꐈF(tu��n)� JA...
- �Ͽƴ��N�x�F(tu��n)� Nat. Comm...
- �Ͼ���W(xu��)�����ڡ����ı� PNA...
- �Ĵ���W(xu��)����/����|�F(tu��n)ꠣ�...