���ԷΓp����ALI��ͨ���Ժ������ȡ�����Ѫ�Y���װY�Ŀ��ٰl(f��)�������������Ʉ�(chu��ng)������Ⱦ��ȫ���Լ������l(f��)�����y(t��ng)�ί�������Ҫ��ه֧�����o����Cеͨ������������@Щ�������ھ������ҟo�����������ړp����λ���M��ˎ���ί�����ALI�ί��ĺ����ֶΣ������R�����ó������ö����ޡ������������俹�����Ϳ������Ԃ����P(gu��n)ע�������R���������R�ش�����(zh��n)����ҪԴ���������öȵ��T���ڷ����ղ��θ�c�����K�д��xѸ�٣������w��(n��i)��Ч��Ƚ��͡����⣬�h(hu��n)�����أ���pHֵ���ضȺ�ø�����ã����ƉĶ�ӵķ�(w��n)���ԣ��Mһ�������䯟Ч���߄������߀�������l(f��)�ζ��ԡ��I���Ի��c����ˎ��a(ch��n)��������������ˣ��O(sh��)Ӌ���m�İ����d�w�Ը��ƶ���ˎ����������ö��c��(w��n)���ԣ����������ALI�ί��еĝ������P(gu��n)��Ҫ��
��ͻ���������ƣ��{���dˎϵ�y(t��ng)���_�l(f��)�ɞ��о����c�����y(t��ng)���Ƃ似�g(sh��)�����܄��]�l(f��)������Һ�ۺϷ������ڹ�ˇȱ�����܄������������������dˎЧ�ʵͼ�ͻ�Ч�����@�����֮�£�늇��F���g(sh��)�{�辫��늈��{(di��o)�ؿ��Ƃ�������һ���Y(ji��)��(g��u)�ɿص��dˎ����͜ؼӹ����������m���ڟ�����ˎ�����ͬ�S������g(sh��)��(g��u)���ĺ˚����H��ͨ�^��϶���{(di��o)�،��F(xi��n)�L�_��(sh��)�ܵľ�ጣ�߀�����ñ��湦�ܻ�������w�B����Ϳ�ӣ��x�財������������@�������β�ˎ����eЧ�ʡ�
�������ᘌ�ALI�о��ɼ����O��ʧ����P(gu��n)�I�C�ƣ��о���ʾ������Ե��ף����w�B����FN����ͨ�^��������̖ͨ·�(q��)��M2�Ϳ��ױ����D(zhu��n)�����c����ˎ��Ŀ����������γɻ��a���@һ�l(f��)�F(xi��n)���O(sh��)Ӌ��ܼ{���d�w�ṩ����Ҫ��ʾ��ͨ�^���g�ָ�ؓ�d��ͬ���Գɷ������˚��Y(ji��)��(g��u)�����@�N�dˎ��ʽ�ȿɱ�������g����Ì��µ�ʧ����܌��F(xi��n)���λ�ij���ጷš����⣬��Ч�{(di��o)����TNF-����IL-1����IL-6�ȴ����������^�ȷ��ڞ�������"���������L��"�����װY�Լ����ί����P(gu��n)�I�h(hu��n)��(ji��)���@Щ�������ӵ��^���a(ch��n)�����ӄ��װY��(li��n)���������܌��¶����ٓp����������

�D1��RPG@FN����Ƃ估����ALI�е��ί��C��ʾ��D��

�D2����A�����Ş�ɹ�̽ᘜy����PCL-PEG�z���R���z����ȣ�CMC������B�����xRes��PCL-PEG/Res��RPG��RPG@BSA��RPG@FN�����w���W�ߴ�ͣ�C��Zeta�λ����D��RPG@FN�Ē�����R��SEM���D��E�������ֲ�ֱ���D����F��FN��RPG@FN��BSA��RPG@BSA��RPG��SDS-PAGE����������G��RPG@FN��ɢ��ˮ��PBS��10%̥ţѪ�壨FBS����RPMI-1640���B(y��ng)���в�ͬ�r�g�ε����w���W�ߴ�׃������H��RPG��RPG@BSA��RPG@FN��PBS�е�Res�۷eጷ���������I��RPG��RPG@BSA��RPG@FN��37 ��C PBS�г��m(x��)8�ܵ��w�⽵���������D��B������C������G-I���Ќ���؏�3�Σ�n=3����"ns"��ʾ�o�y(t��ng)Ӌ�W���

�D3 ��A����ͬ���Res��PCL-PEG/Res��RPG@FN̎��MH-S����24С�r��������n = 6������B��PBS��FN��RPG@FN̎��MH-S����12С�r��ğɹ⏊�ȼ���C������������n = 3������D��RGD�A���]̎�팦RPG@FN����MH-S�����ğɹ⏊��Ӱ푶���������n = 3����C-D�D��FN��(j��ng)Cy5.5��ӛ����E����ͬ����̎��12С�r��DCFH-DA̽ᘙz�yMH-S������������ROS���ğɹ⏊�ȼ���F������������n = 3������G��LPS�����MH-S�����cRes��FN��RPG@BSA��RPG@FN������6С�r��DCFH-DAȾɫ��Ĺ��۽���������@�R��CLSM���D�˳ߣ�40 ��m������H��JC-1�ɹ�̽ᘙz�y��ͬ����̎����MH-S���������wĤ�λ��MMP������ʽ�����g(sh��)������C-D��F�D��***��ʾp < 0.001��

�D4����A����ͬ̎���MMH-S����CD86�cCD206���_ˮƽ����ʽ�����g(sh��)��������B��CD206����c��C��CD86��Ծ��ɼ��������y(t��ng)Ӌ����D��TNF-������E��IL-6����F��IL-1������G��IL-10�ڼ�����(n��i)�ı��_ˮƽ��24С�r̎��������H���������B(y��ng)Һ��һ��������NO����șz�y����I�������|(zh��)ӡ�E��WB��������ͬ̎���MMH-S������NF-��B�c���ữAkt��p-Akt���ı��_ˮƽ��I�M��PBS��II�M��LPS��III�M��Res��IV�M��FN��V�M��RPG@BSA��VI�M��RPG@FN�����D��B-H���Ќ���؏�3�Σ�n = 3����*��ʾp < 0.05��***��ʾp < 0.001��
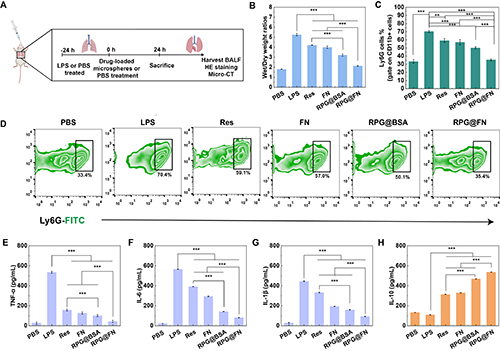
�D5����A��ALIС���w��(n��i)�����ί�ʾ��D����B����ͬ̎���MALIС��νM������رȡ���C�����MС��νM��������������������D����ͬ̎��24С�r��νM��������������ʽ�����g(sh��)�c�D����E-H��֧��ܷ��ݹ�ϴҺ��BALF���д������ӣ�TNF-����IL-6��IL-1�����c�������ӣ�IL-10��ˮƽ�z�y���D��B-C������E-H���Ќ���؏�3�Σ�n = 3����**��ʾp < 0.01��***��ʾp < 0.001��
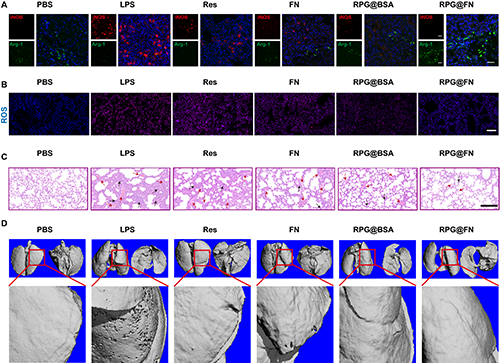
�D6����A��ͨ�^���ߟɹ�Ⱦɫ�u����ͬ̎���MALIС��νM�����ɼ����O����B(t��i)���{ɫ��DAPI��Ⱦɫ���Gɫ��M2�͘�ӛ��Arg-1���tɫ��M1�͘�ӛ��iNOS������B�����MALIС��νM����������ROS�����Ч�����˳ߣ�100 ��m������C���νM��H&EȾɫ��Ƭ����D��Micro-CT����Y(ji��)�����DC�мtɫ�c��ɫ���^�քeָʾ���ݱڳ�Ѫ���װY���������^(q��)�˳ߣ�200 ��m����
������֮�����о�����ͬ�S������g(sh��)�_�l(f��)��һ�N�˚��Y(ji��)��(g��u)���fˎϵ�y(t��ng)��RPG@FN��������ALI�ĸ�Ч�ί���ԓϵ�y(t��ng)��(n��i)����ؓ�dRes��PCL-PEG�z����(g��u)�ɣ��⚤��PLGA�������������(j��ng)FN�������ͨ�^ϵ�y(t��ng)����RPG@FN��������ò����(w��n)���ԡ�ˎ��ጷż��������ܣ��C����Y(ji��)��(g��u)�����ԡ��w�⌍���C��ԓ�wϵ�����ROS�����MM2�;��ɼ����O�����֏;����wĤ�λ���{(di��o)���װY���ӵȷ���Ŀ����������ԡ��Mһ��ͨ�^ALIС��ģ���w��(n��i)����u�����ί�Ч����RPG@FN��ă�(y��u)����ҪԴ���������c����1������늇����g(sh��)��(g��u)���ĺ˚������dˎ�z�����(n��i)�ˣ��Ɍ��F(xi��n)�β��LЧ��ጣ���2���@������Res�cFN���������öȣ������併��ʧ���3��FN����x�����װY���ɼ��������ԣ�ͨ�^ROS����cM2�O���p�ؙC�ƣ��f(xi��)ͬ�֏;����w��(w��n)�B(t��i)�����NF-��B/PI3K-Akt��̖ͨ·��
����朽ӣ�https://doi.org/10.1016/j.jcis.2025.01.249
- �҇��l(f��)��������ٙz�y�·��� 2009-11-10
- �����|(zh��)�ǹ��r�ͺ����늇��F�|(zh��)�V(ESI-MS)�о� 2004-06-02
- �|�A��W�������о��T/ʷ��ꖽ��ڈFꠣ��~���s�Ӡ��p���ٚ������ﹲ�f�͵���/ˎ���{(di��o)���[���p�ش��x���F(xi��n)��(li��n)�Ļ��W�����W/�����ί� 2025-02-08
- �|�A��W������/ʷ���Biomaterials������������Եĺ��ט�����ӹ��f�͵����|(zh��)/ˎ�����ھ��ɼ����ؾ����������P(gu��n)��(ji��)���ί� 2024-12-09
- �|�A��W��ѩ��/ʷ��ꖈF� AHM�����������������Ǽ{�����z���f��ˎ��ͻ���?q��)��F(xi��n)�D(zhu��n)����ǰ���ٰ��ĸ�Ч�ί� 2024-04-30
- �|�A��Wʷ��ꖽ��ڈF� BAM����������������Ե��u�������ט�������X��(n��i)�f���w�B���ׅf(xi��)ͬ�{(di��o)��(ji��)С�z�|(zh��)�������F(xi��n)����ɭ���������ί� 2024-04-26
- �|�A��Wʷ��ꖽ��ڈFꠡ�ACS Nano�����w�B���װ����ĺ��ט�����Ӽ{���w��ͨ�^�����{(di��o)��(ji��)���h(hu��n)���������P(gu��n)��(ji��)���ί� 2024-04-05
�\���P(gu��n)ע�߷��ӿƼ�

- �������C����500+ˎ��...
- ���HƷ�ơ�ǰ�ؕ��h�cչλ�D...
- ������AI�ǿء���Ч�����x��...
- 2025�ؑc����չ���c������...
- ���a(ch��n)������٣�������^�Ƽ�...
- 2025Ϳ��ԭ���x�ϴ��
- �Ј���300�|��PMEC China ɫ...
- ����ע�ԣ�2025����������չ...
- ���a���υ��^�A��ӛ���öY��...
- �ۺ���l(f��)���ИI(y��)���g(sh��)��Ӗ����...
- �����ϸ��Լ��ӹ����g(sh��)Ҫ�I(l��ng)��...