���ڣ�����W�����WԺ�����½��ڈF�ᘌ��ϻ����ί��đ�����������DNA�{��ϵ�y����Q�˻�����Ó����ø���f�͵��y�}���о��ɹ��l����Angewandte Chemie�������û��W�������P�������ʹTʿ�о����μ{���鹲ͬ��һ���ߡ��о��õ�������Ȼ�ƌW������Y��֧�֡�

CRISPR/Cas9����һ�N��Ч�Ļ������g���鼲�������ί��������C�����������������������ί���Ԫ������DNAzyme��Ó����ø��������ί�Ч������Ό��F���ί���Ԫ�Ĺ��f�ͣ�������������ԣ����ڼ����ȿɿ�ጷţ����ϻ����ί����P�I��ᘌ��@һ���}��DNA���Ͽ��ṩ���ؽ�Q������ԭ������DNA���Ӿ������пɾ����Ժͷ����R�e�����������������Ժã�������������ί���Ԫ���d�w���ϡ�
��ԓ�о��У��F�ͨ�^�L�h�U��������rolling circle amplification��RCA���ϳ��˳��LDNA��朣�����а���sgRNA�R�e���С�Ó����ø���к�HhaI����ø�R�e���еȶ�N����ģ�K��sgRNA�R�e����ͨ�^�A�����a�䌦���Ì��FCas9/sgRNA�ĸ�Ч�b�d���Mһ�����i�x��ͨ�^�o����Ì��FDNA�L��有��s�M�b���γ�DNA�{�����ӣ��i�x��Ҳ����Ó����ø���o���ӡ������푑��ۺ��������HhaI����øͨ�^�o�������DNA�{���w������M�b���γɼ{�ͺ��w���{�ͺ��w�M�뼚����푑���ø�w�ȵ��|�ӣ�HhaI����ľۺ���Ϳ�ӷֽ⣬ጷų�HhaI����ø���и�DNA��е��R�eλ�c���|�lCas9/sgRNA��Ó����ø��ጷţ������ڻ���ˮƽ���[���������F���{�ء��{�ͺ��w��С�����ٰ�Ƥ����ģ����ȡ�����@���ί�Ч����ͬ�r�������M���������õ����ﰲȫ�ԡ�ԓDNA�{��ϵ�y���Ժܱ������M�����ж����ģ��������������������ߺͺ���ˎ������f�ͣ������M����ˮƽ�����A�����ί�������Ҫ���x��
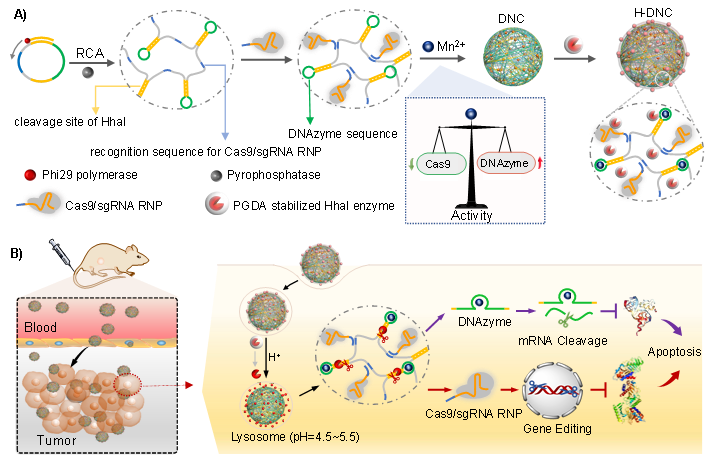
�D1. DNA�{��ϵ�y��Q������Ó����ø���f���y�}�����F�ϻ����ί�
ԭ��朽ӣ�https://doi.org/10.1002/anie.202116569
�������n�}�M����������DNA���о��������۽�DNA���﹦�ܲ��ϻ��W�M�b�c�������죬���������������ͼ����ί���
�n�}�M��퓣�yanglab-dna.com
- ����W Adv. Mater.������DNA�{��ϵ�y����mRNA�DȾ 2023-07-31
- �����d��Ժʿ�F�������/���彭���ԝ����s�������w���zͨ�^�w�Ȱ���Foxo3�����{��ܛ�Ǽ��������w�����Ծ�����P�����Mչ 2025-01-24
- �����d��Ժʿ�F�������/���彭 AM������ܛ�Ǽ����Ŀ�ע�����wFGF18�������ԝ����s�������w���z���ڹ��P�����ί� 2024-01-29
- ������/�����/Ҧ�غ��� AM��DNA�{�ͺ������ڻ���ϵ�y������ί�ԇ���ɿع��f�� 2024-01-19
- �Ĵ���W���������ڈF� Angew: ��ҕ�����ۯB�����D�ǘ����D׃�ğɹ�ۺ������ݼ��������ɫ�����ˎ���f�� 2025-07-11
- ɽ�|��W�������ڈF� ACS Nano: Ӳ�ȿ��{�ľ��Ҷ����{���w���{���{��-��������ã���������ˎ���f�� 2025-06-12
- ���������ڈF� Bioact. Mater.����ˎ���f��ϵ�y"������-����-����ϵ�y���o"��λһ�w�fͬ����ʹ�L���P�����ί� 2025-06-04
